
【题目】体积为1L的某溶液中可能含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 和
和![]() 取该溶液100mL,加入过量NaOH溶液,加热,得到
取该溶液100mL,加入过量NaOH溶液,加热,得到![]() 气体,同时产生的白色沉淀迅速变为灰绿色;过滤、洗涤、灼烧,得到
气体,同时产生的白色沉淀迅速变为灰绿色;过滤、洗涤、灼烧,得到![]() 固体;向上述滤液中加入足量
固体;向上述滤液中加入足量![]() 溶液,得到
溶液,得到![]() 不溶于盐酸的沉淀.下列叙述正确的是()
不溶于盐酸的沉淀.下列叙述正确的是()
A.溶液中的主要离子仅为![]() 、
、![]() 、
、![]()
B.![]() 一定存在,且
一定存在,且![]()
C.向原溶液中加入硫酸,可能有气体生成
D.![]() 、
、![]() 一定不存在,
一定不存在,![]() 可能存在
可能存在
【答案】C
【解析】
加入NaOH溶液共热有气体和白色沉淀,气体为氨气,白色沉淀转化为灰绿色,最后转化为为氢氧化铁,则溶液中一定含有![]() 、
、![]() ,根据离子共存可知不含
,根据离子共存可知不含![]() ,加
,加![]() 溶液生成不溶于盐酸的沉淀,知溶液中含
溶液生成不溶于盐酸的沉淀,知溶液中含![]() ,
,![]() ,知
,知![]() ,n(Fe2O3)=
,n(Fe2O3)=![]() =0.01mol,根据元素守恒,知
=0.01mol,根据元素守恒,知![]() ,n(Ba
,n(Ba
SO4)= ![]() =0.02mol,知
=0.02mol,知![]() , 溶液中
, 溶液中![]() 、
、![]() 所带正电荷为
所带正电荷为![]() ,
,![]() 所带负电荷为
所带负电荷为![]() ,据电荷守恒,知溶液中必然大量存在另一种阴离子,所以
,据电荷守恒,知溶液中必然大量存在另一种阴离子,所以![]() 、硝酸根离子至少存在一种,故原溶液中一定含
、硝酸根离子至少存在一种,故原溶液中一定含![]() 、
、![]() 、
、![]() 和
和![]() 、硝酸根离子中的至少一种,钾离子、铝离子无法判断;
、硝酸根离子中的至少一种,钾离子、铝离子无法判断;
A.原溶液中一定含![]() 、
、![]() 、
、![]() 和
和![]() 、硝酸根离子中的至少一种,故A错误;
、硝酸根离子中的至少一种,故A错误;
B.液中![]() 、
、![]() 所带正电荷为
所带正电荷为![]() ,
,![]() 所带负电荷为
所带负电荷为![]() ,据电荷守恒,知溶液中必然大量存在另一种阴离子,
,据电荷守恒,知溶液中必然大量存在另一种阴离子,![]() 、硝酸根离子中的至少一种,故B错误;
、硝酸根离子中的至少一种,故B错误;
C.向原溶液中加入硫酸,可能存在硝酸根离子,硝酸能将亚铁离子氧化,产生一氧化氮气体,可能有气体生成,故C正确;
D.据以上分析可知,溶液中不能确定是否存在铝离子,故D错误;
故答案选C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列有机物说法不正确的是( )
A. 对甲基苯乙烯中最多有17个原子共面
B. 萘环( )上的一个H原子被-C4H9取代后的产物共有8种
)上的一个H原子被-C4H9取代后的产物共有8种
C. BrCH2CHBrCH2Br的名称为三溴丙烷
D. 立方烷(![]() )一氯代物1种、二氯代物有3种、三氯代物也有3种
)一氯代物1种、二氯代物有3种、三氯代物也有3种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组用0.50mol·L-1NaOH溶液和0.50mol·L-1硫酸进行中和热的测定,测定稀硫酸和稀氢氧化钠溶液反应的中和热的实验装置如图所示:

(1)仪器A的名称为___。
(2)装置中碎泡沫塑料的作用是___。
(3)写出表示该反应中和热的热化学方程式(中和热为57.3kJ·mol-1):___。
(4)取50mLNaOH溶液和30mL硫酸进行实验,实验数据如下表。
实验次数 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差 (t2-t1)/℃ | ||
1 | H2SO4 | NaOH | 平均值 | ||
1 | 26.6 | 26.6 | 26.6 | 29.1 | |
2 | 27.0 | 27.4 | 27.2 | 31.2 | |
3 | 25.9 | 25.9 | 25.9 | 29.8 | |
4 | 26.4 | 26.2 | 26.3 | 30.4 | |
①温度差平均值为___℃。
②近似认为0.50mol·L-1NaOH溶液和0.50mol·L-1硫酸的密度都是1g·cm-3,中和后生成溶液的比热容c=4.18J·(g·℃)-1。则中和热△H=-53.5kJ/mol。
③上述结果与57.3 kJ·mol-1有偏差,产生此偏差的原因可能是___(填字母)。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.一次性把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定硫酸的温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学实验事实及其解释或结论都正确的是![]()
![]()
A.向浓度均为![]() 的
的![]() 、
、![]() 混合溶液中逐滴加入氨水,先生成蓝色沉淀,说明
混合溶液中逐滴加入氨水,先生成蓝色沉淀,说明![]()
B.取少量溶液X,向其中加入适量新制氯水,再加几滴KSCN溶液,溶液变红,说明X溶液中一定含有![]()
C.向![]() 溶液中加入KI溶液,有白色沉淀生成,再加入四氯化碳振荡,四氯化碳层呈紫色,白色沉淀可能为CuI
溶液中加入KI溶液,有白色沉淀生成,再加入四氯化碳振荡,四氯化碳层呈紫色,白色沉淀可能为CuI
D.某待测溶液可能含有等浓度的下列离子中的若干种:![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 。现取少量待测溶液于试管,加入足量NaOH溶液得到白色沉淀,加热产生无色气体,则原溶液中是否含有
。现取少量待测溶液于试管,加入足量NaOH溶液得到白色沉淀,加热产生无色气体,则原溶液中是否含有![]() 、
、![]() ,需通过焰色反应确定
,需通过焰色反应确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由碳、氢、氧3种元素组成的有机物A,相对分子质量为152,其分子中C、H原子个数比为1∶1,氧元素的质量分数为31.58%。A遇FeCl3溶液显紫色,A能与NaHCO3溶液反应,其苯环上的一氯取代物有两种,请回答下列问题:
(1)A的分子式是_______________________________。
(2)A的结构简式为________________________________________。
(3)A可以发生如图所示转化关系,D的分子式为C10H12O3,A与C反应的化学方程式________。

(4)甲、乙两装置均可用作实验室由C制取B的装置,乙图采用甘油浴加热(甘油沸点290 ℃,熔点18.17 ℃),当甘油温度达到反应温度时,将盛有C和浓硫酸混合液的烧瓶放入甘油中,很快达到反应温度。甲、乙两装置相比较,乙装置有哪些优点________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组对人教版教材实验“在200mL烧杯中放入20g蔗糖(C12H22O11),加入适量水,搅拌均匀,然后再加入15mL质量分数为98%浓硫酸,迅速搅拌”进行如下探究;
(1)观察现象:蔗糖先变黄,再逐渐变黑,体积膨胀,形成疏松多孔的海绵状黑色物质,同时闻到刺激性气味,按压此黑色物质时,感觉较硬,放在水中呈漂浮状态,同学们由上述现象推测出下列结论:
①浓硫酸具有强氧化性 ②浓硫酸具有吸水性 ③浓硫酸具有脱水性④浓硫酸具有酸性 ⑤黑色物质具有强吸附性
其中依据不充分的是_________(填序号);
(2)为了验证蔗糖与浓硫酸反应生成的气态产物,同学们设计了如下装置:
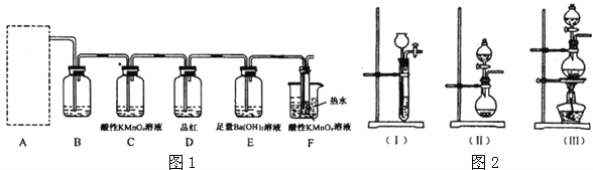
试回答下列问题:
①图1的A中最好选用下列装置_________(填编号);
②图1的 B装置所装试剂是_________;D装置中试剂的作用是_________;E装置中发生的现象是_________;
③图1的A装置中使蔗糖先变黑的化学反应方程式为_________,后体积膨胀的化学方程式为:_________;
④某学生按图2进行实验时,发现D瓶品红不褪色,E装置中有气体逸出,F装置中酸性高锰酸钾溶液颜色变浅,推测F装置中酸性高锰酸钾溶液颜色变浅的原因_________,其反应的离子方程式是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.室温下,向NH4HSO4溶液中加入NaOH溶液至中性,则c(![]() )>c(Na+)>c(
)>c(Na+)>c(![]() )
)
B.体积相等pH=12的氨水和NaOH溶液中和盐酸的能力相同
C.向10ml 0.01mol/L AgNO3溶液中依次滴入2~3滴0.01mol/L NaCl溶液、0.01mol/L NaI溶液,所得沉淀由白色变成黄色,则可推知Ksp(AgI)<Ksp(AgCl)
D.物质的量浓度之比为1:2的CH3COOH和CH3COONa的混合溶液中: 2[c(CH3COOH)+c(CH3COO-)]=3c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列方法中可以说明2HI(g)![]() H2(g)+I2(g)已达到平衡的是:①单位时间内生成n mol H2的同时生成n mol HI;②一个H–H键断裂的同时有两个H–I键断裂;③百分组成ω(HI)=ω(I2);④反应速率υ(H2)=υ(I2)=1/2υ(HI)时;⑤ c(HI):c(H2):c(I2)=2:1:1时;⑥温度和体积一定时,容器内压强不再变化;⑦温度和体积一定时,某一生成物浓度不再变化;⑧条件一定,混合气体的平均相对分子质量不再变化;⑨温度和体积一定时,混合气体的颜色不再变化;⑩温度和压强一定时,混合气体的密度不再变化。( )
H2(g)+I2(g)已达到平衡的是:①单位时间内生成n mol H2的同时生成n mol HI;②一个H–H键断裂的同时有两个H–I键断裂;③百分组成ω(HI)=ω(I2);④反应速率υ(H2)=υ(I2)=1/2υ(HI)时;⑤ c(HI):c(H2):c(I2)=2:1:1时;⑥温度和体积一定时,容器内压强不再变化;⑦温度和体积一定时,某一生成物浓度不再变化;⑧条件一定,混合气体的平均相对分子质量不再变化;⑨温度和体积一定时,混合气体的颜色不再变化;⑩温度和压强一定时,混合气体的密度不再变化。( )
A. ②③⑤ B. ①④⑦ C. ②⑦⑨ D. ⑧⑨⑩
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】葡萄可用于酿酒。
(1)检验葡萄汁含葡萄糖的方法是:向其中加碱调至碱性,再加入新制备的Cu(OH)2,加热,其现象是_______________________________________。
(2)葡萄在酿酒过程中,葡萄糖转化为酒精的过程如下,补充完成下列化学方程式。
C6H12O6(葡萄糖)![]() 2________+2C2H5OH
2________+2C2H5OH
(3)葡萄酒密封储存过程中生成了有香味的酯,酯也可以通过化学实验来制备。实验室用下图所示装置制备乙酸乙酯:

①试管a中生成乙酸乙酯的化学方程式是________________________________。
②试管b中盛放的试剂是饱和_________________溶液。
⑧实验开始时,试管b中的导管不伸入液面下的原因是___________________。
④若分离出试管b中生成的乙酸乙酯,需要用到的仪器是____(填序号)。
a. 漏斗 b. 分液漏斗 c. 长颈漏斗
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com