
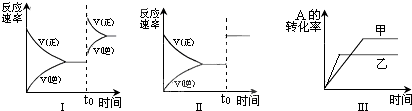
| A、图I研究的是t0时刻增大A的浓度对反应速率的影响 |
| B、图II研究的是t0时刻加入催化剂或增大压强后对反应速率的影响 |
| C、图III研究的是催化剂对平衡的影响,且乙的催化效率比甲高 |
| D、图III研究的是温度对化学平衡的影响,且乙的温度较高 |


 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:
| A、原子序数关系是b<a<d<c<e |
| B、.离子半径关系是d>c>e>b>a |
| C、.原子半径关系是b>a>e>d>c |
| D、.最外层电子数关系为c>d>a>b>e |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、苯和溴苯均为芳香烃 |
| B、酚醛树脂和聚乙烯均为体型高分子材料 |
| C、葡萄糖和麦芽糖均为还原性糖 |
| D、油脂和淀粉均为天然高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、为得到较大的晶体颗粒,结晶时通常采用浓度较低,溶剂蒸发速度较慢或溶液冷却较慢的条件 |
| B、纸层析中,滤纸作为固定相,展开剂作为流动相 |
| C、过滤、结晶、灼烧、萃取、分液和蒸馏等都是常用的分离有机混合物的方法 |
| D、用硝酸银溶液可以鉴别NaCl溶液和NaNO2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 甲、乙两个探究性学习小组,拟在实验室中通过铝与足量的稀硫酸反应生成的氢气来测定铝的摩尔质量.
甲、乙两个探究性学习小组,拟在实验室中通过铝与足量的稀硫酸反应生成的氢气来测定铝的摩尔质量.| 实验前 | 实验后 | |
| 铝铜合金质量/g | m1 | m2 |
| 量液管(C)液面读数/mL | V1 | V2 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com