
【题目】石油铁储罐久置未清洗易引发火灾,经分析研究,事故由罐体内壁附着的氧化物甲与溶于石油中的气态氢化物乙按1:3反应生成的黑色物质丙自燃引起。某研究小组按照以下流程对粉末丙进行研究:
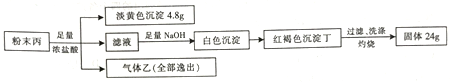
已知:气体乙可溶于水,标准状况下的密度为1.52g/L。
请回答下列问题:
(1)化合物甲的化学式为___________。
(2)化合物丙在盐酸中反应的离子方程式:____________。
(3)化合物丁还可用于氧化法制备高铁酸钾(K2FeO4),试写出在KOH存在条件下用次氯酸钾氧化化合物丁制备高铁酸钾的化学方程式____________。
【答案】 Fe2O3 Fe2S3+4H+=2H2S↑+S↓+2Fe2+ 3KClO+4KOH+2Fe(OH)3=2K2FeO4+3KCl+5H2O
【解析】本题考查无机物推断,涉及物质组成、性质变化、反应特征现象,侧重考查学生分析推理能力、知识迁移应用能力,难度中等。
向丙与浓盐酸反应后的滤液中(假设乙全部逸出)中加入足量的氢氧化钠溶液,先出现白色沉淀最终变为红褐色沉淀,则滤液中含有亚铁离子,灼烧后的固体为氧化铁24克,其物质的量为24/160=0.15mol,则铁的物质的量为0.3mol,丙分投入足量的浓盐酸中发生反应,得到4.8克淡黄色沉淀和气体乙,淡黄色沉淀为硫,物质的量为4.8/32=0.15mol,乙在标况下密度为1.52g/L,则乙的相对分子质量为1.52×22.4=34,气体乙溶于水,说明为硫化氢,在丙中铁元素与硫单质的物质的量比为2:1,而氧化物甲鱼气态氢化物乙按1:3反应生成物质丙,根据元素守恒和电子得失守恒可推断甲为氧化铁,丙为Fe2S3。(1)根据以上分析可知甲为氧化铁,化学式为Fe2O3; (2)化合物丙在盐酸中反应生成硫化氢和硫和氯化亚铁,离子方程式为:Fe2S3+4H+=2H2S↑+S↓+2Fe2+; (3)化合物丁为氢氧化铁,可以在氢氧化钾存在下与次氯酸钾反应生成高铁酸钾,化学方程式为:3KClO+4KOH+2Fe(OH)3=2K2FeO4+3KCl+5H2O。


科目:高中化学 来源: 题型:
【题目】普通锌锰干电池的结构如图所示。回答下列问题。
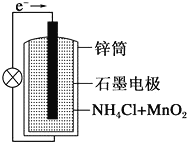
(1) ①电池中电解质溶液为________。
②正极反应式为_______________。
③放电时,NH4+向______(填“正极”或“负极”)移动。
(2)废电池中的锌皮常用于实验室制氢气,废锌皮和纯锌粒分别与同浓度的稀硫酸反应,产生氢气速率较大的是____,原因是____。若用过量的纯锌粒与一定量的稀硫酸反应,为了加快反应速率又不影响产生氢气的量,下列措施可行的是_____(填序号)。
A.微热 B.加入适量氧化铜
C.加入少量硫酸铜溶液 D.加水
E.加入少量氢氧化钡溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列化学反应中既有离子键、极性键、非极性键断裂,又有离子键、极性键、非极性键形成的是( )
A.Cl2+H2O=HClO+HCl
B.Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑
C.2Na2O2+2H2O=4NaOH+O2↑
D.NH4Cl+NaOH![]() NaCl+NH3↑+H2O
NaCl+NH3↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图1所示是某些物质的转化关系图(部分小分子产物没有标出)。

已知:
I.A、B、C是三种常见的气态含碳化合物,A、B的相对分子质量均为28,C的相对分子质量略小于A。
II.化合物D的比例模型如图2所示。
III.硫酸氢乙酯水解得E与硫酸。
V.E与F反应,得一种有浓郁香味的油状液体G,E与D反应得无色液体H。
请按要求回答下列问题:
(1)化合物D所含官能团的名称是______,化合物C的结构简式为__________。
(2)化合物A与F在一定条件下也可发生类似①的反应,其化学方程式为___________。
(3)下列说法正确的是___________。
A.反应①的反应类型是加成反应
B.化合物H可进一步聚合成某种高分子化合物
C.在反应②、③中,参与反应的官能团不完全相同
D.从A经硫酸氢乙酯至E的反应中,硫酸实际起到了催化剂的作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应4NH3(g) + 5O2(g) ![]() 4NO(g) + 6H2O(g),下列叙述正确的是
4NO(g) + 6H2O(g),下列叙述正确的是
A. 化学反应速率关系是:2v正(NH3) = 3v正(H2O)
B. .若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态
C. 达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大
D. 达到化学平衡时,4v正(O2) = 5v逆(NO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】14CuSO4+5FeS2+12H2O =7Cu2S+5FeSO4+12H2SO4说法不正确的是( )
A. Cu2S是还原产物B. 产物中的SO42-有一部分是氧化产物
C. CuSO4是氧化剂,FeS2是还原剂D. 5mol FeS2发生反应,有![]() 21mol 转移
21mol 转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下对比不正确的是
A. 热稳定性:H2O>H2S B. 原子半径:Na>Mg
C. 阴离子的还原性:I->Cl- D. 失电子能力:Na > K
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关甲烷的取代反应的叙述正确的是
A. 甲烷与氯气的物质的量之比为1∶1,混合发生取代反应只生成CH3Cl
B. 甲烷与氯气的取代反应,生成的产物中CH3Cl最多
C. 甲烷与氯气的取代反应生成的产物为混合物
D. 1 mol甲烷生成CCl4最多消耗2 mol氯气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com