
【题目】在给定条件下,下列划线物质在化学反应中能被完全消耗的是( )
A. 用40 mL 10 mol/L浓盐酸与8.7 g 二氧化锰共热制取氯气
B. 标况下,将2.7 g 铝片投入到20 mL 18 mol/L的浓硫酸中
C. 向120 mL 2 mol/L 的盐酸中加入5.6g 铁
D. 向Ba(OH)2和NaOH各0.1 mol的混合溶液中通入标准状况下2.24 L CO2 气体
【答案】C
【解析】试题A、浓盐酸与二氧化锰在加热时发生氧化还原反应,随反应的进行,浓盐酸变为稀盐酸,稀盐酸与二氧化锰不反应,盐酸不会被完全消耗,A错误;B、18mol·L-1的浓硫酸在标况下能与Al发生钝化,生成的致密氧化物薄膜阻止反应的进一步发生,Al不会被完全反应掉,B错误;C、n(Fe)=![]() =0.1mol,n(HCl)=0.1L×3mol·L-1=0.3mol,由Fe+2HCl═FeCl2+H2↑可知,铁在化学反应中能被完全消耗,C正确;D、n(CO2)=
=0.1mol,n(HCl)=0.1L×3mol·L-1=0.3mol,由Fe+2HCl═FeCl2+H2↑可知,铁在化学反应中能被完全消耗,C正确;D、n(CO2)=![]() =0.125mol,先发生CO2+Ba(OH)2═BaCO3↓+H2O,消耗掉0.1molCO2,再发生CO2+2OH-═CO32-+H2O,则NaOH在反应中不会被完全消耗,D错误;选C.
=0.125mol,先发生CO2+Ba(OH)2═BaCO3↓+H2O,消耗掉0.1molCO2,再发生CO2+2OH-═CO32-+H2O,则NaOH在反应中不会被完全消耗,D错误;选C.


科目:高中化学 来源: 题型:
【题目】中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%.
(1)有效“减碳”的手段之一是节能,下列制氢方法最节能的是
A.电解水制氢:2H2O ![]() 2H2↑+O2↑
2H2↑+O2↑
B.高温使水分解制氢:2H2O ![]() 2H2↑+O2↑
2H2↑+O2↑
C.太阳光催化分解水制氢:2H2O ![]() 2H2↑+O2↑
2H2↑+O2↑
D.天然气制氢:CH4+H2O ![]() CO+3H2
CO+3H2
(2)CO2可转化成有机物实现碳循环.在体积为1L的密闭容器中,充入1molCO2和3mol H2 , 一定条件下反应:CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H=﹣49.0kJmol﹣1 , 测得CO2和CH3OH(g)的浓度随时间变化如图所示. ①从3min到9min,v(H2)=molL﹣1min﹣1
②能说明上述反应达到平衡状态的是(填编号).
A.反应中CO2与CH3OH的物质的量浓度之比为1:1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.单位时间内消耗3mol H2 , 同时生成1mol HO
D.CO2的体积分数在混合气体中保持不变.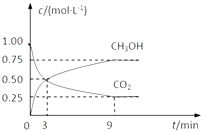
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在有机化学中,同分异构是普遍存在现象.分子式为C4H9Br的有机物共有种.其中,一种有机物通过消去反应可转变为2﹣丁烯,请写出该消去反应的化学方程式 , 另一种有机物的核磁共振氢谱图(1H核磁共振谱图)中显示一个峰,请写出该有机物的结构简式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛酸钡是一种强介电化合物材料,具有高介电常数和低介电损耗,是电子陶瓷中使用最广泛的材料之一,被誉为“电子陶瓷工业的支柱”,工业制取方法如下,先获得不溶性草酸氧钛钡晶体[BaTiO(C2O4)2·4H2O],煅烧后可获得钛酸钡粉体。

(1)酸浸时发生的反应的离子方程式为__________________;
(2)配制TiCl4溶液时通常将TiCl4固体溶于浓盐酸再加水稀释,其目的是_________________________;
(3)加入H2C2O4溶液时,发生反应的化学方程式为____________________;可循环使用的物质X是________(填化学式),设计实验方案验证草酸氧钛钡晶体是否洗涤干净:_______________________;
(4)煅烧草酸氧钛钡晶体得到BaTiO3的同时,生成高温下的气体产物有CO、_______和_________;
(5)工业上用饱和Na2CO3溶液处理重晶石(主要成分是BaSO4),待达到平衡后,移走上层清液,重复多次操作,将其转化为易溶于酸的BaCO3,再由BaCO3制备其它钡盐。已知常温下:Ksp(BaSO4)=1.0×10-10,Ksp(BaCO3)=2.58×10-9,请问至少需要______ mol·L-1的碳酸钠溶液浸泡才能实现上述转化(忽略CO32-的水解)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.向氨水通入足量SO2:SO2+2NH3H2O═2NH4++SO32﹣+H2O
B.将Ba(OH)2溶液滴入NaHSO4溶液中至SO42﹣恰好完全沉淀:Ba2++SO42﹣+2OH﹣+2H+═BaSO4↓+2H20
C.向醋酸溶液中滴加过量NaOH溶液:H++OH﹣═H2O
D.向新制Cu(OH)2悬浊液中加入乙醛溶液并加热:CH3CHO+2Cu(OH)2+OH﹣ ![]() CH3COO﹣+Cu2O↓+3H2O
CH3COO﹣+Cu2O↓+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家最近成功合成了世界上首个五氮阴离子盐![]() (用
(用![]() 代表).回答下列问题:
代表).回答下列问题:
(1)氮原子价层电子对的轨道表达式(电子排布图)为________.
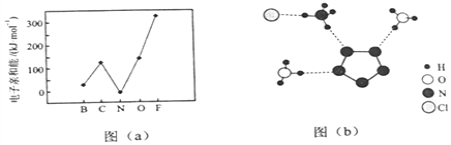
(2)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能![]() .第二周期部分元素的
.第二周期部分元素的![]() 变化趋势如图
变化趋势如图![]() 所示,其中除氮元素外,其他元素的
所示,其中除氮元素外,其他元素的![]() 自左而右依次增大的原因是________;氮元素的
自左而右依次增大的原因是________;氮元素的![]() 呈现异常的原因是________.
呈现异常的原因是________.
(3)经![]() 射线衍射测得化合物
射线衍射测得化合物![]() 的晶体结构,其局部结构如图
的晶体结构,其局部结构如图![]() 所示.
所示.
①从结构角度分析, ![]() 中两种阳离子的相同之处为________,不同之处为________.(填标号)
中两种阳离子的相同之处为________,不同之处为________.(填标号)
![]() .中心原子的杂化轨道类型
.中心原子的杂化轨道类型 ![]() .中心原子的价层电子对数
.中心原子的价层电子对数
![]() .立体结构
.立体结构 ![]() .共价键类型
.共价键类型
②![]() 中阴离子
中阴离子![]() 中的
中的![]() 键总数为________个.分子中的大
键总数为________个.分子中的大![]() 键可用符号
键可用符号![]() 表示,其中
表示,其中![]() 代表参与形成的大
代表参与形成的大![]() 键原子数,
键原子数, ![]() 代表参与形成的大
代表参与形成的大![]() 键电子数(如苯分子中的大
键电子数(如苯分子中的大![]() 键可表示为Π
键可表示为Π![]() ),则
),则![]() 中的大
中的大![]() 键应表示为________.
键应表示为________.
③图![]() 中虚线代表氢键,其表示式为
中虚线代表氢键,其表示式为![]() 、________、________.
、________、________.
(4)![]() 的晶体密度为
的晶体密度为![]() ,其立方晶胞参数为
,其立方晶胞参数为![]() ,晶胞中含有
,晶胞中含有![]() 个
个![]() 单元,该单元的相对质量为
单元,该单元的相对质量为![]() ,则
,则![]() 的计算表达式为________.
的计算表达式为________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com