
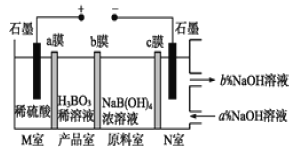
【题目】现代膜技术可使某种离子具有单向通过能力,常用于电解池、原电池中。电解NaB(OH)4溶液可制备H3BO3,其工作原理如图。下列叙述错误的是
A.M室发生的电极反应式:2H2O-4e-=O2↑+4H+
B.产品室发生的反应是:B(OH)4-+H+![]() H3BO3+H2O
H3BO3+H2O
C.理论上每生成1 mol产品,阴极室可生成标准状况下5.6 L气体
D.b膜为阴离子交换膜
【答案】C
【解析】
与电源正极相连的石墨电极为阳极,H2O失电子生成H+和O2,H+通过a膜进入产品室,则a膜为阳膜;与电源负极相连的石墨电极为阴极,H2O得电子生成H2和OH-,从NaOH溶液的流向看,其浓度应增大,所以Na+通过c膜流向N室,c膜为阳膜;B(OH)4-通过b膜流向产品室,则b膜为阴膜。
A. 通过以上分析可知,M室H2O失电子生成H+和O2,则发生的电极反应式为:2H2O-4e-=O2↑+4H+,A正确;
B. 产品室中,通过a膜进入的H+与通过b膜进入的B(OH)4-发生反应,B(OH)4-+H+![]() H3BO3+H2O,B正确;
H3BO3+H2O,B正确;
C. 理论上每生成1 mol H3BO3,通过b膜的B(OH)4-为1mol,通过c膜的Na+为1mol,则生成OH-为1mol,N室电极反应式为2H2O+2e-=2OH-+H2↑,从而得出阴极室可生成H2 0.5mol,标准状况下体积为11.2 L,C不正确;
D. 由以上分析可知,b膜为阴离子交换膜,D正确;
故选C。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】2010年10月30日曲美减肥胶囊全国下架,主要成分在欧美被禁。其主要成分盐酸西布曲明的结构如右图所示,有关说法错误的是( )
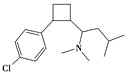
A.分子式:C17H26ClN
B.水解产物之一可用FeCl3溶液检验
C.该物质共平面的原子不少于12个
D.属于芳香烃类,可与3 mol H2加成,不溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设![]() 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是
A.标准状况下,将![]() 通入足量水中,生成
通入足量水中,生成![]() 的分子数为
的分子数为![]()
B.铁与稀硝酸反应生成的气体产物仅有![]() ,转移的电子数一定为
,转移的电子数一定为![]()
C.15g乙烷与1mol氯气充分反应,所得有机物中含有的氯原子数为![]()
D.![]() 中含有的质子数和中子数均为
中含有的质子数和中子数均为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃、101 kPa下,2g氢气燃烧生成液态水,放出285.8kJ热量,表示该反应的热化学方程式正确的是( )
A. 2H2(g)+O2(g) == 2H2O(1) △H= ―285.8kJ/mol![]()
B. 2H2(g)+ O2(g) == 2H2O(1) △H= +571.6 kJ/mol
C. 2H2(g)+O2(g) == 2H2O(g) △H= ―571.6 kJ/mol
D. H2(g)+1/2O2(g) == H2O(1) △H= ―285.8kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在固定容积的密闭容器中,可逆反应:mA(g)+nB(g)![]() pCg)+qD(g),当m、n、p、q为任意正整数时,下列状态:①体系的压强不再发生变化,②体系的密度不再发生变化,③各组分的物质的量浓度不再改变,④各组分的质量分数不再改变,⑤反应速率vA:vB:vC:vD=m:n:p:q,其中,能说明反应已达到平衡的是( )
pCg)+qD(g),当m、n、p、q为任意正整数时,下列状态:①体系的压强不再发生变化,②体系的密度不再发生变化,③各组分的物质的量浓度不再改变,④各组分的质量分数不再改变,⑤反应速率vA:vB:vC:vD=m:n:p:q,其中,能说明反应已达到平衡的是( )
A.只有③④B.②③④C.①②③④D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盖斯定律在生产和科学研究中有很重要的意义。已知3.6g碳在6.4g氧气中燃烧,至反应物耗尽,放出了X kJ热量。已知碳完全燃烧的焓变△H= 一Y kJ·mol-1,则lmol C与O2反应生成CO的反应热△H为 ( ) kJ·mol-1
A.一Y B.—(10X—Y) C.一(5X—O.5Y) D.+(10X—Y)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】50mL 18mol/L的硫酸中加入足量的铜片并加热,被还原的硫酸的物质的量
A. 小于0.45mo1B. 等于0.45molC. 在0.45mol和0.9mol之间D. 大于0.9mo1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设![]() 表示阿伏加德罗常数,下列说法正确的是
表示阿伏加德罗常数,下列说法正确的是
A.![]() 和CO的混合物中,所含分子总数为
和CO的混合物中,所含分子总数为![]()
B.精炼铜时,阳极质量减少64g时转移电子数![]()
C.![]() 时,
时,![]() 的纯水中,含
的纯水中,含![]() 数为
数为![]()
D.![]() 溶液中含
溶液中含![]() 数为
数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】正确掌握化学用语是学好化学的基础.下列化学用语中不正确的是( )
A. 乙烯的结构简式CH2=CH2 B. CH4分子的球棍模型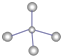
C. Ca2+的结构示意图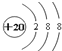 D. 乙醇的分子式C2H6O
D. 乙醇的分子式C2H6O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com