
A、
| ||
B、
| ||
| C、2.5dmol/L | ||
| D、1.25dmol/L |
| m |
| ρ |
| n |
| V |
| 1g |
| 40g/mol |
| 20g |
| dg/cm3 |
| 10-3L |
| mL |
| 1 |
| 50d |
| 0.05mol | ||
|


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
| A、Na+、H+、SO42-、OH- |
| B、K+、Ca2+、CO32-、NO3- |
| C、Na+、H+、Cl-、CO32- |
| D、K+、Cu2+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| m |
| n |
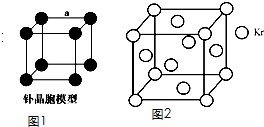
查看答案和解析>>
科目:高中化学 来源: 题型:
A、饱和溶液的物质的量浓度为c=
| ||
B、25℃时R的溶解度为S=
| ||
C、饱和溶液中溶质的质量分数为W=
| ||
D、饱和溶液的密度为ρ=
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硝酸和澄清石灰水的反应 |
| B、盐酸和氢氧化镁的反应 |
| C、硫酸和氢氧化钡的反应 |
| D、盐酸和氨水的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用一束激光照射胶体和溶液都有光亮的通路 |
| B、制备氢氧化铁胶体时加入的饱和氯化铁溶液越多越好 |
| C、用过滤的方法不能分离氢氧化铁胶体和氯化铁溶液 |
| D、向氢氧化铁胶体中加入过量盐酸后出现红褐色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
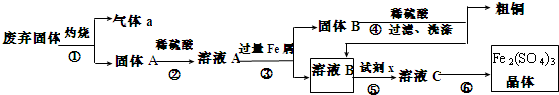
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com