
【题目】如图是实验室制备氯气并进行一系列相关实验的装置(夹持装置已略)。
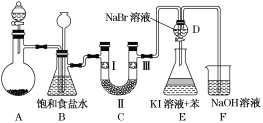
(1)制备氯气选用的试剂为漂粉精固体和浓盐酸,则相关反应的化学方程式为________________。
(2)装置B中饱和食盐水的作用是__________________________________;
同时装置B也是安全瓶,监测实验进行时装置C是否发生堵塞,请写出发生堵塞时装置B中的现象: __________________________________________。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此装置C中Ⅰ、Ⅱ、Ⅲ处依次放入________(填字母)。
a | b | c | d | |
Ⅰ | 干燥的 有色布条 | 干燥的 有色布条 | 湿润的 有色布条 | 湿润的 有色布条 |
Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
Ⅲ | 湿润的 有色布条 | 湿润的 有色布条 | 干燥的 有色布条 | 干燥的 有色布条 |
(4)设计装置D、E的目的是比较氯、溴、碘的非金属性。当向D装置中缓缓通入一定量氯气时,可以看到无色溶液逐渐变为______色,说明氯的非金属性强于溴。
(5)打开活塞,将装置D中少量溶液加入装置E中,振荡后静置。观察到的现象是________。
【答案】Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O 除去Cl2中的HCl 长颈漏斗中液面上升,形成水柱 d 棕黄 装置E中液体分为两层,上层(苯层)为紫红色
【解析】
A装置来制备Cl2,制得的Cl2中含有HCl气体,利用饱和食盐水除去HCl,B中的长颈漏斗平衡内外压强,可以防倒吸,也可以判断后面的装置中是否发生了堵塞。装置C用于进行Cl2的性质实验。在D中Cl2与NaBr反应置换出Br2,Br2再与KI溶液反生置换出I2,I2被苯萃取,上层为紫红色;利用NaOH处理尾气。
(1)根据氧化还原反应的规律,次氯酸钙与浓盐酸反应生成氯化钙、氯气与水,反应的化学方程式为Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O;
(2)浓盐酸易挥发,反应制取的氯气中含有HCl,装置B中饱和食盐水的作用是除去Cl2中的HCl;
若装置C发生堵塞,装置B中的压强会增大,长颈漏斗中液面上升,形成水柱;
(3)验证氯气是否具有漂白性,要对比验证干燥氯气和湿润氯气有无漂白性,因此Ⅰ处应为湿润的有色布条,Ⅱ处应为干燥剂,Ⅲ处应为干燥的有色布条,U形管中应用固体干燥剂,综上d符合;
(4)当向装置D中缓缓通入少量氯气时,可以看到无色溶液逐渐变为棕黄色,发生反应:Cl2+2NaBr=2NaCl+Br2;
(5)打开活塞,将装置D中含Br2的少量溶液加入装置E中,发生反应:Br2+2KI=2KBr+I2,碘单质溶于苯,呈紫红色,振荡后静置,观察到的现象是装置E中液体分为两层,上层(苯层)为紫红色。


科目:高中化学 来源: 题型:
【题目】下列实验、实验现象和相应结论都正确的是
实验 | 现象 | 结论 | |
A | 向1mL | 溶液分层,上层溶液显紫色。 | 氧化性:Fe3+>I2 |
B | 将两块表面积相等的Mg条和Al条放入同浓度同体积的NaOH溶液中。 | Al条产生气泡的速度快。 | 金属性:Al>Mg |
C | 向烧杯中加入一定体积蒸馏水,加热至沸腾时,向其中逐滴滴加饱和FeCl3溶液。 | 得到红褐色透明液体。 | 制得了氢氧化铁胶体。 |
D | 向盛有10 mL溴水的分液漏斗中加入10mL苯,振荡、静置。 | 溶液分为两层,上层为橙色。 | 溴在苯中的溶解能力大于水中。 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某含有![]() 的澄清溶液中,可能还含有
的澄清溶液中,可能还含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 六种离子中的几种。将该溶液进行如下实验:
六种离子中的几种。将该溶液进行如下实验:![]() 滴加适量新制氯水,有气泡生成,溶液变黄色;
滴加适量新制氯水,有气泡生成,溶液变黄色;![]() 向“
向“![]() ”中所得溶液中加入
”中所得溶液中加入![]() 溶液,无沉淀生成;
溶液,无沉淀生成;![]() 向“
向“![]() ”中所得溶液中加入淀粉溶液,不显蓝色。依据上述实验事实推断该溶液中
”中所得溶液中加入淀粉溶液,不显蓝色。依据上述实验事实推断该溶液中![]()
A.一定存在![]() 、
、![]() 、
、![]() B.无法确定
B.无法确定![]() 的存在
的存在
C.一定不存在![]() 、
、![]() 、
、![]() D.一定存在
D.一定存在![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题
(1)已知25℃,NH3·H2O的Kb=1.8×105,H2SO3的Ka1=1.3×102,Ka2=6.2×108。将SO2通入2.0 mol·L-1氨水中(溶液的体积保持不变),当c(OH)降至1.0×107 mol·L1时,溶液中的![]() =______;(NH4)2SO3溶液中的质子守恒_______。
=______;(NH4)2SO3溶液中的质子守恒_______。
(2)土壤的pH一般在4~9之间。土壤中Na2CO3含量较高时,pH可高达10.5,试用离子方程式解释土壤呈碱性的原因为________________(用离子反应方程式)。加入石膏(CaSO4·2H2O)可以使土壤碱性降低,有关反应的化学方程式为________。
(3)SOCl2是一种液态化合物,沸点为77℃化合物,在盛有10mL水的锥形瓶中小心滴加8~10滴SOCl2,可观察到剧烈水解反应,液面有白雾形成,并有刺激性气味的气体逸出,该气体可使滴有品红试液的滤纸褪色,轻轻振荡锥形瓶,等白雾消失后,往溶液中滴加AgNO3溶液,有不溶于HNO3的白色沉淀析出。
①根据上述实验,写出 SOCl2和水反应的化学方程式________________。
②SOCl2与AlCl3·6H2O 混合共热,可得到无水AlCl3,其原因是__________。
(4)当意外失火时,将泡沫灭火器倒过来即可使药液混合,喷出泡沫状物品,阻止火势蔓延,其相关的离子反应方程式为___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下:
实验装置 |
|
|
部分实验现象 | a极质量减小b极质量增加 | b极有气泡产生c极无变化 |
实验装置 |
|
|
部分实验现象 | d极溶解c极有气泡产生 | 电流从a极流向d极 |
由此判断这四种金属的活动性顺序是( )
A. a>b>c>dB. d>a>b>cC. b>c>d>aD. a>b>d>c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表示正确的是( )
A.离子结构示意图:![]() 可以表示16O2-,也可以表示18O2-
可以表示16O2-,也可以表示18O2-
B.比例模型![]() 表示CH4分子或CCl4分子
表示CH4分子或CCl4分子
C.乙烯的结构简式:CH2CH2
D.硅的分子式:Si
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(化学——选修5:有机化学基础)我国第二代身份证采用的是具有绿色环保性能的PETG新材料,PETG新材料可以回收再利用,而且对周边环境不构成任何污染。PETG的结构简式如下:
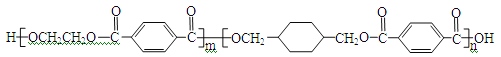
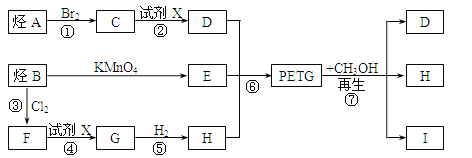
这种材料可采用如下图所示的合成路线:
已知:(1)![]()
(2)RCOORl+R2OH→RCOOR2+R1OH(R、R1、R2表示烃基)
试回答下列问题:
(1)⑥的反应类型是____,试剂X为_______,E中官能团的名称为_______。
(2)写出I的结构简式:__________________。
(3)合成时应控制的单体的物质的量:n(D)∶n(E)∶n(H)=___________(用m、n表示)。
(4)写出反应③的化学方程式:_____________________。
(5)与G的分子式相同,且只含有一个酚羟基的同分异构体(醚类除外)有_______种,其中核磁共振氢谱有6种不同类型的吸收峰,且峰的面积之比为1∶1∶1∶2∶2∶3的结构简式为_____。
(6)D和E在催化剂作用下可生产一种聚酯纤维——涤纶,请写出生产该物质的化学方程式________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠是一种重要的化工产品。某兴趣小组拟制备硫代硫酸钠晶体(Na2S2O3·5H2O)。
Ⅰ. [查阅资料]
(1)Na2S2O3·5H2O是无色透明晶体,易溶于水。其稀溶液与BaCl2溶液混合无沉淀生成。
(2)向Na2CO3和Na2S混合液中通入SO2可制得Na2S2O3,所得产品中常含有少量Na2SO3和Na2SO4。
(3)Na2SO3易被氧化;BaSO3难溶于水,可溶于稀HCl。
(4)硫代硫酸钠与碘反应的离子方程式为:2![]() +I2=
+I2=![]() +2I
+2I
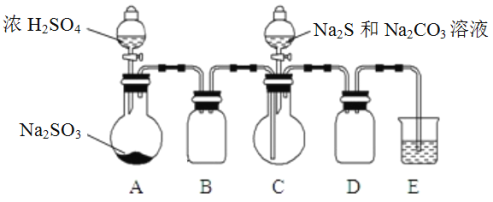
Ⅱ. [制备产品]实验装置如图所示(省略夹持装置)
实验步骤:
(1)按如图所示组装好装置后,应先_________________________________________(填操作名称),再按图示加入试剂。仪器B和D的作用是__________________________________________;
(2)先向烧瓶C中加入Na2S和Na2CO3混合溶液,再向烧瓶A中滴加浓H2SO4。C中反应生成Na2S2O3和CO2,化学方程式为____________________________________________________________________。
(3)待Na2S和Na2CO3完全消耗后,结束反应。过滤C中混合液,滤液经蒸发、结晶、过滤、洗涤、干燥、得到产品。
Ⅲ. [探究与反思]
(4)用I2的标准溶液测定产品的纯度。取10.0g产品,配制成100mL溶液,配制溶液的蒸馏水必须经过煮沸、冷却后才能使用,其目的是杀菌、除_______________________________及二氧化碳。取10.00mL溶液。以________________________________溶液为指示剂,用浓度为0.10 mol/L I2的标准溶液进行滴定,相关数据记录如下表所示。
编号 | 1 | 2 | 3 |
溶液的体积/mL | 10.00 | 10.00 | 10.00 |
消耗I2标准溶液的体积/mL | 19.95 | 17.10 | 20.05 |
滴定时,达到滴定终点的现象是___________________________。Na2S2O3·5H2O在产品中的质量分数是____________________________________(用百分数表示,且保留1位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种无机物具有如图所示的转化关系(反应条件及反应中的水均略去),且A、B、C含有同一种元素。下列说法错误的是
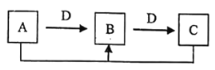
A.若A的溶液显碱性,则D可能是单质
B.A与C的反应可能是非氧化还原反应
C.A或D可能是目前使用最广泛的金属单质
D.若C是能使澄清石灰水变浑浊的气体,则A一定是单质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com