
【题目】A、B、C、D四种无机物具有如图所示的转化关系(反应条件及反应中的水均略去),且A、B、C含有同一种元素。下列说法错误的是
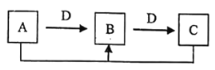
A.若A的溶液显碱性,则D可能是单质
B.A与C的反应可能是非氧化还原反应
C.A或D可能是目前使用最广泛的金属单质
D.若C是能使澄清石灰水变浑浊的气体,则A一定是单质
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A. 因为二氧化硫具有漂白性,所以它能使品红溶液、溴水、高锰酸钾溶液褪色
B. 100mL0.5mol/LH2O2溶液与足量SO2完全反应,转移的电子数为0.1NA
C. 二氧化硫、Cl2以及活性炭都能使红墨水褪色,其原理不同
D. 等物质的量的二氧化硫和氯气相遇在溶液中具有更强的漂白能力
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤族元素包括F、Cl、Br等元素。
(1)下列曲线表示卤族元素某种性质随核电荷数的变化趋势,正确的是_______。
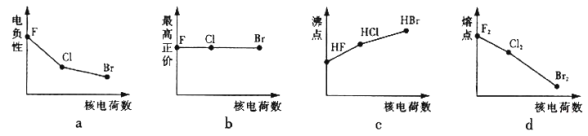
(2)在测定HF的相对分子质量时,实验测定值一般高于理论值的主要原因是______________。
(3)BCl3和NCl3中心原子的杂化方式是否相同_____________(填 是 或 否)。第一电离能介于B、N之间的第二周期元素有_______种。
(4)铑(Rh)与碘属于同周期元素。铑的某配合物的化学式为CsRh(SO4)2,该物质易溶于水,向其水溶液中加入一定浓度的BaCl2溶液,无沉淀生成,该盐溶于水的电离方程式为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有X、Y、Z三种元素,已知:①X、Y、Z的单质在常温下均为气体;②X单质可在Z单质中燃烧,生成XZ,火焰为苍白色;③XZ极易溶于水,其水溶液可使蓝色石蕊试纸变红;④每2个X2分子可与1个Y2分子化合生成2个X2Y分子,X2Y在常温下为液体;⑤Z单质溶于X2Y中,所得溶液具有漂白作用;⑥细铁丝能在Z2(g)中剧烈燃烧,且产生红棕色烟。推断:
(1)X、Y两种元素的名称X___,Y___。
(2)化合物的化学式:XZ___,X2Y___。
(3)过程⑥中涉及的化学反应方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学应用如下所示装置研究物质的性质。其中气体X的主要成分是氯气,还含有少量空气和水蒸气。请回答下列问题:
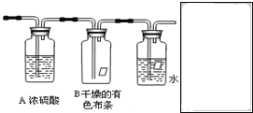
(1)B中观察到的实验现象是___。
(2)从物质性质方面来看,这样的实验设计还存在事故隐患,应如何处理,请画出装置图(填在图方框内),用化学方程式表达原理___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对![]() 的性质进行探究,设计了以下实验
的性质进行探究,设计了以下实验

已知:![]() 、
、![]() 、
、![]() 等称之为拟卤素,它们的化学性质均与卤素单质相似。下列说法正确的是
等称之为拟卤素,它们的化学性质均与卤素单质相似。下列说法正确的是
A.溶液颜色变红时发生反应的离子方程式是:![]()
B.红色溶液褪色表现了![]() 的漂白性
的漂白性
C.氧化性:![]()
D.无色溶液Ⅱ中滴入适量的![]() 溶液,溶液又变成红色
溶液,溶液又变成红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数,下列叙述正确的是( )
A. 标准状况下,22.4L H2O含有的分子数为1 NA
B. 常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA
C. 常温常压下,1 NA 个CO2分子占有的体积为22.4L
D. 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl- 个数为1 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验室需要1.500 mol·L-1硫酸溶液450 mL。根据溶液的配制情况回答下列问题:
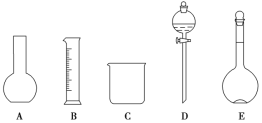
(1)如图所示的仪器中配制溶液肯定不需要的是______(填序号),配制上述溶液还需用到的玻璃仪器是________(填仪器名称)。
(2)现用质量分数为98%、密度为1.84 g·cm-3的浓硫酸来配制450 mL 1.50 mol·L-1的稀硫酸。计算所需浓硫酸的体积为________ mL (保留1位小数),现有 ①10 mL ②25 mL ③50 mL ④100 mL四种规格的量筒,最好选用的量筒是________(填代号)。
(3)配制时,一般可分为以下几个步骤:
①量取 ②计算 ③稀释 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却
其正确的操作顺序为:②→①→③→___→_____→_____→______→④(填序号)。
(4)在配制过程中,下列操作中会导致所配制的溶液浓度偏高的有________。
①用量筒量取浓硫酸时候,俯视刻度线
②洗涤量取浓硫酸后的量筒,并将洗涤液转移到容量瓶中
③转移前,容量瓶中含有少量蒸馏水
④定容时,俯视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温、容积为2L的密闭容器中通入1 mol X和2 mol Y,发生反应:X(g)+2Y(g)![]() M(g) ΔH=-a kJ/mol(a>0),5 min末测得M的物质的量为0.4 mol。则下列说法正确的是
M(g) ΔH=-a kJ/mol(a>0),5 min末测得M的物质的量为0.4 mol。则下列说法正确的是
A. 0~5 min,Y的平均反应速率为0.08 mol·L-1·min-1
B. 当容器中混合气体密度不变时达到平衡状态
C. 平衡后升高温度,X的反应速率降低
D. 到达平衡状态时,反应放出的热量为a kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com