
【题目】已知下列热化学方程式:
①H2(g)+![]() O2(g)=H2O(l);△H=﹣285kJ/mol
O2(g)=H2O(l);△H=﹣285kJ/mol
②H2O(g)=H2(g)+![]() O2(g);△H=+241.8kJ/mol
O2(g);△H=+241.8kJ/mol
③C(s)+![]() O2(g)=CO(g);△H=﹣110.4kJ/mol
O2(g)=CO(g);△H=﹣110.4kJ/mol
④C(s)+O2(g)=CO2(g);△H=﹣393.5kJ/mol
回答下列各问:
(1)上述反应中属于放热反应的是 .(用序号填写)
(2)C的燃烧热为 .
(3)燃烧10g H2生成液态水,放出的热量为 .
(4)CO的燃烧热的热化学方程式为 .
【答案】(1)①③④;(2)393.5kJ/mol;(3)1425 kJ;
(4)CO(g)+![]() O2(g)=CO2(g)△=﹣283.1kJ/mol.
O2(g)=CO2(g)△=﹣283.1kJ/mol.
【解析】(1)热化学方程式中△H为负值的反应为放热反应,△H为正值的为吸热反应:①H2(g)+![]() O2(g)=H2O(l);△H=﹣285kJ/mol
O2(g)=H2O(l);△H=﹣285kJ/mol
②H2O(g)=H2(g)+![]() O2(g);△H=+241.8kJ/mol
O2(g);△H=+241.8kJ/mol
③C(s)+![]() O2(g)=CO(g);△H=﹣110.4kJ/mol
O2(g)=CO(g);△H=﹣110.4kJ/mol
④C(s)+O2(g)=CO2(g);△H=﹣393.5kJ/mol
以上4个反应①③④为放热反应,②为吸热反应,故答案为:①③④;
(2)1mol纯净物完全燃烧生成稳定的氧化物所放出的热量为燃烧热,C的燃烧热为393.5kJ/mol
(3)依据反应①进行计算燃烧10g H2生成液态水放出的热量;
H2(g)+![]() O2(g)=H2O(l)△H=﹣285kJmol﹣1
O2(g)=H2O(l)△H=﹣285kJmol﹣1
2g 285kJ
10g Q
Q=![]() =1425kJ,故答案为:1425 kJ;
=1425kJ,故答案为:1425 kJ;
(4)③C(s)+![]() O2(g)=CO(g);△H=﹣110.4kJ/mol
O2(g)=CO(g);△H=﹣110.4kJ/mol
④C(s)+O2(g)=CO2(g);△H=﹣393.5kJ/mol
依据盖斯定律④﹣③得到CO(g)+![]() O2(g)=CO2(g)△=﹣283.1kJ/mol;
O2(g)=CO2(g)△=﹣283.1kJ/mol;


科目:高中化学 来源: 题型:
【题目】下列有关钠的物理性质的叙述中正确的是( )
①银白色金属 ②质软,可以用小刀切割 ③熔点低 ④密度比水小 ⑤热和电的良导体
A. ①②④ B. ①②③④ C. ①③④ D. ①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2016新课标2】 [化学--选修5:有机化学基础]氰基丙烯酸酯在碱性条件下能快速聚合为![]() ,从而具有胶黏性,某种氰基丙烯酸酯(G)的合成路线如下:
,从而具有胶黏性,某种氰基丙烯酸酯(G)的合成路线如下:
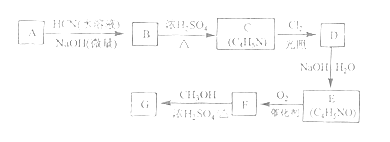
已知:①A的相对分子量为58,氧元素质量分数为0.276,核磁共振氢谱显示为单峰
②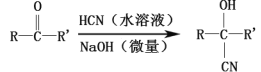
回答下列问题:
(1)A的化学名称为_______。
(2)B的结构简式为______,其核磁共振氢谱显示为______组峰,峰面积比为______。
(3)由C生成D的反应类型为________。
(4)由D生成E的化学方程式为___________。
(5)G中的官能团有_____、 _____ 、_____。(填官能团名称)
(6)G的同分异构体中,与G具有相同官能团且能发生银镜反应的共有_____种。(不含立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(l)基态As原子的核外电子排布式为[Ar]______,有________个未成对电子。
(2) As与N是同主族元素,从原子结构角度分析:为什么As的最高价含氧酸H3AsO4是三元酸(含三个轻基),而N的最高价含氧酸HNO3是一元酸(只含一个烃基)______。
(3)比较下列氢化物的熔点和沸点,分析其变化规律及原因__________。
(4) Na3AsO3中Na、As、O电负性由大至小的顺序是______。AsO33-的空间构型为___, AsO33-中As的杂化轨道类型为_______杂化。
(5)砷化稼(GaAs)为黑灰色固体,熔点为1238℃。该晶体属于___晶体,微粒之间存在的作用力是_________。
NH3 | PH3 | AsH3 | SbH3 | |
熔点/K | 195.3 | 140.5 | 156.1 | 185 |
沸点/K | 239.6 | 185.6 | 210.5 | 254.6 |
(6)图为GaAs的晶胞,原子半径相对大小是符合事实的,则白球代表____原子。
己知GaAs的密度为5.307g·cm3, Ga和As的相对原子质量分别为69.72、74.92,求晶胞参数a=______pm (列出计算式即可)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤作为主要的能源物质,在国民生产和生活中起重要作用,但直接排放煤燃烧产生的烟气会引起严重的环境问题,将烟气通过装有石灰石(主要成分:CaCO3)浆液的脱硫装置可以除去其中的 SO2气体,最终生成硫酸钙。硫酸钙可在如图所示的循环燃烧装置的燃料反应器中与甲烷反应,气体产物分离出水后得到几乎不含杂质的二氧化碳,从而有利于 CO2的回收利用,达到减少碳排放的目的。

请回答下列问题:
(1)煤燃烧产生的烟气直接排放在空气中,不会引发的环境问题是(______)
A. 温室效应 B. 酸雨 C. 粉层污染 D. 水体富营养化
(2)在烟气脱硫的过程中,所用的石灰石浆液在进入脱硫装置前,需通过一段时间的CO2,以增加脱硫效率;脱硫时控制浆液的pH值,此时浆液含有的Ca(HSO3)2可以快速被氧化为CaSO4。
①从分子结构看,CO2是由_____ 共价键构成的_____分子(选填:“极性”或“非极性”)。它与石灰石浆液反应的属于 _________反应。(选填“化合”、“分解”、“置换”、“复分解”),固体的CO2被称为干冰,其受热很容易_______。(填一种物理现象)
②Ca(HSO3)2从晶体类型看属于_____晶体,它溶于蒸馏水的电离方程式为______________________,它与足量氧气反应生成硫酸氢钙的化学方程式是_________________。用单线桥表示出反应物中电子转移的数目和方向:____________________。
③回收的CO2与酚羟基的钠盐在一定条件下反应,生成有机物M,其化学式为C7H5O3Na,M经过稀硫酸酸化后得到一种药物中间体N,N的结构简式为:

M的结构简式为________________除苯基外,药物中间体N所含的官能团还有______________(填写“中文名称”)N在一定条件下可以经过自身缩聚形成一种高分子化合物,试写出形成高分子的化学反应:__________________。分子中无 -O-O- ,醛基与苯环直接相连的N的同分异构体共有_______种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝酸越稀还原产物中氮元素的化合价越低。某同学取铁铝合金与足量很稀的硝酸充分反应没有气体放出。在反应后的溶液中逐渐加入4mol·L-1NaOH溶液,所加NaOH溶液的体积与产生的沉淀的物质的量的关系如图所示(不考虑沉淀的微量溶解)。下列说法不正确的是
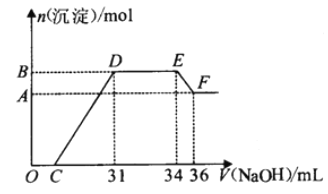
A. D点溶液中存在:c(NH4+)+c(Na+)+c(H+)=c(OH-)+c(NO3-)
B. EF段发生反应的离子方程式为:Al(OH)3+OH-=AlO2-+2H2O
C. D点溶液中n(NH4+)=0.012mol
D. 由水电离产生的c(H+):O点>F点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图将锌片和铜片用导线连接后放入稀硫酸溶液中,发生原电池反应,下列叙述错误的是

A.溶液的pH增大 B.溶液中的Zn2+浓度增大
C.溶液中的SO42-浓度增大 D.溶液的密度增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于钠元素的单质及其化合物的叙述错误的是( )
A.钠是银白色金属,氧化钠是白色粉末,过氧化钠是淡黄色粉末
B.大量的钠着火时可以用沙扑灭,不能用水或泡沫灭火剂灭火
C.金属钠在空气中长期放置,最终变为碳酸钠。
D.Na2O和Na2O2都能由金属钠和氧气化合生成,Na2O和Na2O2氧的价态也相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知0.1 mol·L-1 的醋酸溶液中存在电离平衡: CH3COOH![]() CH3COO-+H+,要使溶液中 c(H+)/c(CH3COOH)值增大,可以采取的措施是( )
CH3COO-+H+,要使溶液中 c(H+)/c(CH3COOH)值增大,可以采取的措施是( )
A.加少量烧碱溶液 B.降低温度 C.加少量冰醋酸 D.加水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com