
在下列物质的转化关系中,A是一种固体单质,且常作半导体材料,E是一种白色沉淀,F是最轻的气体单质。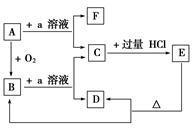
据此填写:(1)B的化学式是 ,目前在现代通讯方面B已被用作 的主要原料。
(2)B和a溶液反应的离子方程式是 。
(3)A和a溶液反应的离子方程式是 。
(4)C和过量盐酸反应的离子方程式是 。
科目:高中化学 来源: 题型:填空题
(10分)A~H等8种物质存在如下转化关系(反应条件、部分产物未标出)。已知A是正盐,B是能使品红溶液褪色的气体,G是红棕色气体。按要求回答问题: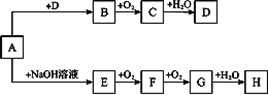
(1)写出下列物质的化学式:A ,B 。
(2)写出下列反应的化学方程式:E→F ;
写出下列反应的离子方程式:A→E ;
H的浓溶液与木炭反应的化学方程式: 。
(3)检验某溶液中是否含D中阴离子的方法是 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
硅是重要的半导体材料,构成了现代电子工业的基础。回答下列问题:
(1)基态Si原子中,电子占据的最高能层符号 ,该能层具有的原子轨道数为 、电子数为 。
(2)硅主要以硅酸盐、 等化合物的形式存在于地壳中。
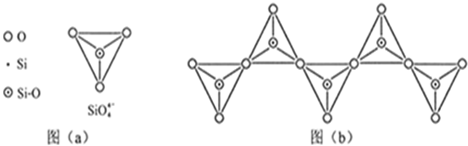
(3)单质硅存在与金刚石结构类似的晶体,其中原子与原子之间以 相结合,其晶胞中共有8个原子,其中在面心位置贡献 个原子。
(4)单质硅可通过甲硅烷(SiH4)分解反应来制备。工业上采用Mg2Si和NH4CI在液氨介质中反应制得SiH4,该反应的化学方程式为 。
(5)碳和硅的有关化学键键能如下所示,简要分析和解释下列有关事实:
| 化学键 | C-C | C-H | C-O | Si-Si | Si-H | Si-O |
| 键能(KJ/mol) | 356 | 413 | 336 | 226 | 318 | 452 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(1)瑞典化学家舍勒将软锰矿(主要成分MnO2)与浓盐酸混合加热,在世界上首先制得了氯气,写出该反应的离子方程式 ;
(2)洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。 漂白粉是常用的消毒剂。工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为 ;
(3)在下图的四条直线分别表示钠、铜、铝、铁与足量Cl2反应时,消耗金属的质量(纵轴)与反应掉的氯气质量(横轴)的关系,其中代表铁与Cl2反应的直线是 ,如果横轴表示消耗掉的硫的质量,则b表示的是四种金属中的 。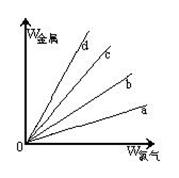
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某学校化学学习小组为探究二氧化氮的性质,按下图所示装置进行实验。
请回答下列问题:
(1)装置甲中盛放浓硝酸的仪器A的名称是 ,该装置中发生反应的化学方程式为 。
(2)实验过程中,装置乙、丙中出现的现象分别是 ;装置丙中的试管内发生反应的离子方程式为 。
(3)为了探究NO的还原性,可以在装置丁的导气管C中通入一种气体,通入的这种气体的名称是 。
(4)取下装置丙中的试管D,在其中滴加FeSO4溶液,溶液变为 色,为了证明铁元素在该反应中的产物,可以再在溶液中滴加KSCN溶液,溶液变为 色。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
金刚石、SiC具有优良的耐磨、耐腐蚀特性,应用广泛。
(1)碳与短周期元素Q的单质化合仅能生成两种常见气态化合物,其中一种化合物R为非极性分子。碳元素在周期表中的位置是____________,Q是____________,R的电子式为________。
(2)一定条件下,Na还原CCl4可制备金刚石。反应结束冷却至室温后,回收其中的CCl4的实验操作名称为________,除去粗产品中少量钠的试剂为________。
(3)碳还原SiO2制SiC,其粗产品中杂质为Si和SiO2。现将20.0 g SiC粗产品加入到过量的NaOH溶液中充分反应,收集到0.1 mol氢气,过滤得SiC固体11.4 g,滤液稀释到1 L。生成氢气的离子方程式为__________________________________,硅酸盐的物质的量浓度为_________。
(4)下列叙述正确的有________(填序号)。
①Na还原CCl4的反应、Cl2与H2O的反应均是置换反应
②水晶、干冰熔化时克服粒子间作用力的类型相同
③Na2SiO3溶液与SO3的反应可用于推断Si与S的非金属性强弱
④钠、锂分别在空气中燃烧,生成的氧化物中阴阳离子数目比均为1:2
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
下表是实验室制备气体的有关内容:
| 编号 | 实验内容 | 实验原理 | 气体发生装置 |
| ① | 制氧气 | H2O2―→O2 | |
| ② | 制氨气 | NH4Cl―→NH3 | |
| ③ | 是氯气 | HCl―→Cl2 | |


查看答案和解析>>
科目:高中化学 来源: 题型:填空题
材料是人类生存和社会发展的物质基础,不同的材料功能各不相同。以下都是有关材料的内容,试根据所给内容回答问题。
(1)氢能是未来能源最佳选择之一,氢能的利用涉及氢的储存、输运和使用。贮氢合金是解决氢的储存等问题的重要材料。贮氢合金中最具代表的是镧镍合金(LaNi5),已知LaNi5(s)+3H2(g)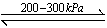 LaNi5H6(s)ΔH=-31.77 kJ·mol-1。
LaNi5H6(s)ΔH=-31.77 kJ·mol-1。
镧镍合金的熔点比镧、镍的熔点________(填“高”“低”或“介于两者之间”),根据反应原理,形成LaNi5H6的化学反应条件是________。最近有人提出可以研制出一种性能优越的催化剂,可以大大提高贮氢合金的贮氢能力,你认为该讲法可信吗?________(填“可信”或“不可信”),其理由是___________________________________________________。
(2)无机非金属材料是日常生活中不可缺少的物质,它往往具有高强度、耐高温、耐腐蚀的特点。Si3N4就是一种重要的精细陶瓷,合成氮化硅的方法之一为:
3SiO2+6C+2N2 Si3N4+6CO。Si3N4属于________晶体,在上述反应中氧化剂为________。
Si3N4+6CO。Si3N4属于________晶体,在上述反应中氧化剂为________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
氯气是重要的化工原料。
(1)氯气溶于水得到氯水,氯水中存在下列反应:Cl2+H2O??H++Cl-+HClO,其平衡常数表达式为K=________。
(2)工业上常用熟石灰和氯气反应制取漂白粉,反应的化学方程式是____________________________。流程如下图所示,其主要设备是氯化塔,塔从上到下分四层。将含有3%~6%水分的熟石灰从塔顶喷洒而入,氯气从塔的最底层通入,这样加料的目的是__________________________。处理从氯化塔中逸出气体的方法是________。
(3)某科研小组在实验室用较浓的KOH溶液直接吸收氯气,研究发现反应进行一段时间后开始出现KClO3并逐渐增多,产生KClO3的离子方程式是____________________________________,其原因可能是__________________,由此可知(2)中氯化塔设计为四层是为了减少生产中类似副反应的发生。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com