
 ��ij���↑�ɵ�ʯ��������һ��̼�⻯����--����飬���ķ�������ṹ��ͼ��ʾ��
��ij���↑�ɵ�ʯ��������һ��̼�⻯����--����飬���ķ�������ṹ��ͼ��ʾ��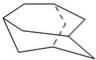
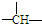 ���ṹ��
���ṹ��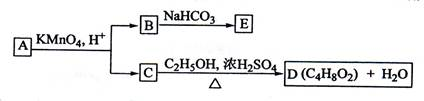
���� ��1���ɽṹ��֪����4��CH��6��CH2���Դ˷�������ʽ���ɽṹ��֪����4����Ԫ����4��C�����������ã����Ժ�4��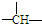 ��6��CH2����2��λ�õ�H���ݴ˴��⣻
��6��CH2����2��λ�õ�H���ݴ˴��⣻
��2��A��ʯ�͵ķ���Ϊ�����仯��
B�����������л������ᣬ�ɼӱ���Na2CO3��Һ�������������ڱ���Na2CO3��Һ��������̼���Ʒ�Ӧ������ˮ��Ȼ���Һ��ȥ��
C����ȥ�������л��е�����NaCl������AgNO3��Һ����ˣ���Һ�л������������ʣ�
D��̼̼˫����ʹ����KMnO4��Һ��ɫ��
��3��̼����Ԫ�ص�����������Ϊ0.814������Ϊ��Ԫ�أ���������������Ϊ0.186���ٶ�A����Է�������Ϊ90����N��O��=$\frac{90��0.186}{16}$=1.0463����������ԭ�Ӹ���Ϊ1����A����Է�������Ϊ��$\frac{16}{0.186}$=86�������෨��$\frac{86-16}{12}$=5��10������A�÷���ʽΪC5H10O�����C+C2H5OH$��_{��}^{Ũ����}$C4H8O2+H2O��֪��CΪCH3COOH��DΪCH3COOC2H5������B��NaHCO3��Һ��ȫ��Ӧ�������ʵ���֮��Ϊ1��2������B�к���2��-COOH��B�к���3��Cԭ�ӣ�����֪B�к���2��-COOH����B�л�����һ��CH2������B�Ľṹ��ʽΪHOOCCH2COOH���л���EΪNaOOCCH2COONa��A��������������÷ų�������˵��A�к��еĹ�����Ϊ-OH����ʹ������Ȼ�̼��Һ��ɫ��˵��A�к���C=C����AΪֱ������������Ŀ��Ϣ��B��C�ṹ���ɵ�A�Ľṹ��ʽΪ��HOCH2CH2CH=CHCH3���ݴ˽��
��4��A�ķ���ʽΪC4H6O5���л��� A��NaOH��Һ��Ӧ���������κ���ʽ�����ֲ��˵�����л�������к��������Ȼ������л����������ᷴӦ��������ζ����������˵�����д��ǻ����Ȼ��ʹ��ǻ�����������Ʒ�Ӧ�������������� 1mol���л��������������Ʒ�Ӧ����1.5molH2��˵������һ�����ǻ����û�������һ���¶��µ���ˮ������ǻ�״������ɺ���ˮ�����ӳɷ�Ӧ��˵���������ǻ���λ̼������ԭ�ӣ���A�Ľṹ��ʽΪHOOCCH��OH��CH2COOH���ݴ˽��
��� �⣺��1�����ɽṹ��֪����4��CH��6��CH2�������ʽΪC10H16���ʴ�Ϊ��C10H16��
���ɽṹ��֪����4����Ԫ����4��C�����������ã����Ժ�4��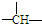 ���ʴ�Ϊ��4��
���ʴ�Ϊ��4��
���ɽṹ��֪�������к�2��λ�õ�H����һ�ȴ�����2�֣��ʴ�Ϊ��2��
��2��A��ʯ�͵ķ���Ϊ�����仯����A����
B�����������л������ᣬ�ɼӱ���Na2CO3��Һ�������������ڱ���Na2CO3��Һ��������̼���Ʒ�Ӧ������ˮ��Ȼ���Һ��ȥ����B��ȷ��
C����ȥ�������л��е�����NaCl������AgNO3��Һ����ˣ���Һ�л������������ʣ���C����
D��̼̼˫����ʹ����KMnO4��Һ��ɫ��������KMnO4��Һû����ɫ����˵������̼̼˫������D��ȷ��
��ѡBD��
��3��̼����Ԫ�ص�����������Ϊ0.814������Ϊ��Ԫ�أ���������������Ϊ0.186���ٶ�A����Է�������Ϊ90����N��O��=$\frac{90��0.186}{16}$=1.0463����������ԭ�Ӹ���Ϊ1����A����Է�������Ϊ��$\frac{16}{0.186}$=86�������෨��$\frac{86-16}{12}$=5��10������A�ķ���ʽΪC5H10O�����C+C2H5OH$��_{��}^{Ũ����}$C4H8O2+H2O��֪��CΪCH3COOH��DΪCH3COOC2H5������B��NaHCO3��Һ��ȫ��Ӧ�������ʵ���֮��Ϊ1��2������B�к���2��-COOH��B�к���3��Cԭ�ӣ�����֪B�к���2��-COOH����B�л�����һ��CH2������B�Ľṹ��ʽΪHOOCCH2COOH���л���EΪNaOOCCH2COONa��A��������������÷ų�������˵��A�к��еĹ�����Ϊ-OH����ʹ������Ȼ�̼��Һ��ɫ��˵��A�к���C=C����AΪֱ������������Ŀ��Ϣ��B��C�ṹ���ɵ�A�Ľṹ��ʽΪ��HOCH2CH2CH=CHCH3��
��������ķ�����֪��A�ķ���ʽΪC5H10O���ʴ�Ϊ��C5H10O��
��B�Ľṹ��ʽΪHOOCCH2COOH��B��������C2H5OH��Ӧ�Ļ�ѧ����ʽΪ��HOOCCH2COOH+2C2H5OH$��_{��}^{Ũ����}$C2H5OOCCH2COOC2H5+2H2O��
�ʴ�Ϊ��HOOCCH2COOH+2C2H5OH$��_{��}^{Ũ����}$C2H5OOCCH2COOC2H5+2H2O��
��������ķ�����֪��A�Ľṹ��ʽΪ��HOCH2CH2CH=CHCH3��
�ʴ�Ϊ��HOCH2CH2CH=CHCH3��
��A�ķ���ʽΪC4H6O5���л��� A��NaOH��Һ��Ӧ���������κ���ʽ�����ֲ��˵�����л�������к��������Ȼ������л����������ᷴӦ��������ζ����������˵�����д��ǻ����Ȼ��ʹ��ǻ�����������Ʒ�Ӧ�������������� 1mol���л��������������Ʒ�Ӧ����1.5molH2��˵������һ�����ǻ����û�������һ���¶��µ���ˮ������ǻ�״������ɺ���ˮ�����ӳɷ�Ӧ��˵���������ǻ���λ̼������ԭ�ӣ���A�Ľṹ��ʽΪHOOCCH��OH��CH2COOH������û��̼̼˫�����������Ȼ����϶����ǻ���û��-COOR�����ţ���ѡBC��
���� ���⿼���л�����ƶϣ��ؼ��Ǽ���ȷ��A�ķ���ʽ���ٽ����Ŀ��Ϣ����Ӧ���������ʵķ���ʽ�����ƶϣ����ؿ���ѧ�����������������Ѷ��еȣ�


 ��ѧ�̸̳����¿α�ϵ�д�
��ѧ�̸̳����¿α�ϵ�д� Сѧ��ʱ��ѵϵ�д�
Сѧ��ʱ��ѵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ͨ��һ������SO2 | B�� | ������ϵ�ݻ� | ||
| C�� | ������ȥ����SO3 | D�� | ������ϵ�¶� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ʪ��pH��ֽ��ϡ����Һ��pH���ⶨֵƫС | |
| B�� | ������ƿ������Һ������ʱ���ӿ̶��ߣ�������ҺŨ��ƫС | |
| C�� | �ñ�Һ�ζ�����Һ���ζ�ǰ�ζ����������ݣ��յ����ʱ�����ݣ��������ƫС | |
| D�� | �к��Ȳⶨʵ���У�������������У������¶�ֵƫС |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

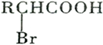
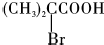 ��
�� ���÷�Ӧ����Ϊȡ����Ӧ��
���÷�Ӧ����Ϊȡ����Ӧ��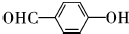 ��
��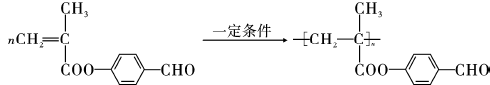 ��
��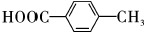 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| n/mol t/min | NO | N2 | CO2 |
| 0 | 2.00 | 0 | 0 |
| 10 | 1.16 | 0.42 | 0.42 |
| 20 | 0.80 | 0.60 | 0.60 |
| 30 | 0.80 | 0.60 | 0.60 |
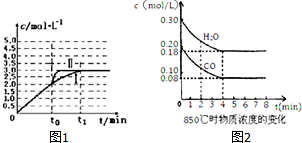
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | A��ת���ʱ�С | B�� | ƽ�����淴Ӧ�����ƶ� | ||
| C�� | D������������ | D�� | a+b��c+d |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �״���һ�ֺܺõ�ȼ�ϣ���ҵ����CH4��H2O��g��Ϊԭ�ϣ�ͨ����ӦI��II���Ʊ��״�����ش��������⣺
�״���һ�ֺܺõ�ȼ�ϣ���ҵ����CH4��H2O��g��Ϊԭ�ϣ�ͨ����ӦI��II���Ʊ��״�����ش��������⣺| ʵ���� | T���棩 | n��CO��/n��H2�� | p��MPa�� |
| l | 150 | 1/3 | 0.1 |
| 2 | n | 1/3 | 5 |
| 3 | 350 | m | 5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �μӼ����Լ��Ժ�ɫ����Һ�У�Na +��Fe2+��Cl-��NO3- | |
| B�� | ��ˮ�����c��H+��=1.0��10-13mol•L-1����Һ�У�K +��Na +��AlO2-��CO3 2- | |
| C�� | �����£�pH=7 ��Һ�У�NH4+��Al3+��NO3-��CO32- | |
| D�� | KW/c��H+��=0.1 mol•L-1����Һ��Na+��K+��SiO32-��NO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com