
 甲醇是一种很好的燃料,工业上用CH4和H2O(g)为原料,通过反应I和II来制备甲醇.请回答下列问题:
甲醇是一种很好的燃料,工业上用CH4和H2O(g)为原料,通过反应I和II来制备甲醇.请回答下列问题:| 实验编号 | T(℃) | n(CO)/n(H2) | p(MPa) |
| l | 150 | 1/3 | 0.1 |
| 2 | n | 1/3 | 5 |
| 3 | 350 | m | 5 |
分析 (1)①根据图知道平衡时甲烷的转化率,求出△c(CH4),根据v=$\frac{△C}{△t}$计算v(CH4),利用速率之比等于化学计量数之比计算v(H2).
②根据定一议二原则,定温度同,再比较压强,即作垂直x轴的辅助线,比较平衡时甲烷的转化率,由此判断;
平衡常数k=$\frac{c(CO)×C{\;}^{3}(H{\;}_{2})}{C(CH{\;}_{4})×C(H{\;}_{2}O)}$,计算出平衡时,各组分的浓度,代入平衡常数计算.
③由图可知,温度越高甲烷的转化率越大,即升高温度平衡向正反应方向移.
(2)①容器容积不变,增加甲醇产率,平衡向正反应移动,根据外界条件对平衡的影响分析.
②a.采取控制变量法,探究合成甲醇的温度和压强的适宜条件,据此判断a、b的值.
b.根据定一议二原则,定温度同,再比较压强,即作垂直x轴的辅助线,比较平衡时CO的转化率,由此判断.
解答 解:(1)①由图知道平衡时甲烷的转化率为0.5,所以△c(CH4)=$\frac{1.0mol×0.5}{100L}$=0.005mol/L,
所以v(CH4)=$\frac{0.005mol/L}{5min}$=0.001mol/(L•min),速率之比等于化学计量数之比,所以v(H2)=3v(CH4)=3×0.001mol/(L•min)=0.003mol/(L•min).
故答案为:0.003mol/(L•min);
②温度相同时,作垂直x轴的辅助线,发现压强为P1的CH4的转化率高,反应为前后体积增大的反应,压强增大平衡向体积减小的方向移动,即向逆反应移动,CH4的转化率降低,所以P1<P2.
CH4(g)+H2O(g) CO(g)+3H2(g),
CO(g)+3H2(g),
开始(mol):1.0 2.0 0 0
变化(mol):1.0×0.5 0.5 0.5 1.5
平衡(mol):0.5 1.5 0.5 1.5
所以平衡常数k=$\frac{c(CO)×C{\;}^{3}(H{\;}_{2})}{C(CH{\;}_{4})×C(H{\;}_{2}O)}$=$\frac{\frac{0.5mol}{100L}×({\frac{1.5mol}{100L})}^{3}}{\frac{0.5mol}{100L}×\frac{1.5mol}{100L}}$=2.25×10-4,
故答案为:<;2.25×10-4;
③由图可知,温度越高甲烷的转化率越大,即升高温度平衡向正反应方向移,温度升高平衡向吸热方向移动,所以正反应为吸热反应,即△H>0,
故答案为:>;
(2)①A、该反应为放热反应,升高温度,平衡向吸热方向移动,即向逆反应方向移动,甲醇的产率降低,故A错误;
B、将CH3OH(g)从体系中分离,产物的浓度降低,平衡向正反应移动,甲醇的产率增加,故B错误;
C、充入He,使体系总压强增大,容器容积不变,反应混合物各组分浓度不变,平衡不移动,甲醇的产率不变,故C错误;
D、再充入1mol CO和3mol H2,可等效为压强增大,平衡向体积减小的方向移动,即向正反应方向移动,甲醇的产率增加,故D正确.
故选:BD;
②a、采取控制变量法,探究合成甲醇的温度和压强的适宜条件,所以温度、压强是变化的,$\frac{n(CO)}{n(H{\;}_{2})}$应保持不变,所以m=$\frac{1}{3}$;比较使用1、2,压强不同,所以温度应相同,故n=150.
故答案为:150;$\frac{1}{3}$;
b、温度相同时,作垂直x轴的辅助线,发现压强为Py的CO的转化率高,反应为前后体积减小的反应,压强增大平衡向体积减小的方向移动,即向正反应移动,所以Px<Py,所以压强Px=0.1MPa.
故答案为:0.1.
点评 本题考查化学反应速率、平衡常数、化学平衡计算、化学平衡的影响因素及读图能力等,综合性较大,难度中等,知识面广,应加强平时知识的积累.注意控制变量法与定一议二原则应用.


 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:选择题
| A. | ①③⑥ | B. | ②③⑥ | C. | ①④⑤ | D. | ②③④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 地沟油和矿物油都属于酯类物质 | |
| B. | 人们用明矾对水进行消毒、杀菌 | |
| C. | 反应 原子利用率最高 原子利用率最高 | |
| D. | 甲烷、苯和油脂均不能使酸性KMnO4溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .某油田开采的石油中溶有一种碳氢化合物--金刚烷,它的分子立体结构如图所示:
.某油田开采的石油中溶有一种碳氢化合物--金刚烷,它的分子立体结构如图所示: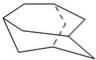
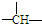 ”结构.
”结构.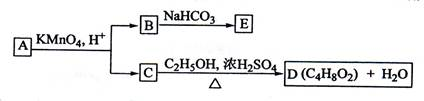
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18gH2O中含有的质子数为10NA | |
| B. | 常温常压下,22.4L氯气与足量镁粉充分反应,转移的电子数为2NA | |
| C. | 46g NO2和N2O4混合气体中含有原子总数为3NA | |
| D. | 1molNa与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀释浓硫酸时,应将蒸馏水沿玻璃棒缓慢注入浓硫酸中 | |
| B. | 过滤操作时,为了加快过滤速率,可用玻璃棒不断搅拌过滤器中液体 | |
| C. | 分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 将固体加入容量瓶中溶解并稀释至刻度,配制成一定物质的量浓度的溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com