
【题目】某模拟“人工树叶”电化学实验装置如下图所示,该装置能将H2O和CO2转化为O2和燃料(C3H8O),下列说法正确的是( ) 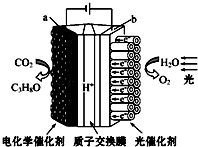
A.该装置将化学能转化为光能和电能
B.a电极的反应为:3CO2+18H+﹣18e﹣═C3H8O+5H2O
C.每生成1 mol O2 , 有44 g CO2被还原
D.该装置工作时H+从b极区向a极区迁移
【答案】D
【解析】解:A、该装置是电解池装置,是将电能转化为化学能,所以该装置将光能和电能转化为化学能,故A错误;B、a与电源负极相连,所以a是阴极,发生还原反应,电极反应式为:3CO2+18H++18e﹣=C3H8O+5H2O,故B错误;
C、电池总的方程式为:6CO2+8H2O ![]() 2C3H8O+9O2 , 即生成9mol的氧气,阴极有6mol的二氧化碳被还原,也就是1mol的氧气,阴极有
2C3H8O+9O2 , 即生成9mol的氧气,阴极有6mol的二氧化碳被还原,也就是1mol的氧气,阴极有 ![]() mol的二氧化碳被还原,所以被还原的二氧化碳为29.3g,故C错误;
mol的二氧化碳被还原,所以被还原的二氧化碳为29.3g,故C错误;
D、a与电源负极相连,所以a是阴极,而电解池中氢离子向阴极移动,所以H+从阳极b极区向阴极a极区迁移,故D正确;
故选D.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列关于氮气的说法中,错误的是( )
A.通常情况下,氮气性质比较稳定
B.氮气可经一步反应转化成二氧化氮
C.通常情况下,氮气在水中的溶解度很小
D.跟氢气在一定条件下发生反应时,氮气是氧化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组研究铝土矿中Al2O3的含量。已知铝土矿的主要成分是Al2O3,杂质是Fe2O3、SiO2等。从铝土矿中提取Al2O3的过程如下:
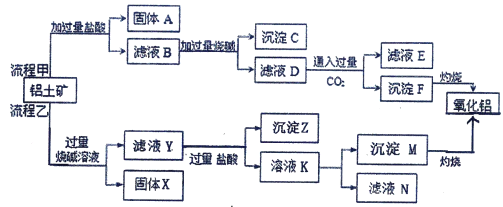
(1)流程甲中加入盐酸后生成Fe3+的离子方程式为________________;固体A是___________(填化学式),写出沉淀F转化为氧化铝的化学方程式是___________________________。
(2)流程乙中,向铝土矿中加入过量烧碱溶液后,发生反应的离子方程式是__________;固体X的主要用途有(写出1条即可) _____。沉淀Z为_______(填化学式)。由溶液K生成沉淀M的离子方程式是_________________________。
(3)流程乙中,将实验过程中所得固体精确称量,课外小组发现所得氢氧化铝固体的质量与原铝土矿质量相等,则该铝土矿中Al2O3的质量分数是________(保留一位小数)
(4)工业上制取AlCl3用Al2O3与C、Cl2在高温条件下反应,每消耗0.5mol碳单质,转移1mol电子,反应的化学方程式是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A. 硫酸氢钠溶液与小苏打溶液的反应:H+ + HCO3- = CO2↑ + H2O
B. 用苛性钠溶液吸收过量SO2:SO2 +2OH-= SO32- + H2O
C. 二氧化锰和浓盐酸反应:MnO2+4HCl![]() Mn2++2Cl2↑+2H2O
Mn2++2Cl2↑+2H2O
D. 工业上氯气和石灰乳反应制漂白粉:Cl2 + 2OH-= ClO-+ Cl- + H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化合物能用相应元素的单质直接化合生成的是
①CuS ②FeS ③Al2S3 ④Fe2S3 ⑤Cu2S ⑥FeCl2 ⑦H2S ⑧FeCl3
A. ②③⑤⑦⑧ B. ①④⑥⑦ C. ①②③⑦⑧ D. ②③⑤⑥⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A,B,C,D,E五种元素,其相关信息如表:
元素 | 相关信息 |
A | A原子的1s轨道上只有1个电子 |
B | B是电负性最大的元素 |
C | C基态原子的2p轨道中有3个未成对电子 |
D | D是主族元素且与E同周期,其最外能层 |
E | E能形成红色(或砖红色)的E2O和黑色的EO两种氧化物 |
请回答下列问题:
(1)写出E元素原子基态时的电子排布式 .
(2)C元素的第一电离能比氧元素的第一电离能(填“大”或“小”).
(3)CA3分子中C原子的杂化类型是 .
(4)A、C、E三种元素可形成[E(CA3)4]2+ , 其中存在的化学键类型有(填序号);
①配位键 ②金属键 ③极性共价键 ④非极性共价键 ⑤离子键 ⑥氢键
若[E(CA3)4]2+具有对称的空间构型,且当[E(CA3)4]2+中的两个CA3被两个Cl﹣取代时,能得到两种不同结构的产物,则[E(CA3)4]2+的空间构型为(填序号).
a.平面正方形 b.正四面体 c.三角锥形 d.V形
(5)B与D可形成离子化合物,其晶胞结构如图所示.其中D离子的配位数为 , 若该晶体的密度为a gcm﹣3 , 则该晶胞的体积是cm3(写出表达式即可). 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的Mg和Al的混合物投入200 ml稀盐酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示。则下列说法不正确的是( )
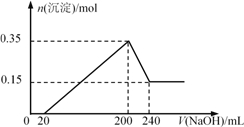
A. Mg和Al的总质量为9g
B. 盐酸的物质的量浓度为5 mol/L
C. NaOH溶液的物质的量浓度为5 mol/L
D. 生成的H2在标准状况下的体积为11.2 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、Q、R是五种短周期元素,原子序数依次增大,部分元素在周期表中的位置关系如右图所示.其中X是周期表中原子半径最小的元素,Q与X同主族;Z的最外层电子数是次外层的3倍.
Y | Z | ||
R |
请回答下列问题:
(1)写出Y元素的名称:________,Q的原子结构示意图________;R在周期表中的位置为________.
(2)Q2Z电子式为:________,Q2Z2含的化学键类型为:________.
(3)R、Z分别形成简单离子的半径大小:________________(离子符号表示)
(4)Y的氢化物与其最高价氧化物对应的水化物反应的化学方程式为:__________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤炭可以转化为清洁能源和化工原料。
⑴用煤可以制得水煤气,其化学反应方程式为________________________________。
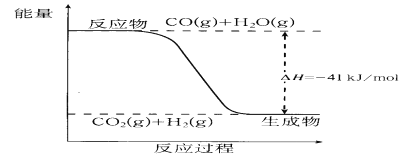
⑵已知一氧化碳与水蒸气反应过程的能量变化如图所示。则此反应为_________(填“放热”或“吸热”)反应,反应的热化学方程式为___________________________________。
⑶已知1mol C完全转化为水煤气时吸收热量131.5kJ,则1mol C与CO2反应生成CO吸收热量______kJ。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com