
【题目】X、Y、Z、Q、R是五种短周期元素,原子序数依次增大,部分元素在周期表中的位置关系如右图所示.其中X是周期表中原子半径最小的元素,Q与X同主族;Z的最外层电子数是次外层的3倍.
Y | Z | ||
R |
请回答下列问题:
(1)写出Y元素的名称:________,Q的原子结构示意图________;R在周期表中的位置为________.
(2)Q2Z电子式为:________,Q2Z2含的化学键类型为:________.
(3)R、Z分别形成简单离子的半径大小:________________(离子符号表示)
(4)Y的氢化物与其最高价氧化物对应的水化物反应的化学方程式为:__________________________.
【答案】 氮 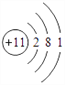 第三周期ⅢA族
第三周期ⅢA族 ![]() 离子键、共价键 Al3+<O2﹣ NH3+HNO3═NH4NO3
离子键、共价键 Al3+<O2﹣ NH3+HNO3═NH4NO3
【解析】X是周期表中原子半径最小的元素,则X为H元素,Z的最外层电子数是次外层的3倍,则Z为O元素,所以Y为N元素,故R为Al元素,Q与X同主族, Q的原子序数小于Al的原子序数大于O的原子序数,所以Q为Na。
(1)根据上面分析知Y的名称为:氮;Na的原子结构示意图为: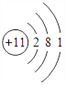 ;Al在周期表中的位置为:第三周期ⅢA族。
;Al在周期表中的位置为:第三周期ⅢA族。
(2)Na2O的电子式为:![]() ;Na2O2为离子化合物,阳离子为Na+,阴离子为O22-,故含有的化学键为离子键和共价键。
;Na2O2为离子化合物,阳离子为Na+,阴离子为O22-,故含有的化学键为离子键和共价键。
(3)Al3+、O2-的电子层结构相同,根据“序大径小”的规律可知离子半径大小关系为:Al3+<O2﹣。
(4)N的氢化物为NH3,N的最高价氧化物的水合物为HNO3,两者反应的化学方程式为:NH3+HNO3═NH4NO3。


科目:高中化学 来源: 题型:
【题目】电解Na2PbCl4溶液,生成Pb,装置如下图,下列说法不正确的是
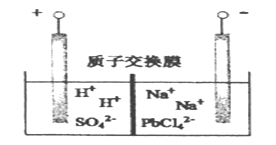
A. 阴极的电极反应式为 PbCl42- +2e- =Pb + 4Cl-
B. 电解一段时间后,Na2PbCl4浓度极大下降,可加入PbO恢复其浓度
C. 电解过程中阳极溶液的pH减小,阴极的pH保持不变
D. 电路中通过0.2mol,则阴极的质量增加20.7g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某模拟“人工树叶”电化学实验装置如下图所示,该装置能将H2O和CO2转化为O2和燃料(C3H8O),下列说法正确的是( ) 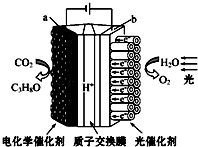
A.该装置将化学能转化为光能和电能
B.a电极的反应为:3CO2+18H+﹣18e﹣═C3H8O+5H2O
C.每生成1 mol O2 , 有44 g CO2被还原
D.该装置工作时H+从b极区向a极区迁移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】还原铁粉是化工生产及实验室中常用的还原剂。工业上以绿矾为原料制备还原铁粉的工艺如下:
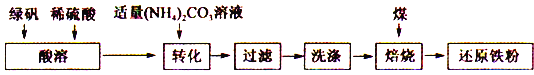
回答下列问题:
(1)酸溶过程中硫酸的作用是________________________ 。
(2)转化的目的是制得FeCO3,加液时应将(NH4)2CO3溶液加入到FeSO4中,原因是_____________。
(3)转化过程中温度不超过35℃,原因是___________________________ 。
(4)生成的FeCO3沉淀需充分洗涤,检验洗涤是否完全的方法是___________________ 。
(5)将FeCO3浊液暴露在空气中,固体表面变为红褐色,同时释放出CO2,写出该反应的化学方程式:________________________ 。
(6)在焙烧过程中需加入CaCO3进行脱硫处理。下图为加CaCO3和不加CaCO3对还原铁粉产率的影响,据图分析CaCO3的另一作用为________________________ 。
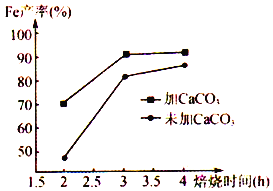
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用二氧化氯(ClO2)可制备用途广泛的亚氯酸钠(NaClO2),实验室可用下列装置(略去部分夹持仪器)制备少量的亚氯酸钠。
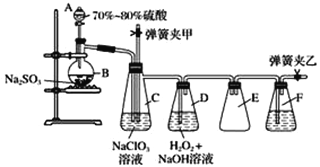
装置C中发生反应:2NaClO3+SO2===2ClO2+Na2SO4(Ⅰ)
装置D中发生反应:2ClO2+H2O2+2NaOH===2NaClO2+2H2O+O2(Ⅱ)
(1)仪器组装完毕,关闭两个弹簧夹,打开A中活塞,向A中注入水可检验装置气密性,装置气密性良好的现象是________________________。实验开始时,打开A的活塞,两个弹簧夹的开关操作是__________________。
(2)装置B中进行的是用硫酸与亚硫酸钠制备二氧化硫的反应,该处使用的是70%~80%的硫酸,而不是98%的浓硫酸或极稀的硫酸,原因是___________________________________。
(3)装置C的作用是________________,装置E的作用是________________。
(4)在碱性溶液中NaClO2比较稳定,所以装置D中应维持NaOH稍过量,判断NaOH是否过量所需要的试剂是________。
a.稀盐酸 b.品红溶液 c.石蕊溶液 d.酚酞溶液
(5)一次实验制备中,通过检验发现制备的NaClO2中含有NaOH、Na2SO3,出现这些杂质的可能原因是__________________。检验产物中含有Na2SO3杂质的实验操作和现象是______________________。 (供选择的试剂有:Ba(OH)2溶液、H2O2溶液、AgNO3溶液、品红溶液、H2SO4溶液)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“空气中氧气体积分数的测定”有多种方法,请按要求回答下列问题:在燃烧匙内盛过量红磷,红磷必须过量的原因是______,点燃红磷后立即插入集气瓶内,塞紧橡皮塞红磷燃烧的现象是____________,其反应的化学方程式为____________________。待红磷火焰熄灭,集气瓶冷却至室温,打开止水夹,观察到的现象是______,该实验除了得出氧气在空气中的体积分数之外,还能得出氮气具有的性质是______(任写一点);若测得空气中氧气的体积分数约为1/7,则可能的原因是______。
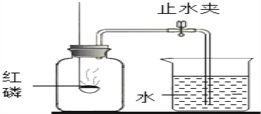
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A. 用醋酸除去水垢:CaCO3+2H+=Ca2++H2O+CO2↑
B. 用铜为电极电解饱和食盐水:2Cl-+2H2O![]() Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
C. FeBr2溶液中通入过量Cl2:2Fe2++Cl2=2Fe3++2Cl-
D. 用FeCl3溶液腐蚀印刷电路板上铜箱:2Fe3++Cu=2Fe2++Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制Cl2的反应为:MnO2+4HC1(浓) ![]() MnCl2+Cl2+2H2O,下列有关该反应的说法正确的是( )
MnCl2+Cl2+2H2O,下列有关该反应的说法正确的是( )
A.MnO2是还原剂
B.HCl被氧化
C.MnO2发生氧化反应
D.4molHCl参加反应则转移4mol电子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com