

���� ��1����Ӧ��=��Ӧ���ܼ���-�������ܼ��ܣ�
��2�������������䣬ƽ����������ݻ�ѹ����ԭ����$\frac{1}{2}$��ѹǿ���������淴Ӧ���ʶ���������Ӧ����������࣬ƽ��������Ӧ�����ƶ����������Ũ�����������¶Ȳ��䣬��ƽ�ⳣ�����䣬���ƽ�ⳣ����֪��ƽ��ʱ��Ӧ�����ֵ�Ũ�ȶ�����
��3����Ϊ���º��ݣ���Ϊ���º�ѹ���淴Ӧ���л���������ʵ�����С��ƽ��ʱ����ѹǿ��С������ƽ���Ч�ټ�ƽ�����������ѹǿ����Ӧ���ʼӿ죬��ƽ��ʱ���̣�ƽ�������ƶ���������ת�������ӣ�
��4����ƽ�����������Ҫ���ƽ��ʱ�������������������Ͷ����֮��Ӧ���ڷ�Ӧ��Ļ�ѧ������֮�ȣ�
��� �⣺��1�����1molN-H����Ҫ��������x kJ����
3��436kJ+946kJ-6��x kJ=-92��
���x=391��
�ʴ�Ϊ��391kJ��
��2��A��ƽ����������ݻ�ѹ����ԭ����$\frac{1}{2}$��ѹǿ����ƽ��������Ӧ�����ƶ����������Ũ����������ƽ�ⳣ�����䣬���ƽ�ⳣ����֪��ƽ��ʱ��Ӧ�����ֵ�Ũ�ȶ�����A����
B��ѹǿ���������淴Ӧ���ʶ���������Ӧ����������࣬��B����
C��ѹǿ����ƽ��������Ӧ�����ƶ���NH3�����ʵ������ӣ���C��ȷ��
D��ƽ�ⳣ��ֻ���¶�Ӱ�죬�¶Ȳ��䣬ƽ�ⳣ�����䣬��D����
E������ӦΪ���������С�ķ�Ӧ��ѹǿ����ƽ��������Ӧ�����ƶ�����E��ȷ��
�ʴ�Ϊ��CE��
��3����Ϊ���º��ݣ���Ϊ���º�ѹ���淴Ӧ���л���������ʵ�����С��ƽ��ʱ����ѹǿ��С������ƽ���Ч�ټ�ƽ�����������ѹǿ����Ӧ���ʼӿ죬��ƽ��ʱ���̣�ƽ�������ƶ���������ת�������ӣ�����������H2��ת������ʱ��仯��ͼ��Ϊ��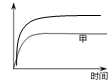 ��
��
�ʴ�Ϊ�� ��
��
��4����ƽ�����������Ҫ���ƽ��ʱ�������������������Ͷ����֮��Ӧ���ڷ�Ӧ��Ļ�ѧ������֮�ȣ�����a��b=1��3��
�ʴ�Ϊ��1��3��
���� ���⿼�黯ѧƽ�������Ӱ�����ء������뷴Ӧ�ȹ�ϵ�ȣ������ڻ�ѧƽ���ƶ����ۺϿ��飬��Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 25��ʱ����0.02 mol•L-1�İ�ˮ��a mol•L-1������������ϣ�����仯���Բ��ƣ�����Ӧ����Һ�����ԣ����ú�a�Ĵ���ʽ��ʾNH3•H2O�ĵ��볣��ΪKb=$\frac{a��1{0}^{-7}}{0.02-a}$ | |
| B�� | ��������Һ�м�ˮϡ�ͣ���Ӧ��ƽ�����淴Ӧ�����ƶ� | |
| C�� | ����������Һ�м������������ᣬ����Һ�л������ɫ���� | |
| D�� | ��֪��H+��aq��+OH-��aq���TH2O��l����H=-57.3 kJ•mol-1����1 L 0.1 mol•L-1��ˮ�����������ᷴӦ�ų�����������5.73 kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | pH=5��H2S��Һ�У�c��H+��=c��HS-��=1��10-5mol•L-1 | |
| B�� | ��0.1mol•L-1��ˮ��pHΪ11������ΪNH2•H2O?NH4++OH- | |
| C�� | 0.01mol•L-1NaHCO3��Һ�����ʵĵ��뷽��ʽΪNa++H++CO32- | |
| D�� | CH3COOH��Һ��ˮϡ�ͺ���Һ��$\frac{c��C{H}_{3}COOH��}{c��C{H}_{3}CO{O}^{-}��}$��ֵ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ļ����ڿ�����ȼ�տɿ�����ɫ���棬��Ϳ�г���ʯ��ˮ��С�ձ����ڻ����Ϸ����ձ��ڱڱ���� | |
| B�� | �������ʦ�Ƿ�ƺ�ݳ�������ͬ־����װ��K2Cr2O7�����Լ��Ĵ�������Ǽ�⣬����������ɳ�ɫ��Ϊ��ɫ��˵������ʦ�ƺ�ݳ�Ӧ�����д��� | |
| C�� | ��ѧ̽����С���ڼ���ʳ���ݼ������۲쵽�����DZ���û�в������ݣ�˵��ʳ����Ҫ�ɷ�����û������ | |
| D�� | ��Ȼ��ά��������ά���ϳ���ά�о�������ά�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ������H2O2����Ϊ��ɫ������������ܵ�����Խ��Խ��Ĺ�ע��ijʵ��С���Թ�������ֽ�Ϊ����̽��Ũ�ȡ���Һ������ԶԷ�Ӧ���ʵ�Ӱ�죮�ڳ����°����±����ʵ�飮
������H2O2����Ϊ��ɫ������������ܵ�����Խ��Խ��Ĺ�ע��ijʵ��С���Թ�������ֽ�Ϊ����̽��Ũ�ȡ���Һ������ԶԷ�Ӧ���ʵ�Ӱ�죮�ڳ����°����±����ʵ�飮| ʵ���� | ��Ӧ�� |
| a | 10mL2%H2O2��Һ�������ռ� |
| b | 10mL2%H2O2��Һ |
| c | 10mL2%H2O2��Һ���������� |
| d | 10mL5%H2O2��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C5H12����������������ͬ���칹�� | |
| B�� | ���ᡢ��������һ�������¾�����Cu��OH��2��Ӧ | |
| C�� | ����Ũ���ᡢŨ�����Ϲ�����ȡ���ᱽ�Ƿ���ȡ����Ӧ | |
| D�� | ���ۺ���ά�ؾ����ã�C6H10O5��n��ʾ��������ǻ�Ϊͬ���칹�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
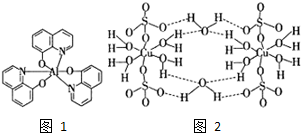 2012��10��1�����ҹ�������̭�׳�ƶ����ø�Ч�����ĵ��·����Ʒ�����·�������в���Mn2+��Cu2+����п���쵥����8һ�ǻ�������ȣ�
2012��10��1�����ҹ�������̭�׳�ƶ����ø�Ч�����ĵ��·����Ʒ�����·�������в���Mn2+��Cu2+����п���쵥����8һ�ǻ�������ȣ�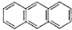 ��ƽ��ṹ�����ڷǼ��ԣ�����ԡ��Ǽ��ԡ������ӣ�
��ƽ��ṹ�����ڷǼ��ԣ�����ԡ��Ǽ��ԡ������ӣ��鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com