
向溴水中加入足量乙醛溶液,可以看到溴水褪色。据此对溴水与乙醛发生的有机反应类型进行如下探究,请你完成下列填空:
I.猜测:
(1)溴水与乙醛发生取代反应;
(2)溴水与乙醛发生加成反应;
(3)溴水与乙醛发生_______反应。
II.设计方案并论证:
为探究哪一种猜测正确,某研究性学习小组提出了如下两种实验方案:
方案l:检验褪色后溶液的酸碱性。
方案2:测定反应前用于溴水制备的Br2的物质的量和反应后Br-离子的物质的量。
(1)方案1是否可行? _______,理由是__________________________________________
(2)假设测得反应前用于溴水制备的Br2的物质的量为a mol 。
若测得反应后n(Br-) = _______mol,则说明溴水与乙醛发生加成反应;;
若测得反应后n(Br-) = _______mol,则说明溴水与乙醛发生取代反应;
若测得反应后n(Br-) = _______mol,则说明猜测(3)正确。
III.实验验证:某同学在含0.005molBr2的10mL溶液中,加入足量乙醛溶液使其褪色;再加入过量AgNO3溶液,得到淡黄色沉淀l.88 g(已知反应生成有机物与AgNO3不反应)。根据计算结果,推知溴水与乙醛反应的离子方程式为__________________________________________。
IV.拓展
请你设计对照实验,探究乙醛和乙醇的还原性强弱(填写下表)。
| 实验操作步骤 | 实验现象 | 结论 |
| | | |
I.(3)氧化(1分)
II.(1)不可行(1分) 溴水与乙醛发生取代反应和乙醛被溴水氧化都有HBr生成,溶液均呈酸性(2分)
(2)0 (1分) a (1分) 2a(1分)
III.CH3CHO+Br2+H2O=CH3COOH+2H++2Br-(2分)
IV.实验操作步骤 实验现象 结论 在两支洁净的试管中分别加入2mL新制银氨溶液(或新制氢氧化铜),各滴入3滴(或0.5mL)乙醛和乙醇振荡,水浴加热(或加热)试管(3分) 滴入乙醛的试管中有银镜(或红色沉淀)生成,而滴入乙醇的试管中无现象(1分) 乙醛的还原性比乙醇强(1分)
解析试题分析:
I.根据溴水的性质和乙醛的结构片断去推两者可能的反应是取代、加成或氧化;
II.(1)显然是不可行的,因为无论是溴水与乙醛发生的是取代反应还氧化反应产物中都有HBr生成,溶液均会呈现出酸性;
(2)根据加成、取代、氧化反应的特点可知n(Br-)分别为0、a、2a;
III.经过计算AgBr的物质的量为0.01mol,整好是Br2的2倍,因而发生的是氧化反应。
V.设计实验探究乙醛和乙醇的还原性强弱,可以利用醛基的强还原性可以和银氨溶液或新制Cu(OH)2悬浊液的反应来进行验证。
考点:本题以探究实验为基础,考查了溴水和乙醛反应的实质、探究实验的基本方法、有机反应的特点以及化学实验的基础知识。


 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案科目:高中化学 来源: 题型:实验题
为测定某铝镁合金中镁的质量分数,某小组计划将铝镁合金与足量稀硫酸溶液反应,测定生成气体的体积。填写下列空白。
(1)同学们选用甲装置进行实验:实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻打开其活塞,一会儿后稀硫酸就不能顺利滴入锥形瓶。请你帮助分析原因是________________。
(2)同学们经讨论认为甲装置有两个方面会引起较大误差,分别是__________和__________。
(3)于是他们设计了实验装置乙。乙中导管a的作用是__________。若实验前后滴定管中液面读数分别为V1 mL、V2 mL。则产生氢气的体积为______mL。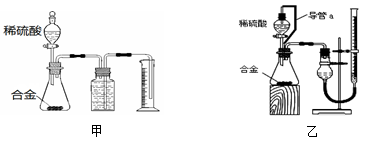
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
铁是人体不可缺少的微量元素,摄入含铁的化合物可补充铁。“速力菲”是市场上一种常见的补铁药品,下表是说明书的部分内容。
[规格]每片含琥珀酸亚铁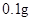 [适应症]用于缺铁性贫血症,预防及治疗用。 [用量用法]成人预防量 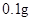 /日,成人治疗量 /日,成人治疗量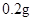 — —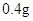 /日。 /日。小儿用量预防量 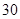 — —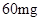 /日,治疗量 /日,治疗量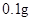 — — /日 /日[贮藏]避光、密封、在干燥处保存。 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
白云石的主要成分为CaCO3、MgCO3,还含有少量Fe、Si的化合物,实验室以白云石为原料制Mg(OH)2及CaCO3。步骤如下:
实验过程中需要的数据见下表:
| | 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Mg2+ | 9.5 | 11.0 |

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
过碳酸钠(2Na2CO3·3H2O2)是一种集洗涤、漂白、杀菌于一体的氧系漂白剂,该晶体具有Na2CO3和H2O2的双重性质。利用图-2装置制备过碳酸钠,在冷水浴中充分反应后,按图-1流程可获得过碳酸钠产品。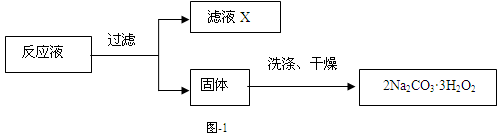
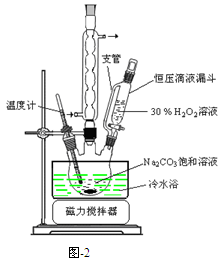
完成下列填空:
(1)恒压滴液漏斗中支管的作用是 。
(2)制备过碳酸钠的关键是 。
(3)不会使过碳酸钠失效的物质是_______(选填编号)。
a.Na2S b.CH3COOH c.NaHCO3
过碳酸钠产品中往往含有少量碳酸钠,可用重量法测定过碳酸钠的质量分数。
(4)完成实验步骤:
溶解 → 沉淀反应 → ________ → ________ → ________ → ________ 。
(5)写出沉淀反应的离子方程式________________________________________。
(6)需要直接测定的物理量有:________________________________(用字母表示并注明其含义)。产品中过碳酸钠质量分数的表达式为:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
氧化铁是重要工业颜料。工业上通常以废铁屑(杂质不与酸反应)为原料制备FeCO3,再将其煅烧制取氧化铁。工业制备FeCO3的流程如下:
回答下列问题:
(1)操作Ⅰ的名称是 。
(2)写出生成FeCO3沉淀的离子方程式 。
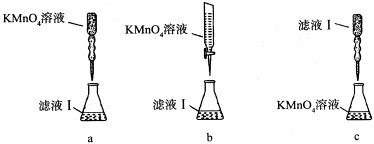
(3)有些同学认为滤液Ⅰ中铁元素含量可用KMnO4溶液来测定(5Fe2++MnO-4+8H+=5Fe3++Mn2++4H2O)。
①实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250 mL,配制时需要的玻璃仪器除玻璃棒、烧杯、胶头滴管外,还需 。
②某同学设计了下列滴定方式(夹持部分略去),最合理的是 。(填字母序号)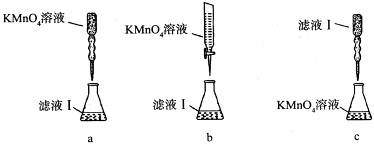
(4)该流程中用到的Na2CO3在工业生产中常含有少量NaCl。某校化学活动社团设计如图所示装置来测定Na2CO3的含量。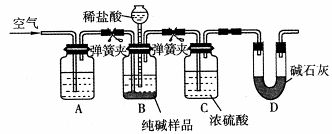
①要检验Na2CO3中杂质的存在,选用下列试剂中的 (选填序号)。
a.氢氧化钡溶液 b.稀硝酸 c.硫氰酸钾溶液 d.硝酸银溶液
②检验装置B气密性的方法是:塞紧带长颈漏斗的三孔橡胶塞,夹紧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于瓶内的水面,停止加水后静置,若 ,说明装置不漏气。
③装置A中的试剂 ,装置C的作用 。
④以上实验装置存在明显缺陷,该缺陷导致测定结果偏高,该缺陷为 。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
白菜中含有钙铁等元素,某化学小组设计如下方案测定干白菜中钙元素的质量分数。首先取10.00g干白菜叶,灼烧得白菜灰粉进行下列实验: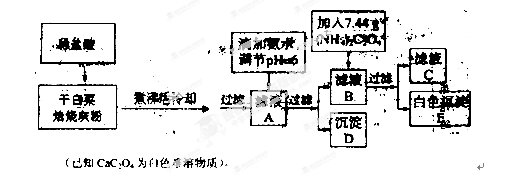
(1)实验前要先将干白菜叶样品高温灼烧成灰粉,其主要目的是使样品中的有机物完全分解,使干白菜叶中的钙、铁元素溶解完全,灼烧用到的部分仪器有
A.坩埚 B.蒸发皿 C.玻璃棒 D.泥三角
(2)写出从滤液A→沉淀D的离子反应方程式 。
(3)用KMnO4标准溶液滴定滤液C:先将滤液C稀释至500 mL,再取其中的25.00 mL溶液,用硫酸酸化后,用0.100 0 mol·L-1’的KMnO4标准溶液滴定,终点时消耗KMnO4溶液10.00mL。
发生的反应为:
①滴定的过程中,同学们发现一个现象:向C溶液中加入第一滴KMnO4溶液时,需要振摇锥形瓶较长时间才能褪色,当溶液褪色后,再滴入KMnO4溶液,则迅速褪色,直至达到终点;为了加快滴入第一滴KMnO4溶液时的褪色速度,可采取的方法是 .(选择合适的选项)
A.适当加热锥形瓶内溶液 B.在锥形瓶内加少量水
C.在锥形瓶内加适量乙醇 D.在锥形瓶内加入几滴MnSO4溶液
②判断滴定达到终点的方法是 。
(4)原干白菜叶中钙元素的质量分数为 。
(5)为保证实验精确度,沉淀D及E需要分别洗涤,并将洗涤液转移回母液中,试判断沉淀D已经洗涤干净的方法是 。如果沉淀E未洗涤,或未将洗涤液转移回母液,则测得的钙元素质量分数 (填“偏高”“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
现有三组溶液:①汽油和氯化钠溶液;②39%的乙醇溶液;③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是 ( )
| A.分液、萃取、蒸馏 | B.分液、蒸馏、萃取 |
| C.萃取、蒸馏、分液 | D.蒸馏、萃取、分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
小华家中有如下生活用品:碘酒、食盐、食醋、84消毒液(内含NaClO),小华利用上述用品不能完成的任务是
| A.检验买来的奶粉中是否加有淀粉 | B.检验自来水中是否含有Cl- |
| C.除去保温瓶中的水垢 | D.洗去白色衣服上的番茄汁 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com