
������ʵĵ���ƽ�⡢�����ˮ��ƽ�����������ܽ�ƽ������ڻ�ѧƽ�⡣
��֪H2A��ˮ�д�������ƽ�⣺H2A=H����HA����HA�� H����A2����
H����A2����
(1)������NaHA��Һ��pH________(����ţ���ͬ)��ԭ����_____________��
A������7������������ B��С��7 C������7 D����ȷ��
(2)ij�¶��£�����0.1 mol��L��1��NaHA��Һ����εμ�0.1 mol��L��1 KOH��Һ����Һ������(���Ի�Ϻ���Һ������仯)����ʱ�û����Һ�е����й�ϵһ����ȷ����________��
A��c(H��)��c(OH��)��1.0��10��14
B��c(Na��)��c(K��)��c(HA��)��2c(A2��)
C��c(Na��)>c(K��)
D��c(Na��)��c(K��)��0.05 mol��L��1
(3)��֪������H2A�ĸ���(CaA)�ı�����Һ�д�������ƽ�⣺CaA(s)??Ca2��(aq)��A2��(aq)����H>0����Ҫʹ����Һ��Ca2��Ũ�ȱ�С���ɲ�ȡ�Ĵ�ʩ��________��
A�������¶ȡ����������� B�������¶�
C������NH4Cl���� D������Na2A����
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
ij��Ԫ��(��H2A��ʾ)��ˮ�еĵ��뷽��ʽ�ǣ�H2A=H����HA����HA�� H����A2�����ش��������⣺
H����A2�����ش��������⣺
(1)NaHA��Һ________(������ԡ������Լ��ԡ����������ԡ����������ȷ����)��ԭ����______________________��
(2)ij�¶��£���0.1 mol��L��1��NaHA��Һ�е���0.1 mol��L��1 KOH��Һ�����ԣ���ʱ��Һ�����¹�ϵһ����ȷ����________(����ĸ)��
| A��c(H��)��c(OH��)��1��10��14 mol��L��1 |
| B��c(Na��)��c(K��)��c(HA��)��2c(A2��) |
| C��c(Na��)>c(K��) |
| D��c(Na��)��c(K��)��0.05 mol��L��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
25 ��ʱ,����ƽ�ⳣ��:
| ����Ļ�ѧʽ | CH3COOH | HClO | H2CO3 |
| ����ƽ�ⳣ��(25 ��) | 1.8��10-5 | 3.0�� | K1=4.3��10-7 K2=5.6��10-11 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�ⶨNaOH��Na2CO3�Ļ��Һ��NaOH�ĺ���ʱ�������ڻ��Һ�м��������BaCl2��Һ��ʹNa2CO3��ȫ���BaCO3������Ȼ������֪Ũ�ȵ�����ζ�(�÷�̪��ָʾ�������ɫpH��ΧΪ8��10)���Իش�
(1)�ζ�ʱBaCO3�ܷ��ܽ⣿________(��ܡ� ���ܡ�)��������____________________________________________________��
(2)���ü�����ָʾ��(���ɫpH��ΧΪ3.1��4.4)����ⶨ�Ľ��________(�ƫ�ߡ���ƫ�͡�����Ӱ�족)��ԭ����_________________________________________________
(3)��ͼ��3�ֶ���������һ���֣�������к͵ζ�ʱӦѡ________(�����)���ڵζ��ӽ��յ�ʱ��Ӧ������ˮ��ϴ��ƿ�ڱڣ�Ŀ����________________________________________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
ij�¶�(t ��)ʱ��ˮ�����ӻ�ΪKW��1.0��10��13mol2��L��2������¶�(����ڡ�����С�ڡ����ڡ�)________25 �棬��������_______________________________________��
�������¶���pH��11�Ŀ�������Һa L��pH��1��ϡ����b L���(���Ϻ���Һ�����С�仯���Բ���)����ͨ��������д���²�ͬ���ʱ������Һ������ȣ�
(1)�����û��ҺΪ���ԣ���a��b��________������Һ�и������ӵ�Ũ���ɴ�С����˳����___________________________________��
(2)�����û��Һ��pH��2����a��b��________������Һ�и������ӵ�Ũ���ɴ�С����˳����__________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
(1)��25 ��ʱ,��20 mL 0.1 mol��L-1 CH3COOH��Һ��20 mL 0.1 mol��L-1 HSCN��Һ�ֱ���20 mL 0.1 mol��L-1 NaHCO3��Һ���,ʵ���ò������������(V)��ʱ��(t)�ı仯��ͼ��ʾ����Ӧ��ʼ��������Һ����CO2��������ʴ������Բ����ԭ�������������������������������������� 
��Ӧ��������������Һ��,c(CH3COO-)��������c(SCN-)(�>����<����=��)��
���������¶Ȳ���,�ڴ�����Һ�м�����������,���������С������������(�����)��
| A��c(CH3COO-) | B��c(H+) | C��KW | D���������ƽ�ⳣ�� |


 )(�<����>����=��)��
)(�<����>����=��)�� �鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
������ʵ�����������õ���Ⱥ͵���ƽ�ⳣ����ʾ����1�dz����¼�������ĵ���ƽ�ⳣ��(Ka)������ĵ���ƽ�ⳣ��(Kb)����2�dz����¼�����()������ܶȻ�����(Ksp)��
��1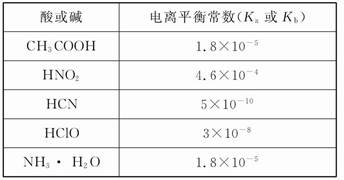
��2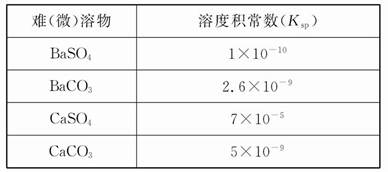
��ش��������⣺
(1)CH3COONH4��ˮ��Һ�� (ѡ����ԡ��������ԡ����ԡ�)�������� ����Һ�и�����Ũ�ȴ�С��ϵ�� ��
(2)���ʵ���֮��Ϊ1��1��NaCN��HCN�Ļ����Һ����pH>7������Һ������Ũ�ȴӴ�С������Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
ijͬѧ�ù�ҵ����ͭ�����������������ʣ��Ʊ�������CuSO4��5H2O��������������
�����ֲ����������ԣ���
I��ȡ��ҵ����ͭ���壬��ϡ�����ܽ⣬���ˡ�
II������Һ�еμ�H2O2��Һ���Լ��ȡ�
III����II����Һ�м���CuO��ĩ��pH��4��
IV��������У����ˣ���Һ��ϡ�����ữ��pH��1��
V������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ�����þ��塣
��֪�����������������������pH��Ksp��25�棩���±���
| ���� | Fe(OH)3 | Fe (OH)2 | Cu(OH)2 |
| ��ʼ����ʱpH | 2.7 | 7.6 | 4.7 |
| ��ȫ����ʱpH | 3.7 | 9.6 | 6.7 |
| Ksp | 4.0��10�C38 | 8.0��10�C16 | 2.2��10�C20 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��1��������pH="5" HCl��Һ��pH=5��AlCl3��Һ����ˮ���������c (H+) ֮�ȵ��� ��
��2��д����ĭ��������ʱ������Ӧ�����ӷ���ʽ ��
��3�������½�0.01molCH3COONa��0.02mol��������ˮ�����0.5L�����Һ����Һ�й��� ������������Ũ�ȴӴ�С��˳��Ϊ ��
��4�������£���100 mL 0.01 mol��L��1HA��Һ��μ���0.02 mol��L��1MOH��Һ��ͼ����ʾ���߱�ʾ�����Һ��pH�仯�����������Һ���ʱ������仯����
�ش��������⣺
����ͼ����Ϣ��֪HAΪ_______�ᣨ�ǿ���������� �� K���Ӧ����Һ��c(M+)��c(MOH)= mol��L��1��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com