
����Ŀ��ij�¶��£���ˮ(D2O)�����ӻ�����Ϊ1.6��10-15���ö���pHһ�����涨pD����pD=-lg[c(D+))�����¶��£�����������ȷ����
A. ��������ˮ(D2O)�У�pD=7
B. ��������ˮ�У�c(D+)��c(OD-) > 1��10-14
C. ��0.01 mol DC1����ˮ�γ�1 L����ˮ��Һ����pD=2
D. NH4Cl����D2O�����ɵ�һˮ�ϰ���ˮ�������ӵĻ�ѧʽΪNH3��D2O��HD2O+
 ������ʱ����ҵ����ϵ�д�
������ʱ����ҵ����ϵ�д� ��ĩ���ƾ�ϵ�д�
��ĩ���ƾ�ϵ�д� ���ɿ��ñ���ϵ�д�
���ɿ��ñ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Һ�У���ӦA+2B![]() C�ֱ������ֲ�ͬʵ�������½��У����ǵ���ʼ״̬��Ϊc(A) = 0.100 mol��L-1 c(B) = 0.200 mol��L-1 ��c(C) = 0 mol��L-1 �������������£���Ӧ��A��Ũ����ʱ��ı仯��ͼ��ʾ������˵������ȷ����
C�ֱ������ֲ�ͬʵ�������½��У����ǵ���ʼ״̬��Ϊc(A) = 0.100 mol��L-1 c(B) = 0.200 mol��L-1 ��c(C) = 0 mol��L-1 �������������£���Ӧ��A��Ũ����ʱ��ı仯��ͼ��ʾ������˵������ȷ����

A. ��Ӧ��ƽ�ⳣ������<�� B. ��ӦA+2B![]() C����H >0
C����H >0
C. ʵ����ƽ��ʱB��ת����Ϊ60% D. ʵ����ƽ��ʱc(C) = 0.04 mol��L-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NaOH��Һ�ζ��ڱ���������أ��ڱ����������H2A��Ka1=1.1��103 ��Ka2=3.9��106����Һ�������Һ����Ե��������仯������ͼ��ʾ������b��Ϊ��Ӧ�յ㡣���������������

A. �����Һ�ĵ�������������Ũ�Ⱥ������й�
B. Na+��A2�ĵ�������֮�ʹ���HA��
C. b��Ļ����ҺpH=7
D. c��Ļ����Һ�У�c(Na+)>c(K+)>c(OH)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����
A. ����FeCl3��Һʱ����FeCl3�����ܽ���������Һ�У��ټ�ˮϡ��
B. ��Fe3����CuCl2��Һ�м���CuO������pH�ɳ�ȥ��Һ�л��е�Fe3��
C. �����������¯����ʱCaSO4������ת����
D. ��AlCl3��6H2O��SOCl2��ϲ����ȣ��ɵõ���ˮAlCl3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ����ʽ�У�������ȷ���ﷴӦ��ɫ�仯����
A. ��CuSO4��Һ�м�������Zn�ۣ���Һ��ɫ��ʧZn+CuSO4![]() Cu+ZnSO4
Cu+ZnSO4
B. �����ʯ��ˮ���ú���ְ�ɫ����Ca(OH)2+CO2![]() CaCO3��+H2O
CaCO3��+H2O
C. Na2O2�ڿ����з��ú��ɵ���ɫ��Ϊ��ɫ2Na2O2![]() 2Na2O+O2��
2Na2O+O2��
D. ��Mg(OH)2����Һ�еμ�����FeCl3��Һ���ֺ��ɫ����3Mg(OH)2+2FeCl3![]() 2Fe(OH)3+3MgCl2
2Fe(OH)3+3MgCl2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��T �棬�ֱ���10 mLŨ�Ⱦ�Ϊ1 mol/L����������HA��HB�в��ϼ�ˮϡ�ͣ�����pH�������ⶨ��ҺpH��������ҺpH������(2pH)����ҺŨ�ȶ���(lgc)�Ĺ�ϵ��ͼ��ʾ��
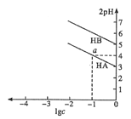
��֪��pKa = -lgKa��
����������ȷ����
A. �����Ka����ҺŨ�ȵĽ��Ͷ�����
B. a���Ӧ����Һ��c(HA) = 0.1 mol/L��pH=4
C. ���ԣ�HA<HB
D. ����HB��pKa��5
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ҹ���ѧ�ҷ�����һϵ�������ش����ϵ�������ϣ�����һ��ΪFeSmAsFO��ɵĻ�����ش��������⣺
��1��Ԫ��As��Nͬ�塣Ԥ��As���⻯����ӵ�����ṹΪ_______����е��NH3��_______�������������������������ж�������_________________________��
��2��Fe��Ϊ������ʱ����ʧȥ______������ӣ�Sm�ļ۲�����Ų�ʽΪ4f66s2��Sm3+�ļ۲�����Ų�ʽΪ______________________��
��3���Ƚ����Ӱ뾶��F__________O2����������������������С��������
��4��һ���ķ��ṹ�ij���������ľ����ṹ��ͼ1��ʾ��������Sm��Asԭ�ӵ�ͶӰλ����ͼ2��ʾ��

ͼ��F��O2��ͬռ�ݾ��������µ���λ�ã������ߵı���������x��1x��������û�����Ļ�ѧʽ��ʾΪ____________��ͨ���ⶨ�ܶ����;������������Լ�������ʵ�xֵ��������ǹ�ϵ����ʽ����=________g��cm3��
�Ծ�������Ϊ��λ���Ƚ���������ϵ���Ա�ʾ�����и�ԭ�ӵ�λ�ã�����ԭ�ӷ������꣬����ͼ1��ԭ��1������Ϊ(![]() )����ԭ��2��3������ֱ�Ϊ__________��__________��
)����ԭ��2��3������ֱ�Ϊ__________��__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ϩ����Ҫ�Ļ���ԭ�ϡ���ʵ�����Ʊ��������£�

�ش��������⣺
��������ϩ���Ʊ����ᴿ
��1��ԭ�ϻ������������������ʣ������Լ�Ϊ____________������Ϊ__________________��
��2������1��װ����ͼ��ʾ�����Ⱥͼг�װ������ȥ����

����ƿA�н��еĿ��淴Ӧ��ѧ����ʽΪ________________________��Ũ����Ҳ�����÷�Ӧ�Ĵ�����ѡ��![]() ������Ũ�����ԭ��Ϊ________________________������ţ���
������Ũ�����ԭ��Ϊ________________________������ţ���
a��Ũ������ʹԭ��̼��������![]()
b��![]() ��ȾС����ѭ��ʹ�ã�������ɫ��ѧ����
��ȾС����ѭ��ʹ�ã�������ɫ��ѧ����
c��ͬ�������£���![]() ��Ũ�����ƽ��ת���ʸ�
��Ũ�����ƽ��ת���ʸ�
������B������Ϊ____________��
��3������2�õ��IJ���������____________��
��4��������3�����IJ��貹�룺��װ����װ�ã��������������ʺͷ�ʯ��____________����ȥǰ��֣��ռ�83������֡�
��������ϩ�����IJⶨ
��һ�������£���![]() ����ϩ��Ʒ�м��붨���Ƶõ�
����ϩ��Ʒ�м��붨���Ƶõ�![]() ���뻷��ϩ��ַ�Ӧ��ʣ���
���뻷��ϩ��ַ�Ӧ��ʣ���![]() ������
������![]() ��������
��������![]() ����
����![]() ��
��![]() ����Һ�ζ����յ�ʱ����
����Һ�ζ����յ�ʱ����![]() ����Һ
����Һ![]() ���������ݾ��ѿ۳��������أ���
���������ݾ��ѿ۳��������أ���
�ⶨ�����У������ķ�Ӧ���£�
��![]()
��![]()
��![]()
��5���ζ�����ָʾ��Ϊ____________����Ʒ�л���ϩ����������Ϊ____________������ĸ��ʾ����
��6����������ᵼ�²ⶨ���ƫ�͵���____________������ţ���
a����Ʒ�к��б�������
b���ڲⶨ�����в��ֻ���ϩ�ӷ�
c��![]() ����Һ���ֱ�����
����Һ���ֱ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���Ӧ![]() +H2O
+H2O![]() H2CO3+OH��ƽ�ⳣ��K=2.2��108����NH4HCO3��Һ�Ͱ�ˮ��һ��������ϣ������ڽ�ȡ�����е�ZnO������Һ������������仯�ɺ��ԣ�����ʱ����ָ����Һ�������ʵ���Ũ�ȹ�ϵ��ȷ����
H2CO3+OH��ƽ�ⳣ��K=2.2��108����NH4HCO3��Һ�Ͱ�ˮ��һ��������ϣ������ڽ�ȡ�����е�ZnO������Һ������������仯�ɺ��ԣ�����ʱ����ָ����Һ�������ʵ���Ũ�ȹ�ϵ��ȷ����
A. 0.2mol��L1��ˮ��c(NH3��H2O)>c(![]() )>c(OH)>c(H+)
)>c(OH)>c(H+)
B. 0.2mol��L1NH4HCO3��Һ(pH>7)��c(![]() )>c(
)>c(![]() )>c(H2CO3)>c(NH3��H2O)
)>c(H2CO3)>c(NH3��H2O)
C. 0.2mol��L1��ˮ��0.2mol��L1NH4HCO3��Һ�������ϣ�c(![]() )+c(NH3��H2O)=c(H2CO3)+c(
)+c(NH3��H2O)=c(H2CO3)+c(![]() )+c(
)+c(![]() )
)
D. 0.6mol��L1��ˮ��0.2mol��L1NH4HCO3��Һ�������ϣ�c(NH3��H2O)+c(![]() )+c(OH)=0.3mol��L1+c(H2CO3)+c(H+)
)+c(OH)=0.3mol��L1+c(H2CO3)+c(H+)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com