
����Ŀ���о��������ˮ��Һ�е�ƽ�����˽����Ĵ�����ʽ������Ҫ��ʵ�����塣

��1�������£���100mL0.01mol��L-1HA����Һ����μ���0.02mol��L-1MOH��Һ��������Һ��pH��MOH��Һ������仯��ͼ��ʾ����Һ����仯���Բ��ƣ���
�ٳ����£�0.01mol��L-1HA��Һ����ˮ�������c��H+��=_____mol��L-1��
�ڳ�����һ��Ũ�ȵ�MAϡ��Һ��pH=a����a____7����������������������=�����������ӷ���ʽ��ʾ��ԭ��Ϊ_____��
��X��ʱ����Һ��c��H+����c��M+����c��A-���ɴ�С��˳����_____��
��K��ʱ����Һ��c��H+��+ c��M+��- c��OH-��=____molL-1��
��2��25 ��ʱ����֪Ka��CH3COOH����1.75��10��5��Kb��NH3��H2O����1.76��10��5��ȡŨ�Ⱦ�Ϊ0.100 0 mol��L��1�Ĵ�����Һ�Ͱ�ˮ��Һ��20.00 mL����ƿ�У��ֱ���0.1000 mol��L��1NaOH��Һ��0.1000 mol��L��1������еζ����ζ�������pH��μ���Һ����仯��ϵ��ͼ��ʾ��
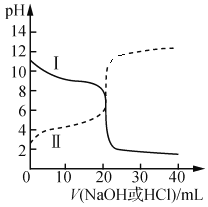
�ٴ�����I��֪���õζ�����ʱ��Ӧѡ______��Ϊָʾ����
�������ߢ��μ���Һ��10.00 mLʱ��
c��CH3COO������c��OH���� ___ c��H������c��CH3COOH�� ����������������������=����
���𰸡�10-12 < M++ H2OMOH+H+ c(A-)> c(H+)> c(M+) 0.0005 ���� >
��������
(1)����pH֪��HAΪǿ�ᣬ��Һ����ˮ�������c(H+)������Һ�е�OH-Ũ�ȡ�
�ڶ���ǿ�������Σ��������ӷ���ˮ�⣬��Һ�����ԡ�
��X��ʱ������Һ�е����ʼ������������з������Ӷ��ó���Һ��c(H+)��c(M+)��c(A-)�ɴ�С��˳��
�ܴӵ���غ���з��������c(A-)��
(2) ����Ϊ�ζ��յ�ʱ����Һ�����ԣ�Ӧѡ��ɫ��Χ�������������ָʾ����
�����øõ���Һ����ɼ�������ˮ������Σ�ȷ����Ũ�ȵ���Դ�С��
��1����ͼ�п��Կ�����0.01mol��L-1HA��pH=2��˵����Ϊǿ�ᡣ
�ٳ����£�0.01mol��L-1HA��Һ����ˮ�������c(H+)= c(OH-)=![]() mol��L-1��
mol��L-1��
�𰸣�10-12��
�ڵ�pH=7ʱ��V(MOH)=51mL��n(HA)=0.001mol��n(MOH)=0.00102mol��MOH�������Ӷ�˵��MAΪǿ�������Σ�pH=a����a<7��
���ӷ���ʽ��ʾ��ԭ��ΪM++ H2OMOH+H+��
�𰸣�<��M++ H2OMOH+H+��
��X��ʱ��n(HA)=0.001mol��n(MOH)=0.0005mol����Ӧ����n(MA)=0.0005mol��ʣ��n(HA)=0.0005mol����Һ��c(H+)��c(M+)��c(A-)�ɴ�С��˳����c(A-)> c(H+)> c(M+)��
�𰸣�c(A-)> c(H+)> c(M+)��
��K��ʱ��n(HA)=0.001mol��n(MOH)=0.002mol����Ӧ����n(MA)=0.001mol��ʣ��n(HA)=0.001mol����Һ��c(H+)+ c(M+)- c(OH-)= c(A-)=0.0005molL-1��
�𰸣�0.0005��
��2���Ӵ���Ͱ�ˮ��������жϣ�����IΪ��ˮ�����ߢ�Ϊ���ᡣ
�ٴ�����I��֪���õζ�����ʱ���ζ��յ������������ڣ�Ӧѡ������Ϊָʾ����
�𰸣����ȡ�
�������ߢ��μ���Һ��10.00 mLʱ��n(CH3COOH)=0.002mol��n(NaOH)=0.001mol��
��Ӧ����Һ�У�n(CH3COOH)=0.001mol��n(CH3COONa)=0.001mol���Դ���ĵ���Ϊ����
c(CH3COO��)��c(OH��) >c(H��)��c(CH3COOH) ��
�𰸣�>��


 �����Ծ�ϵ�д�
�����Ծ�ϵ�д� �ο�����������100��ϵ�д�
�ο�����������100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij���ӷ�Ӧ���漰![]() ��
��![]() ��
��![]() ��
��![]() ��
��![]() ��
��![]() ������������
������������![]() �����ʵ�����ʱ��仯��������ͼ��ʾ���������ж���ȷ���ǣ� ��
�����ʵ�����ʱ��仯��������ͼ��ʾ���������ж���ȷ���ǣ� ��
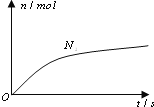
A.��Ӧ����Һ������������ǿ
B.����1mol��ԭ����ת��6mol����
C.�������뻹ԭ�������ʵ���֮��Ϊ2��3
D.�÷�Ӧ�Ļ�ԭ����![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������(���THC)���Ǵ����е���Ҫ����������ʣ���ṹ��ͼ�������й�THC��˵������ȷ����

A. THC������ˮ
B. 1mol THC�����뺬3mol�嵥�ʵ���ˮ������Ӧ
C. THC��FeCl3��Һ�ܷ�����ɫ��Ӧ
D. THC��������������Һ��̼������Һ��̼��������Һ������ѧ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ����
A.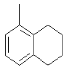 �����е�̼ԭ�ӿ�����ͬһƽ����
�����е�̼ԭ�ӿ�����ͬһƽ����
B.![]() ��һ�ȴ�����4��
��һ�ȴ�����4��
C.![]() ������Ϊ2��3-����-1-����
������Ϊ2��3-����-1-����
D.1mol![]() ��������NaOH��Һ����ˮ��Ӧʱ������NaOH��Br2�����ʵ���Ϊ4mol��2mol
��������NaOH��Һ����ˮ��Ӧʱ������NaOH��Br2�����ʵ���Ϊ4mol��2mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2018�꣬�����˳��ˡ�����Э����ʵ���ٹ�ҵ��ս�ԣ����й�ȴ�Ӵ��˻������ȣ�����ڹ�����ҹ������εĴ�������������ҹ�������ǿ��������CO2���⻯�ϳɼ״������Ĺ�ҵ�������о���ʵ�ֿɳ�����չ��
��1����֪��CO2��g��+ H2��g��![]() H2O��g�� +CO��g�� ��H1 = + 41.1 kJmol-1
H2O��g�� +CO��g�� ��H1 = + 41.1 kJmol-1
CO��g��+2H2��g��![]() CH3OH��g�� ��H2= ��90.0 kJmol-1
CH3OH��g�� ��H2= ��90.0 kJmol-1
д��CO2���⻯�ϳɼ״����Ȼ�ѧ����ʽ_________��
��2��Ϊ���CH3OH���ʣ�������Ӧ���õ�������_________������ĸ����
a ���¸�ѹ b ���µ�ѹ c ���µ�ѹ d ���¸�ѹ
��3��250�桢�����Ϊ2.0 L�ĺ����ܱ������м���6 mol H2��2 mol CO2�ʹ�����10 minʱ��Ӧ�ﵽƽ�⣬���c��CH3OH�� = 0.75 mol�� L��1��
�� ǰ10 min��ƽ����Ӧ����v��H2����______ mol��L��1��min��1��
�� ��ѧƽ�ⳣ����ֵ ______��
��4����CO2��g����H2��g��Ϊԭ�Ϻϳɼ״�����Ӧ�������仯����ͼ��ʾ��

�� ��ȫ��ͼ��ͼ��A��Ӧ����_____��
�� �÷�Ӧ��Ҫ����ͭ��п����������������÷�Ӧ���� H_____���������������С����������������
��5��CO2��������CH4��Ӧ����CH3COOH����Ӧ��������ͼ1�����м����������ϵ�������������ʾ�� ������ij��Һ��CH3COOH��CH3COO��������Ũ����pH�仯�����ߣ�����ͼ2��
���м�����������______�м���ڵ������������>������=������<����
�ڴ�ͼ2�еó��������£�CH3COOH�ĵ��볣��ֵΪ____��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���п�Ժ��ѧ�����Ƶľ�����ϡ��������������������ں˴Ź�����Ӱ��ҽҩ���й㷺��;�����������̵IJ�������������ʾ��![]() ���������������������й�����������ǣ� ��
���������������������й�����������ǣ� ��
A.���������������ɷ�ɢ��ˮ���γɽ��壬����![]() ��Һ�ķ�ɢ��ֱ���൱
��Һ�ķ�ɢ��ֱ���൱
B.�����������������д��ԣ�����Ϊҩ�������������Ƽ���
C.�ڷ�Ӧ���л����������ÿ����Ǵٽ�![]() ת��Ϊ
ת��Ϊ![]()
D.��Ӧ�ڵĻ�ѧ����ʽ��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijʵ��С��ѧϰ�˷�ӦCO2+2Mg![]() 2MgO+C�����֪ʶ����̽��þ�Ƿ���SO2���巴Ӧ�����������ʵ��װ��ͼ(ע��ʯ������һ���ͻ���ϣ������뷴Ӧ)��
2MgO+C�����֪ʶ����̽��þ�Ƿ���SO2���巴Ӧ�����������ʵ��װ��ͼ(ע��ʯ������һ���ͻ���ϣ������뷴Ӧ)��

��ش��������⣺
(1)���ɹ�ѡ������Լ��У�ľ̿��ͭƬ���������ƹ��壬��װ��A�з�����Ӧ�Ļ�ѧ����ʽΪ____________________________________________��
(2)װ��B����ʢ���ҩƷ��______________________��
(3)����a��������___________����������______________________��
(4)ʵ����Ϻ�۲쵽ʯ�������л�ɫ�������ɣ���ʯ�����丽����Ͷ�뵽ϡ�����У���������г�������ζ�����壬��þ��SO2������SO2+2Mg![]() 2MgO+S��Ӧ�⣬�������ķ�Ӧ��____________��
2MgO+S��Ӧ�⣬�������ķ�Ӧ��____________��
(5)��װ��C��D�����ͼ��ʾװ�ã����Ի��������(H2SO3)��Һ��
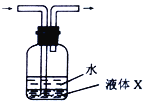
��Һ��X�����������Լ��е�___________(�����)��
A.�� B.���� C.���Ȼ�̼ D.�ƾ�
��ʵ����Ϻ�ͨ��___________(ʵ���������)���Խ��ϡ�������Һ��ֿ���
������������Һ��ͨ���������Һ��pH_______(���������С�����䡱)����ԭ����______(�û�ѧ����ʽ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˸���̵���ʶ±�ص����ʣ�ij��ѧС���±�ؼ��仯������Ʊ������ʽ�������̽��ʵ�飬����ʵ��ش����⡣
[ʵ��һ]�������Ʊ�
��1����С������ͼ��ʵ��װ�����Ʊ�������������������������������ķ�Ӧ(�г�������ȥ)��ÿ�����߿��ʾһ����Ԫװ�ã�������������������װ�õĴ���֮��������___��
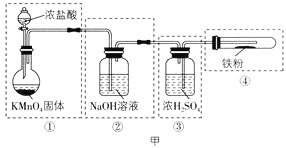
[ʵ���]̽���Ȼ�������������Ӧ�IJ���
��֪�Ȼ��������۵�Ϊ674�棬�е�Ϊ1023�棻���Ȼ�����100������ʱ����������ˮ�⡣��500���������Ȼ��������������ܷ������з�Ӧ��12FeCl2+3O2![]() 2Fe2O3+8FeCl3��4FeCl2+3O2
2Fe2O3+8FeCl3��4FeCl2+3O2![]() 2Fe2O3 +4Cl2���û�ѧС��ѡ��ͼ�Ҳ���װ��(װ�ÿ����ظ�ѡ��)�����Ȼ�������������Ӧ�����̽����
2Fe2O3 +4Cl2���û�ѧС��ѡ��ͼ�Ҳ���װ��(װ�ÿ����ظ�ѡ��)�����Ȼ�������������Ӧ�����̽����
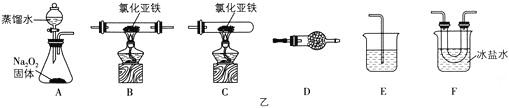
��2��ʵ��װ�õĺ�������˳��ΪA��___��E��
��3��������װ��F�еĹ��������Һ�IJ���������___��
[ʵ����]±�ػ�����֮�䷴Ӧ��ʵ����������̽��
��4���ڲ�ͬʵ��������KClO3�ɽ�KI����ΪI2��KIO3����С��ͬѧ��Ƶ�һ��ʵ������ݼ�¼���±�(ʵ������������½���)��
�Թܱ�� | 1 | 2 | 3 | 4 |
0.20molL-1KI��Һ/mL | 1.0 | 1.0 | 1.0 | 1.0 |
KClO3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
6.0molL-1H2SO4��Һ/mL | 0 | 3.0 | 6.0 | 9.0 |
����ˮ/mL | 9.0 | 6.0 | 3.0 | 0 |
ʵ������ |
�ٸ���ʵ���Ŀ����___��
��2���Թܷ�Ӧ��ȫ��ȡ�����Թ��е���Һ���μӵ�����Һ������ɫ�����軹ԭ����ֻ��KCl��д����Ӧ�����ӷ���ʽ��___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҫ��������и��⡣
(1)��ͼ����������Ӱ��������ζ�Ļ��Գɷֵ�����һ�ַ��ӵĽṹ���京�еĹ�������_______�֣����������ŵ�������________��
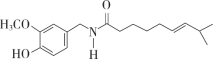
(2)���CH3CH(C2H5)CH(CH3)2��������________��
(3)Ϊ�˲ⶨ������A�Ľṹ��������ʵ�飺
�ٽ�9.2g�÷�����A��ȫȼ�գ����ɱ����15.68L CO2��7.2g H2O��
���������Dzⶨ����Է�������������ͼ��ʾ������ͼ����ͼ��֪�÷��ӵ���Է���������________�����л���A�ķ���ʽΪ________��
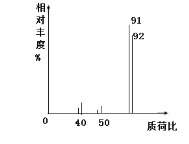
���ú˴Ź������ײ�ø��л������ĸ��壬���ĸ�������֮����1��2��2��3������л���A�Ľṹ��ʽΪ________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com