
【题目】下列事实,不能用勒夏特列原理解释的是( )
A.新制的氯水在光照下颜色变浅
B.H2O2中加入MnO2,产生O2的速度加快
C.合成氨为提高NH3的产率,理论上应采取高压低温的条件
D.氨水应密闭保存、放置于低温处
【答案】B
【解析】
A. 新制的氯水光照,次氯酸分解,次氯酸浓度减小,氯气与水反应平衡正向移动,氯气消耗,颜色变浅,能用勒夏特列原理解释,故A不符合题意;
B. H2O2中加入MnO2,催化剂使产生O2的速度加快,平衡未移动,不能用勒夏特列原理解释,故B符合题意;
C. 合成氨为提高NH3的产率,理论上应采取高压低温的条件,高压,平衡向生成氨气方向移动,反应是放热反应,低温,平衡正向移动,能用勒夏特列原理解释,故C不符合题意;
D. NH3 + H2O![]() NH3H2O
NH3H2O![]() NH4+ + OH-氨水应密闭保存、放置于低温处,有利于氨水长时间保存,温度高,氨气逸出,平衡移动,能用勒夏特列原理解释,故D不符合题意。
NH4+ + OH-氨水应密闭保存、放置于低温处,有利于氨水长时间保存,温度高,氨气逸出,平衡移动,能用勒夏特列原理解释,故D不符合题意。
综上所述,答案为B。


科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y 和 Z 的原子序数依次增大,W 的气态氢化物的水溶液使酚酞变红 并且可与X 的氢化物形成一种共价化合物。Y 是地壳中含量最多的金属元素,Z原子最外层电子数是其内层电子总数的 3/5。下列说法中一定正确的是
A.它们的简单离子半径大小顺序: W<X<Y<Z
B.X的简单气态氢化物稳定性比Z 的强
C.W的氧化物对应水化物为强酸,具有强氧化性
D.工业上一般采取电解Y 的熔融氯化物来生产Y的单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下用![]() 盐酸分别滴定
盐酸分别滴定![]() 浓度均为
浓度均为![]() 的NaOH溶液和二甲胺
的NaOH溶液和二甲胺![]() 溶液
溶液![]() 在水中电离方式与氨相似
在水中电离方式与氨相似![]() ,利电用传感器测得滴定过程中溶液的电导率如图所示。已知电解质溶液电导率越大导电能力越强。
,利电用传感器测得滴定过程中溶液的电导率如图所示。已知电解质溶液电导率越大导电能力越强。
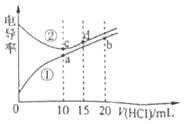
①a、b、c、d四点的水溶液中,由水电离出氢离子浓度大于1.0×10-7![]() 的是______,原因为______。
的是______,原因为______。
②化学反应往往伴有热效应,若为绝热体系,a的温度______![]() 填“
填“![]() ”,“
”,“![]() ”或“
”或“![]() ”
”![]() 点的温度。
点的温度。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】熟悉和使用中学化学实验中常见仪器及用途,是化学学习的基本要求。试回答下列问题。
(1)在仪器a.分液漏斗 b.试剂瓶 c.集气瓶 d.滴定管 e.容量瓶 f.量筒 g.托盘天平中,标有“0”刻度的是________(填序号)。
(2)“磨砂”是增加玻璃仪器密封性的一种处理工艺,在下列仪器中,没有用到“磨砂”工艺处理的有________(填序号)。
a.试管 b.分液漏斗 c.带滴管的试剂瓶(滴瓶)d.集气瓶 e.酸式滴定管 f.碱式滴定管
(3)用装置甲、乙、丙和乳胶管组成一套装置(气密性已检查),可用于制取并收集NH3或HCl气体,可供选择的液体试剂有:浓硫酸、浓盐酸、浓氨水,丙中试剂为紫色石蕊溶液。试回答下列问题:
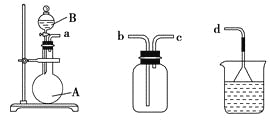
甲 乙 丙
①若制取某气体的过程中,丙中的石蕊溶液变红,且烧瓶中的试剂A与分液漏斗中的试剂B均为无色液体,则试剂A为________,制取该气体利用了B的性质有________、________。
通过丙中紫色石蕊溶液变红或变蓝,说明乙中气体已集满。若石蕊溶液变蓝,则烧瓶甲中应加入的固体试剂A为________。
②若在乙中收集氨气,气体流经装置的顺序是:a―→____―→_____―→d(填接口代号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室利用反应TiO2(s)+CCl4(g) ![]() TiCl4(g)+CO2(g),在无水无氧条件下制取TiCl4,实验装置如图所示(CCl4、TiCl4的沸点分别为76 ℃、136 ℃,CCl4与TiCl4互溶)。下列说法正确的是
TiCl4(g)+CO2(g),在无水无氧条件下制取TiCl4,实验装置如图所示(CCl4、TiCl4的沸点分别为76 ℃、136 ℃,CCl4与TiCl4互溶)。下列说法正确的是
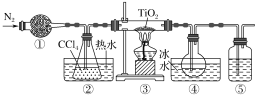
A.①、⑤分别盛装碱石灰、NaOH溶液
B.②中热水的作用是使CCl4汽化,④中冰水的作用是使TiCl4冷凝
C.③中反应结束后,先停止通N2,再停止加热
D.分离④中的液态混合物,采用的操作是分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙苯是主要的化工产品。某课题组拟制备乙苯:查阅资料如下:
①几种有机物的沸点如下表:
有机物 | 苯 | 溴乙烷 | 乙苯 |
沸点/℃ | 80 | 38.4 | 136.2 |
②化学原理: ![]() +CH3CH2Br
+CH3CH2Br![]()
![]() +HBr。
+HBr。
③氯化铝易升华、易潮解。
I.制备氯化铝
甲同学选择下列装置制备氯化铝(装置不可重复使用):

(1)本实验制备氯气的发生装置的玻璃仪器有________种。
(2)连接装置之后,检查装置的气密性,装药品。先点燃A处酒精灯,当___________ 时(填实验现象)点燃F处酒精灯。
(3)气体流动方向是从左至右,装置导管接口连接顺序a→______→k→i→f→g→_____。
(4)D装置存在明显缺陷,若不改进,导致的实验后果是______________。
II.制备乙苯

乙同学设计实验步骤如下:
步骤1:连接装置并检查气密性(如图所示,夹持装置省略)。
步骤2:用酒精灯微热烧瓶。
步骤3:在烧瓶中加入少量无水氯化铝、适量的苯和溴乙烷。
步骤4:加热,充分反应半小时。
步骤5:提纯产品。
回答下列问题:
(5)本实验加热方式宜采用_______ (填“酒精灯直接加热”或“水浴加热”)。
(6)确认本实验A中已发生了反应的试剂可以是___。
A 硝酸银溶液 B 石蕊试液
C 品红溶液 D 氢氧化钠溶液
(7)提纯产品的操作步骤有:
①过滤; ②用稀盐酸洗涤; ③少量蒸馏水水洗 ④加入大量无水氯化钙;⑤用大量水洗; ⑥蒸馏并收集136.2℃馏分 ⑦分液。
操作的先后顺序为⑤⑦__ __⑦__ __⑥(填其它代号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成具有良好生物降解性的有机高分子材料是有机化学研究的重要课题之一。聚醋酸乙烯酯(PVAc)水解生成的聚乙烯醇(PVA),具有良好生物降解性,常用于生产安全玻璃夹层材料PVB。有关合成路线如图(部份反应条件和产物略去)。
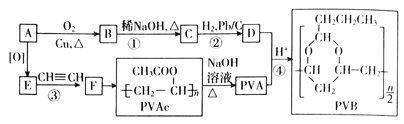
已知:I.A为饱和一元醇,其中氧的质量分数约为34.8%;
II.![]()
![]() ;
;
III.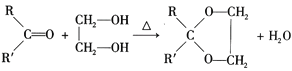 (R、R’可表示烃基或氢原子)
(R、R’可表示烃基或氢原子)
请回答:
(1)C中官能团的名称为_____________,写出C的反式异构体的结构简式:_______________,该分子中最多有______________个原子共面
(2)D与苯甲醛反应的化学方程式为_________________________________________________。
(3)③的反应类型是_________________________
(4)写出两种与F具有相同官能团的同分异构体的结构简式_____________________________。
(5)参照上述信息,设计合成路线,以溴乙烷为原料(其他无机试剂任选)合成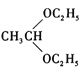 ,_____________
,_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
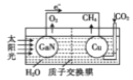
【题目】氮化镓(GaN)被称为第三代半导体材料,其应用取得了突破性的进展。一种镍催化法生产GaN的工艺如图:

(1)“热转化”时Ga转化为GaN的化学方程式是_____。
(2)“酸浸”的目的是_____,“操作Ⅰ”中包含的操作是_____。
某学校化学兴趣小组在实验室利用图装置模拟制备氮化镓:

(3)仪器X中的试剂是_____,仪器Y的名称是_____,装置G的作用是_____。
(4)加热前需先通入一段时间的H2,原因是_____。
(5)取某GaN样品m克溶于足量热NaOH溶液,发生反应 GaN+OH﹣+H2O![]() GaO2-+NH3↑,用H3BO2溶液将产生的NH3完全吸收,滴定吸收液时消耗浓度为c mol/L的盐酸V mL,则样品的纯度是_____。(已知:NH3+H3BO3=NH3H3BO3;NH3H3BO3+HCl=NH4Cl+H3BO3)
GaO2-+NH3↑,用H3BO2溶液将产生的NH3完全吸收,滴定吸收液时消耗浓度为c mol/L的盐酸V mL,则样品的纯度是_____。(已知:NH3+H3BO3=NH3H3BO3;NH3H3BO3+HCl=NH4Cl+H3BO3)
(6)科学家用氮化镓材料与铜组装成如图所示的人工光合系统,成功地实现了用CO2和H2O合成CH4,请写出铜极的电极反应式_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2是一种国际上公认的安全无毒的绿色水处理剂。ClO2易爆炸,若用“惰性气体”等稀释时,爆炸性则大大降低。某化学小组用如图所示装置制备ClO2并处理废水。回答下列问题:
(1)仪器A的作用是__________,C装置的作用为__________。
(2)装置B中发生反应的离子方程式为______________________________。选用以上试剂制备ClO2的优点是______________________________。

(3)ClO2可与工业废水中CN-反应生成对大气无污染的气体,该反应中氧化剂和还原剂的物质的量之比为__________。
(4)有同学认为装置B反应后的溶液中可能存在Cl-,请设计实验验证。简要写出所需试剂、实验操作、现象和结论(已知AgClO3可溶于水)______________________________________。
(5)二氧化氯也可采用电解法生产:4ClO3-+2H2O![]() 4ClO2↑+O2↑+4OH-,写出电解过程中阴极反应方程式为__________________________________________。
4ClO2↑+O2↑+4OH-,写出电解过程中阴极反应方程式为__________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com