
【题目】(6分)对实验:①中和滴定、②中和热的测定、③实验室制备乙烯、④乙酸乙酯的制取,叙述正确的是( )
A. ①④必须加热 B. ②③必须隔热 C. ①②必须用指示剂 D. ③④必须用催化剂
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列各组内的两种海水处理方法都能制取高纯度水的是( )
A.蒸馏法、离子交换法
B.电渗析法、反渗透法
C.蒸发法、反渗透法
D.电渗析法、离子交换法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】300mL Al2(SO4)3溶液中,含Al3+为1.62g,在该溶液中加入0.1molL﹣1 Ba(OH)2溶液100mL,反应后溶液中SO42﹣的物质的量浓度约为( )
A.0.4 molL﹣1
B.0.3 molL﹣1
C.0.2 molL﹣1
D.0.1 molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)体积相同,浓度均为0.2 mol·L-1的盐酸和CH3COOH溶液,分别加水稀释10倍,溶液的pH分别变成m和n,则m与n的关系为_______。
(2)体积相同,浓度均为0.2 mol·L-1的盐酸和CH3COOH溶液,分别加水稀释m倍、n倍,溶液的pH都变成3,则m与n的关系为_______。
(3)体积相同,pH均等于1的盐酸和CH3COOH溶液,分别加水稀释m倍、n倍,溶液的pH都变成3,则m与n的关系为_______。
(4)体积相同,pH均等于13的氨水和NaOH溶液,分别加水稀释m倍、n倍,溶液的pH都变成9,则m与n的关系为_______。
(5)将等体积等物质的量浓度的盐酸和氨水混合后,溶液呈______性(填“酸”、“中”或“碱”,下同),溶液中c(NH![]() )_______c(Cl-)(“>”、“=”或“<”)。
)_______c(Cl-)(“>”、“=”或“<”)。
(6)pH=3的盐酸和pH=11的氨水等体积混合后,溶液呈_______性(填“酸”、“中”或“碱”),溶液中c(NH![]() )________c(Cl-)(“>”、“=”或“<”)。
)________c(Cl-)(“>”、“=”或“<”)。
(7)写出NaHCO3在水溶液中的电离方程式___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们。
(1)卤族元素位于元素周期表的_________区;溴的价电子排布式为_________;
(2)在一定浓度的溶液中,氢氟酸是以二分子缔合(HF)2 形式存在的。使氢氟酸分子缔合的作用力是________;
(3)已知碘酸(HIO3)和高碘酸(H5IO6)的结构分别如图 I、 II 所示:
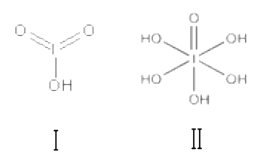
请比较二者酸性强弱: HIO3_____ (填“>”、“<”或“=”)H5IO6;
(4)已知 ClO2- 为 V 形结构,中心氯原子周围有四对价层电子。ClO2-中心氯原子的杂化轨道类型为___________,写出一个ClO2-的等电子体_________;
(5)如图为碘晶体晶胞结构。有关说法中正确的是_____________。
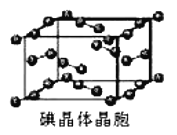
A.碘分子排列有2 种不同取向,2 种取向不同的碘分子以4 配位数交替配位形成层结构
B.用均摊法可知平均每个晶胞中有 4 个碘原子
C.碘晶体为无限延伸的空间结构,是原子晶体
D.碘晶体中存在的相互作用有非极性键和范德华力
(6)已知 CaF2 晶体(如图)的密度为 ρg/cm3, NA为阿伏加德罗常数,棱上相邻的两个 Ca2+的核间距为 a cm,则CaF2 的相对分子质量可以表示为___________。
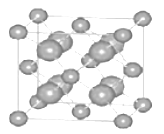
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现用0.1mol/L的HCl溶液滴定10mL0.05mol/L的NaOH溶液,若酸式滴定管未润洗,达到终点时所用盐酸的体积应是
A. 10mL B. 5mL C. 大于5mL D. 小于5mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的用途说法不正确的是
A. Si 可用于制造光导纤维 B. 钠、钾合金可用于原子反应堆作热交换剂
C. FeCl3 溶液可作为铜质电路板蚀刻剂 D. 漂白粉可用于自来水杀菌消毒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】测血钙的含量时,进行如下实验:
①可将2 mL血液用蒸馏水稀释后,向其中加入足量草酸铵(NH4)2C2O4晶体,反应生成 CaC2O4沉淀,将沉淀用稀硫酸处理得H2C2O4溶液。
②将①得到的H2C2O4溶液,再用酸性KMnO4溶液滴定,氧化产物为CO2,还原产物为Mn2+。
③终点时用去20mL l.0×l0-4 mol./L的KMnO4溶液。
(1)写出用KMn04滴定H2C2O4的离子方程式___________。
(2)判断滴定终点的方法是____________。
(3)③步骤中取酸性KMnO4溶液溶液时,酸式滴定管用蒸馏水洗过后没有润洗,则测得的血钙质量分数_______(填“偏大”、“偏小”或“无影响”)。
(4)计算:血液中含钙离子的浓度为_____mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生配制0.1mol·L-1的NaOH溶液500mL,下列说法正确的是( )
A. 不选用胶头滴管
B. 把烧碱固体放在纸上称量
C. 把称好的固体放入容量瓶中稀释至刻度线
D. 定容时俯视容量瓶的刻度线浓度偏大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com