
��֪��
(1)����ʧˮ���Ȼ�ѧ����ʽΪCuSO4��5H2O(s)===CuSO4(s)��5H2O(l) ��H����Q1 kJ/mol
(2)�����£���ˮ����ͭ����ˮ���Ȼ�ѧ����ʽΪCuSO4(s)===Cu2��(aq)��SO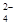 (aq) ��H��
(aq) ��H��
��Q2 kJ/mol
(3)����(CuSO4��5H2O)����ˮʱ��Һ�¶Ƚ��͡���Q1��Q2�Ĺ�ϵ��(Q1��Q2Ϊ����) �� ��
| A��Q1>Q2 | B��Q1��Q2 | C��Q1<Q2 | D����ȷ�� |
A
���������������������ˮ���Կ����������裬��һ����ʧˮ����������Q���ڶ������ǣ���ˮ����ͭ����ˮ���Ƿ��ȵĹ��̣�����˵��������ˮ���������������ͷ��������ɿ�����(1)(2)�ĵ��ӣ����������ʱ�ֵΪQ1+����Q2���������⣬��������ˮʱ�¶Ƚ��ͣ����Կ�֪��������ˮʱһ�����ȵĹ��̣����Q1+����Q2������0���Ӷ���֪Q1>Q2���Դ�ѡA
���㣺���黯ѧ��Ӧ����������ؼ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��Ȼ��������Ҫ����Դ��Ҳ����Ҫ�Ļ���ԭ�ϣ�����Ҫ�ɷ��Ǽ��顣
��1��������һ�������¿����ɣ�
A��̼�����ӣ�CH3-������������ B��̼�����ӣ�CH3-��
C��������CH3�� D��̼ϩ��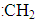 ��
��
���������У�����Ϊ120�����________��������ţ�
����̼�����ӣ�CH3-����Ϊ�ȵ������һ�ַ��ӵĽṹʽΪ_________________________________________________________��
��2�������ش����Ŀ�ȼ���������ˮ��������ڿ�ȼ����˵������ȷ����________��
A�����������ˮ���Ӿ��Ǽ��Է���
B����ȼ���м��������ˮ���Ӽ����������
C����ȼ������ԭ�Ӿ���
D�����������ˮ�����еĦҼ�����s��sp3�������ص����ɵ�
��3���ڸ����£�����ɻ�ԭCuO�õ�Cu2O��
��Cu���ĺ�������Ų�ʽΪ____________��
��Cu2O����ľ����ṹ��ͼ��ʾ�����С��������������ӷ���Ϊ________��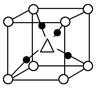
��4��һ�������£�������ˮ����������H2��CO���������ɵ������ЦҼ�������м�����֮��Ϊ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��֪��ӦA+B=C+D�������仯��ͼ��ʾ������˵����ȷ���� �� ��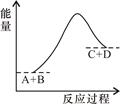
| A���÷�ӦΪ���ȷ�Ӧ |
| B���÷�ӦΪ���ȷ�Ӧ |
| C����Ӧ�������������������������� |
| D���÷�Ӧֻ���ڼ��������²��ܽ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��֪����1 mol C��H����Ҫ��������414.4 kJ������1 mol C��C����Ҫ��������347.4 kJ������1 mol C===C������ų�����615.3 kJ������1 mol H��H������ų�����435.3 kJ��ij�л���ֽ�ķ�Ӧ�ɱ�ʾΪ��
���ڷ�Ӧ��������1 mol����(��Ӧ��)�����йظ÷�Ӧ��˵����ȷ����(����)
| A���÷�Ӧ�ų�251.2 kJ������ | B���÷�Ӧ����251.2 kJ������ |
| C���÷�Ӧ�ų�125.6 kJ������ | D���÷�Ӧ����125.6 kJ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��֪25 �桢101 kPa�£����з�Ӧ
C(ʯī) + O2(g) === CO2(g) ��ȼ��1 mol C(ʯī)����393.51 kJ��
C(���ʯ) + O2(g) === CO2(g)��ȼ��1 mol C(���ʯ)����395.41 kJ��
���Եó��Ľ�����
| A�����ʯ��ʯī�ȶ� | B��1 molʯī�����е�������1 mol���ʯ�� |
| C�����ʯת���ʯī�������仯 | D��ʯī�ͽ��ʯ����̼��ͬλ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
SF6��һ�������ľ�Ե���壬���ӽṹ��ֻ����S-F������֪�� 1molS(s)ת��Ϊ��̬��ԭ����������280kJ,����1molF-F ��S-F�������յ������ֱ�Ϊ160kJ��330kJ����S(s)��3F2(g)=SF6(g)�ķ�Ӧ�ȡ�HΪ
| A��-1780kJ/mol | B��+1220 kJ/mol | C��-1220 kJ/mol | D��+1780 kJ/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��101kPa 25��ʱ��1.0g����������ȫȼ������Һ̬ˮʱ�ų�����52.0kJ��������ȼ�յ��Ȼ�ѧ����ʽΪ
A��C2H6(g) �� 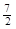 O2(g)��2CO2(g) ��3H2O(l)��H =��1560kJ��mol��1 O2(g)��2CO2(g) ��3H2O(l)��H =��1560kJ��mol��1 |
| B��2C2H6(g) �� 7O2(g)��4CO2(g) ��6H2O(g)��H =��1560kJ��mol��1 |
| C��2C2H6(g) �� 7O2(g)��4CO2(g) ��6H2O(l)��H =��3120 kJ��mol��1 |
D��C2H6(g) ��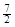 O2(g)��2CO2(g) ��3H2O(l)��H =��52.0kJ��mol��1 O2(g)��2CO2(g) ��3H2O(l)��H =��52.0kJ��mol��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���շ�ӦBr+H2��HBr+H�������淴Ӧ���̱仯��ʾ��ͼ��������������ȷ����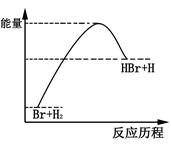
| A������ӦΪ���ȷ�Ӧ |
| B���÷�Ӧ���淴Ӧ�����ȹ��� |
| C��HBr������һ������H2������ |
| D����Ӧ����е�������������������е������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���й�����Ҫ���ȵ��ǡ���������
| A��H2��2H | B��Fe + S  FeS �� FeS �� | C��CaO + H2O = Ca(OH)2 | D��2Cl��Cl2 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com