
| A.熔点由高到低SiO2>CsCl>CBr4>CF4 | B.热稳定性:HF>H2S>H2O |
| C.离子半径:O2->Na+>Mg2+ | D.酸性:HClO4>H2SO4>H3PO4 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:填空题
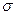 键和
键和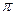 键的数目之比为 ;F、G对应的氢化物中键能大小为F—H键 G—H键。
键的数目之比为 ;F、G对应的氢化物中键能大小为F—H键 G—H键。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 粒子代号 | A | B | C | D | E | F | G |
| 原子核数 | 单核 | 单核 | 双核 | 4核 | 单核 | 多核 | 多核 |
| 电荷数 | 0 | 1+ | 1— | 0 | 2+ | 1+ | 0 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.离子半径 Am+< Bn- | B.A的质子数比B的质子数多(m+n) |
| C.原子半径A < B | D.A在元素周期表中位于B的下一周期 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.溴化氢比氯化氢稳定,HClO4酸性强于HBrO4 |
| B.在周期表中金属和非金属元素的分界线附近可以寻找制取新农药的元素 |
| C.铷的硫酸盐易溶解于水,其氢氧化物一定是弱碱 |
| D.砹是一种有色固体,它的气态氢化物很不稳定, |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com