
| 化学反应 | 平衡 常数 |
温度 | |
| 973k | 1173k | ||
| ①Fe(s)+CO2(g)?FeO(s)+CO(g) | K1 | 1.47 | 2.15 |
| ②Fe(s)+H2O(g)?FeO(s)+H2(g) | K2 | 2.38 | 1.67 |
| ③CO(g)+H2O(g)?CO2(g)+H2(g) | K3 | ? | ? |


| C(CO2).C(H2) |
| C(CO).C(H2O) |
| 1 | ||
|
| C(H2) |
| C(H2O) |
| 1 |
| K1 |
| 1 |
| K1 |
 ,
, ;
;

科目:高中化学 来源: 题型:
 25℃,在20mL 0.1mol?L-1氨水溶液中逐滴加入0.1mol?L-1 HCl溶液,其pH与所加盐酸溶液体积(V/mL)的关系如图所示,下列说法正确的是( )
25℃,在20mL 0.1mol?L-1氨水溶液中逐滴加入0.1mol?L-1 HCl溶液,其pH与所加盐酸溶液体积(V/mL)的关系如图所示,下列说法正确的是( )| A、可以选择酚酞作指示剂 |
| B、在C点,V1<10,且有c(NH4+)=c(Cl-)>c(OH-)=c(H+) |
| C、在A、C间任一点,溶液中一定都有:c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
| D、在D点:c(NH4+)+c(NH3?H2O)═c(Cl-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 阳离子 | NH4+、Na+、Al3+、Ba2+ |
| 阴离子 | SO42-、OH-、Cl-、CO32- |
| c(Br-) |
| c(Cl-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| c(H+) |
| c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
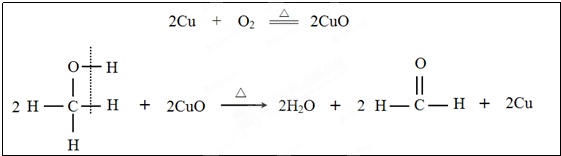
| ||
| 650℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com