
【题目】在反应5H2O + 3BrF3 = Br2 + O2↑+ HBrO3 + 9HF中,当有45克水被氧化时,被水还原的BrF3的物质的量是( )
A. 5/3 mol B. 5/2 mol C. 3/2 mol D. 4/3 mol
科目:高中化学 来源: 题型:
【题目】已知:AgOH很不稳定,易分解生成Ag2O(黑色)。溶液X中可能含有下列离子:Ag+,NH4+、Fe3+、SO42-、SO32-、Cl-中的几种离子。为了确定其组成,某同学进行了如下实验:
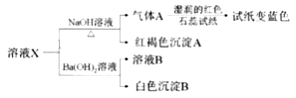
下列说法不正确的是( )
A. 溶液X与NaOH反应生成红褐色沉淀A,可推测该溶液中不存在SO32-
B. 溶液X中一定不含Ag+
C. 溶液X中一定存在NH4+、Fe3+、SO42-
D. 取少量溶液B,加入AgNO3溶液,若有沉淀产生,则有Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅是带来人类文明的重要元素之一,从传统材料到信息材料的发展过程中创造了一个又一个奇迹。
(1)硅在元素周期表中的位置是_______。
(2)工业生产粗硅的反应有:SiO2+2C![]() Si(粗)+2CO↑,SiO2+3C
Si(粗)+2CO↑,SiO2+3C![]() SiC+2CO↑。若产品中单质硅与碳化硅的物质的量之比为1:1,则参加反应的C和SiO2的质量之比为 。
SiC+2CO↑。若产品中单质硅与碳化硅的物质的量之比为1:1,则参加反应的C和SiO2的质量之比为 。
(3)工业上可以通过如下图所示的流程制取纯硅:

①若反应I为 Si(粗)+3HCl![]() SiHCl3+H2,
SiHCl3+H2,
则反应II的化学方程式为 。
②整个制备过程必须严格控制无水无氧。SiHCl3遇水剧烈反应生成H2SiO3、HCl和另 一种物质,写出该反应的化学方程式: 。
③假设每一轮次制备1mol纯硅,且生产过程中硅元素没有损失,反应I中HCl的利用率为90%,反应II中H2的利用率为93.75%,则在第二轮次的生产中,补充投入HCl 和H2的物质的量之比是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某溶液中存在较多的H+、SO42-、NO3-,则溶液中还可能大量存在的离子组是
A. A13+、CH3COO-、C1- B. Na+、NH4+、C1-
C. Mg2+、C1-、Fe2+ D. Mg2+、Ba2+、Br-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家制造出由4个氧原子构成的氧分子,并用质谱仪探测后证实了它的存在。若该氧分子具有空间对称结构,下列关于该氧分子的说法正确的是( )
A. 是氧元素的一种同位素 B. 是臭氧的同分异构体
C. 是一种新的氧化物 D. 是氧气的同素异形体,分子内含有共价键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com