
【题目】如图所示两套实验装置,分别回答下列问题。
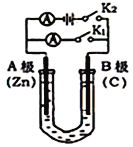
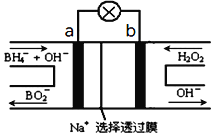
图1 图2
(1)如图1所示,U形管内盛有100mL的溶液,
①打开K2,闭合K1,若所盛溶液为CuSO4溶液:则B极的电极反应式为_______________________。
②打开K1,闭合K2,若所盛溶液为MgCl2溶液,则可观察到的现象是_________________________,总反应化学方程式是_________________________________。
③如要用电解方法精炼粗镍(元素符号Ni),打开K1,闭合K2,电解液选用NiSO4溶液,则A电极的材料应换成是______,反应一段时间后电解质溶液中Ni2+浓度_____(填“增大”、“减小”、“不变”)。
(2)图2装置为硼氢化物NaBH4(B元素的化合价为+3价)燃料电池(DBFC), 由于具有效率高、产物清洁无污染和燃料易于储存和运输等优点,被认为是一种很有发展潜力的燃料电池。
①电池的负极反应式为__________________________
②放电时,每转移2mol电子,理论上需要消耗_________g NaBH4
【答案】Cu2++2e﹣═Cu AB两极都产生气体且A、B两极间溶液变浑浊 MgCl2+2H2O![]() Mg(OH)2↓+H2↑+Cl2↑ 纯镍或精镍 减小 BH4-+8OH--8e-=BO2-+6H2O 9.5g
Mg(OH)2↓+H2↑+Cl2↑ 纯镍或精镍 减小 BH4-+8OH--8e-=BO2-+6H2O 9.5g
【解析】
(1)①打开K2,闭合K1,该装置为原电池, Zn作负极、B极的C作正极;
②打开K1,闭合K2,该装置是电解池,A为阴极、B为阳极;
③如要用电解方法精炼粗镍(元素符号Ni),打开K1,闭合K2,电解液选用NiSO4溶液,粗镍作阳极、纯镍作阴极;
(2)以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,电解质溶液呈碱性,由工作原理装置图可知,负极发生氧化反应,电极反应式为BH4-+8OH--8e-=BO2-+6H2O,正极H2O2发生还原反应,得到电子被还原生成OH-,电极反应式为H2O2+2e-=2OH-,结合原电池的工作原理解答该题。
(1)①打开K2,闭合K1,该装置为原电池,A极的Zn易失电子作负极,电极反应式为Zn-2e-=Zn2+,B极的C作正极,铜离子得电子发生还原反应,电极反应式为Cu2++2e-=Cu;
答案:Cu2++2e﹣═Cu;
②打开K1,闭合K2,该装置是电解池,A为阴极,电极反应式为Mg2++2H2O+2e-=Mg(OH)2↓+H2↑;B为阳极,电极反应式为2Cl--2e-=Cl2↑,总反应为MgCl2+2H2O![]() Mg(OH)2↓+H2↑+Cl2↑;
Mg(OH)2↓+H2↑+Cl2↑;
答案:AB两极都产生气体且A、B两极间溶液变浑浊;MgCl2+2H2O![]() Mg(OH)2↓+H2↑+Cl2↑;
Mg(OH)2↓+H2↑+Cl2↑;
③如要用电解方法精炼粗镍(元素符号Ni),打开K1,闭合K2,电解液选用NiSO4溶液,粗镍作阳极,纯镍作阴极,电解精炼是电解质溶液浓度略有减小,基本不变;
答案:纯镍或精镍;减小;
(2)以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,电解质溶液呈碱性,由工作原理装置图可知,负极发生氧化反应,电极反应式为BH4-+8OH--8e-=BO2-+6H2O,根据电极反应式可知每转移2mol电子,理论上需要消耗NaBH40.25mol,质量为0.25mol×38g/mol=9.5g;
答案:BH4-+8OH--8e-=BO2-+6H2O;9.5g。


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案科目:高中化学 来源: 题型:
【题目】铁是应用最广泛的金属,自远古时代人类就学会了炼铁,到目前为止,人类研制出了很多炼铁的方法。某研究性学习小组同学在实验室中模拟工业炼铁的过程,实验装置如下:

(1)写出得到单质铁的化学方程式:_________________________。
(2)实验过程中看到玻璃管内的粉末由红棕色逐渐变黑,请设计一个实验来验证生成了单质铁:______。
(3)装置末端气球的作用为_____________________________。实验结束时,应该先停止加热还是先停止通入CO?原因是什么?_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用如图所示裝置制备氯气并进行性质实验(必要时可加热,省略夹持装置)
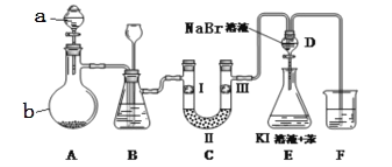
(1)仪器a的名称是:_______;装置B中长颈漏斗的作用是:_______。蒸馏烧瓶b中发生反应的化学方程式为________。
(2)洗气装置B试剂是饱和食盐水,其作用是______,分液漏斗D中发生反应的化学方程式为________。
(3)F处为尾气吸收装置,写出实验室利用烧碱溶液吸收Cl2的离子方程式_______。
(4)设计实验比较氯、溴的氧化性强弱。操作和现象和结论为:取适量溴化钠溶液和苯混合于试管中,通入_______,振荡静置,_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.同一元素各核素的质量数不同,但它们的化学性质几乎完全相同
B.任何元素的原子都是由核外电子和核内中子、质子组成的
C.钠原子失去一个电子后,它的电子数与氖原子相同,所以变成氖原子
D.![]() Ar、
Ar、![]() K、
K、![]() Ca的质量数相同,所以它们是互为同位素
Ca的质量数相同,所以它们是互为同位素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲酸![]() 是还原性酸,又称作蚁酸,常用于橡胶、医药、染料、皮革等工业生产。某化学兴趣小组在分析甲酸的组成和结构后,对甲酸的某些性质进行了探究。请回答下列问题。
是还原性酸,又称作蚁酸,常用于橡胶、医药、染料、皮革等工业生产。某化学兴趣小组在分析甲酸的组成和结构后,对甲酸的某些性质进行了探究。请回答下列问题。

Ⅰ.甲酸能与醇发生酯化反应
该兴趣小组用如上图所示装置进行甲酸![]() 与甲醇
与甲醇![]() 的酯化反应实验:
的酯化反应实验:
有关物质的性质如下:
沸点/℃ | 密度 | 水中溶解性 | |
甲醇 | 64.5 | 0.79 | 易溶 |
甲酸 | 100.7 | 1.22 | 易溶 |
甲酸甲酯 | 31.5 | 0.98 | 易溶 |
(1)装置中,仪器A的名称是__________,长玻璃管c的作用是__________、__________
(2)甲酸和甲醇进行酯化反应的化学方程式为____________________。
(3)要从锥形瓶内所得的混合物中提取甲酸甲酯,可采用的方法为____________________。
Ⅱ.甲酸能脱水制取一氧化碳,一定条件下,![]() 能与
能与![]() 固体发生反应:
固体发生反应:![]() 。
。
(1)如图所示是以甲酸钠![]() 溶液为电解质溶液的甲醇燃料电池:
溶液为电解质溶液的甲醇燃料电池:

则a极电极反应式为_______________。
(2)测定产物中甲酸钠![]() 的纯度:
的纯度:![]() 与足量
与足量![]() 充分反应后,消耗标况下
充分反应后,消耗标况下![]() ,所得固体物质为
,所得固体物质为![]() ,则所得固体物质中甲酸钠的质量分数为_______(计算结果精确到0.1%)。
,则所得固体物质中甲酸钠的质量分数为_______(计算结果精确到0.1%)。
(3)甲酸钠溶液呈弱碱性的原因:__________________(用离子方程式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁与溴化合生成溴化镁,回答下列问题:
(1)镁与溴反应的化学方程式是__。
(2)用电子式表示溴化镁的形成过程__。
(3)用电子式表示离子化合物的形成过程与化学方程式有何不同__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)据中新社2017年6月29日电,也门遭世界最严重霍乱疫情 1400人死亡疑20余万人感染。霍乱是由霍乱弧菌引起的急性肠道传染病,患者常出现呕吐、腹泻、脱水和高烧等症状,重症和延误治疗可致死亡。据联合国儿童基金会专家表示,正常情况下,霍乱可以预防并且治愈率很高,但由于也门基础设施被完全损坏,将很难控制疾病传播。
请根据此信息和题意回答下列问题(填字母,下同)。
a.蛋白质 b.氨基酸 c.葡萄糖 d.变性 e.盐析
①霍乱弧菌中的主要成分中含有____________;该成分经水解后变为__________;
②为了预防霍乱,该疫情地区普遍采用喷洒消毒水进行消毒,对所接触到的器具均采用高温灭菌处理,这是因为在高温条件下病毒和细菌都发生了__________。
(2)化学与材料密切相关,材料是人类生存和发展的物质基础。
①在快中子反应堆中得以广泛应用的钠钾合金在常温下呈液态,这个事实说明合金的熔点比其成分金属的熔点_______(填“高”或者“低”)。
②有机玻璃(聚甲基丙烯酸甲酯)实际上不是硅酸盐材料而是一种线型高分子化合物,它具有_____________性(选填“热塑”或“热固”)。
③据报道,每年我国因金属腐蚀造成的损失占国民生产总值(GDP)的4%。钢铁在潮湿的空气中发生________腐蚀时,负极的电极反应为 ______________。
(3)化学与环境紧密联系。
①空气质量报告的各项指标可以反映出各地空气的质量。下列物质不属于空气污染物的是______(填字母)
a.SO2 b.NO2 c.PM2.5 d.CO2
② 天然水中杂质较多,常需加入明矾,ClO2等物质处理后才能饮用。加入ClO2的作用是__________________;加入明矾后, Al3+水解的离子方程式是 ________________。
③为减少SO2的排放量,可向煤中加入适量 __________(填名称);也可以将煤气化,即在高温条件下与水蒸气反应转化为水煤气,该反应方程式为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列判断中一定正确的是( )
A. NaCl及Na2O2固体中阴、阳离子数之比均为1:1
B. 等质量的O2与O3中,氧原子的个数比为3:2
C. 分别用H2O2、KMnO4分解制O2,当制得等质量O2时,转移电子数之比为1:2
D. 10 mL 0.3 mol·L-1 NaCl溶液与30 mL 0.1 mol·L-1 AlCl3溶液中Cl -物质的量浓度比为1:3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com