
【题目】Ⅰ.用序号回答:①HCl ②NaOH ③Cl2 ④H2O ⑤NH4Cl ⑥P4 ⑦NH3· H2O ⑧Na2O2 ⑨HClO ⑩CaO HF MgCl2。
(1)只存在离子键的是____________________
(2)属于共价化合物的是____________________
(3)既存在离子健又存在共价键的是____________________
Ⅱ.同学们已经学习了同位素、同系物、同素异形体、同分异构体,你能区别这些概念吗?下面列出了几组物质,请将物质的合适组号填写在下表中。
①![]() 和
和![]() ; ②CH3C(CH3)2CH3和
; ②CH3C(CH3)2CH3和![]() ;
;
③CH4和CH3CH2CH3; ④金刚石与石墨;⑤氕、氘与氚;⑥16O、17O和18O;⑦乙醇(CH3CH2OH)和甲醚(CH3OCH3);⑧氧气(O2)与臭氧(O3)。
类别 | 同位素 | 同系物 | 同素异形体 | 同分异构体 |
组号 | ________ | ___________ | ________ | _______ |
【答案】⑩ ①④⑦⑨ ②⑤⑧ ⑤⑥ ①③ ④⑧ ②⑦
【解析】
Ⅰ.①HCl只存在共价键,是共价化合物;
②NaOH存在离子键和共价键,是离子化合物;
③Cl2只含有共价键,是单质;
④H2O只含有共价键,是共价化合物;
⑤NH4Cl存在离子键和共价键,是离子化合物;
⑥P4只含有共价,是单质;
⑦NH3H2O只含有共价,是共价化合物;
⑧Na2O2存在离子键和共价键,是离子化合物;
⑨HClO只含有共价键,是共价化合物;
⑩CaO只含有离子键,是离子化合物;
HF只含有共价键,是共价化合物;
MgCl2只含有离子键,是离子化合物;
(1)只存在离子键的是⑩;
(2)属于共价化合物的是①④⑦⑨;
(3)既存在离子健又存在共价键的是②⑤⑧;
Ⅱ.①![]() 和
和![]() 结构相似,分子组成相差1个“CH2”,故互为同系物;
结构相似,分子组成相差1个“CH2”,故互为同系物;
②CH3C(CH3)2CH3和![]() 分子式相同,但结构不同,故互为同分异构体;
分子式相同,但结构不同,故互为同分异构体;
③CH4和CH3CH2CH3结构相似,分子组成相差2个“CH2”,故互为同系物;
④金刚石与石墨是由碳元素形成的不同单质,故互为同素异形体;
⑤氕、氘、氚质子数相同,中子数不同,故互为同位素;
⑥16O、17O和18O质子数相同,中子数不同,故互为同位素;
⑦乙醇(CH3CH2OH)和甲醚(CH3OCH3)分子式相同,但结构不同,故互为同分异构体;
⑧氧气(O2)与臭氧(O3)由氧元素形成的不同单质,故互为同素异形体;
综上所述:同位素为:⑤⑥;同系物①③;同素异形体为④⑧;同分异构体为②⑦。


 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:高中化学 来源: 题型:
【题目】已知(b)![]() 、(d)
、(d)![]() 、(p)
、(p)![]() 的分子式均为C6H6,下列说法正确的是
的分子式均为C6H6,下列说法正确的是
A. b的同分异构体只有d和p两种B. b、d、p的二氯代物均只有三种
C. b、d、p均可与酸性高锰酸钾溶液反应D. b、d、p中只有b的所有原子处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知短周期元素的离子![]() A2+、
A2+、![]() B+、
B+、![]() C2-、
C2-、![]() D- 都具有相同的电子层结构,则下列叙述中正确的是
D- 都具有相同的电子层结构,则下列叙述中正确的是
A.原子序数d > c > b > aB.离子半径:C2- > D- > B+ > A2+
C.单质的还原性:A > BD.非金属性:D < C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】300mLAl2(SO4)3溶液中,含有Al3+为1.62 克,在该溶液中加入0.1mol/LBa(OH)2溶夜300ml,反应后溶液中SO42-的物质的量浓度约为
A. 0.4 mol/L B. 0.3 mol/L C. 0.1 mol/L D. 0.2mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁被称为“第一金属”,铁及其化合物在生产、生活中有广泛用途。
(1)铁原子核外电子发生跃迁时会吸收或释放不同的光,可以用___________摄取铁元素的原子光谱。
(2)FeCl3的熔点为306℃,沸点为315℃。由此可知FeCl3属于______晶体。FeSO4常作净水剂和补铁剂,SO42-的立体构型是____________。
(3) 铁氰化钾K3[Fe(CN)6]是检验Fe2+的重要试剂。
①基态N原子的轨道表示式为___________。
②写出一种与铁氰化钾中配体互为等电子体的极性分子的化学式_______。
③铁氰化钾中,所涉及的元素的第一电离能由大到小的顺序为____________。
④铁氰化钾中,不存在___________(填字母标号)。
A.离子键 B. σ键 C. π键 D.氢键 E.金属键
(4)有机金属配位化合物二茂铁[(C5H5)2Fe]是汽油中的抗震剂。分子中的大 π键可用符号πmn表示,其中m代表参与形成大π键的原子数, n代表参与形成大π键的电子数(如苯分子中的大π键可表示为π66),则![]() 中的大π键应表示为________,其中碳原子的杂化方式为________。
中的大π键应表示为________,其中碳原子的杂化方式为________。
(5)羰基铁[Fe(CO)5]可用作催化剂、汽油抗爆剂等。1mol [Fe(CO)5]分子中含_____molσ键。
(6)某种磁性氮化铁的结构如图所示,N随机排列在Fe构成的正四 面体空隙中。其中铁原子周围最近的铁原子个数为_____;六棱柱底边长为acm,高为c cm,阿伏加德罗常数的值为NA,则该磁性氮化铁的晶体密度为_________g/cm3(列出计算式)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向X溶液中加入Y试剂,产生沉淀或气体如图,与所述情形几乎完全相符的是( )

A. 向HCl和AlCl3的混合液滴加NaOH溶液 B. 向NH4Al(SO4)2 溶液滴加 Ba(OH)2溶液
C. 向NaOH和Ca(OH)2混合液中通入CO2 D. 向NaOH和Na2CO3混合液滴加稀HCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钠(Na2FeO4)具有很强的氧化性,是一种新型的绿色净水消毒剂。工业上以菱铁矿(主要成分是FeCO3及少量SiO2)为原料制备高铁酸钠生产过程如下:
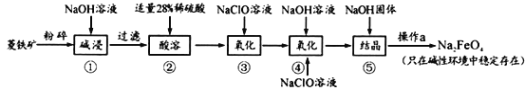
(1)Na2FeO4中铁元素的化合价为_____________,高铁酸钠用于杀菌消毒时的化学反应类型为_______________(填“氧化还原反应”、“复分解反应”或“化合反应”)。
(2)按照上述流程,步骤①中碱浸时能否用较便宜的Ca(OH)2替代NaOH___________ (填“能”或“不能”),理由是________________________。
(3)步骤③中检验Fe2+全部转化成Fe3+的方法是:___________________________。
(4)步骤④中除生成Na2FeO4外,还有NaCl生成,其离子方程式为_____________。己知步骤⑤是向Na2FeO4溶液中继续加入氢氧化钠固体得到悬浊液,则操作a的名称为_____。
(5)生产过程中,理论上每获得0.5mol的FeO42-消耗 NaClO的总质量为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁镍蓄电池又称爱迪生电池,放电时的总反应为:Fe+Ni2O3+3H2O![]() Fe(OH)2+2Ni(OH)2,下列有关该电池的说法不正确的是( )
Fe(OH)2+2Ni(OH)2,下列有关该电池的说法不正确的是( )
A. 电池的电解液为碱性溶液,正极为Ni2O3、负极为Fe
B. 电池充电过程中,阴极附近溶液的酸性增强
C. 电池放电时,负极反应为Fe+2OH--2e-=Fe(OH)2
D. 电池充电时,阳极反应为2Ni(OH)2+2OH--2e-=Ni2O3+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物A由C、H、O三种元素组成,相对分子质量为90。将4.5 g A完全燃烧的产物依次通过足量的浓硫酸和碱石灰,分别增重2.7 g和6.6 g。A能与NaHCO3溶液产生CO2,且两分子A之间脱水可生成六元环状化合物。有关A的说法正确的是
A. 有机物A的分子式为C3H8O3
B. 0.1 mol A与足量Na反应生成2.24 L H2
C. A催化氧化的产物不能发生银镜反应
D. A能在一定条件下发生缩聚反应生成![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com