
用某浓度NaOH溶液滴定一元酸HA的滴定曲线如图所示(横坐标为滴入NaOH的体积,纵坐标为所得混合液的pH;甲基橙变色范围为3.1~4.4)。下列判断正确的是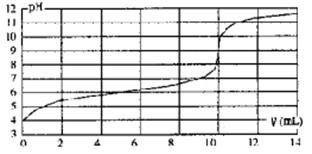
| A.HA的浓度为l×10-4mol·L-1 |
| B.实验时可选甲基橙作指示剂 |
| C.V=10mL,酸碱恰好中和 |
| D.pH=7时,溶液中c(Na+)>c(A-) |
C
解析试题分析:A、根据图像可知恰好反应时溶液的pH=9,溶液显碱性,这说明生成的盐水解,因此HA是弱酸。起始时HA溶液的pH=4,所以HA的浓度大于l×10-4mol·L-1,A不正确;B、反应终点时溶液显碱性,而甲基橙变色范围为3.1~4.4,所以不能选择甲基橙作指示剂,B不正确;C、根据图像可知曲线发生突变是消耗氢氧化钠溶液的体积是10ml,所以V=10mL,酸碱恰好中和,C正确;D、根据电荷守恒可知,pH=7时,即c(H+)=c(OH-),所以溶液中c(Na+)=c(A-),D不正确,答案选C。
考点:考查酸碱中和反应、指示剂选择、弱电解质的电离、溶液中离子浓度大小比较等


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:单选题
常温下,浓度均为0.1000 mol / L的三种一元酸HX、HY、HZ,分别用0. 1000 mol/ L的NaOH溶液进行滴定,滴定曲线如图所示。下列有关叙述正确的是
| A.NaOH溶液与三种酸的反应均是吸热反应 |
| B.滴定酸HY可用酚酞作指示剂 |
| C.酸性强弱:HX>HY>HZ |
| D.滴定三种酸都可用甲基橙作指示剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列混合溶液中,各离子浓度的大小关系不正确的是( )
| A.物质的量浓度相等CH3COOH和CH3COONa溶液等体积混合: c(CH3COO-) + c(CH3COOH)=2c(Na+) |
| B.0.1 mol/L Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+c(H2CO3) |
| C.物质的量浓度相等Na2CO3和NaHCO3溶液等体积混合,离子浓度的大小顺序是 c (Na+)>c (HCO3-)> c(CO32-)>c(OH-)> c(H+) |
| D.NH4Cl溶液中:c(H+) = c(NH3·H2O) +c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是
| A.加入Na2SO4可使溶液由a点变到b点 |
| B.通过蒸发可以使溶液由d点变到c点 |
| C.b点有BaSO4沉淀生成 |
| D.a点对应的Ksp大于c点对应的Ksp |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列事实可证明氨水是弱碱溶液的是( )。
| A.氨水能被弱酸醋酸中和 | B.铵盐受热易分解 |
| C.氨水可以使酚酞试液变红 | D.0.lmol/L氯化铵溶液的pH约为5 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
把Ca(0H)2放入蒸馏水中,—段时间后达到平衡:
下列说法正确的是( )。
| A.向溶液中加CaO,并恢复原温度时,溶液的pH升高 |
| B.给溶液加热,溶液的pH升高 |
| C.向溶液中加入Na2CO3溶液,其中固体质量增加 |
| D.向溶液中加入少量NaOH固体,Ca(0H)2固体质量不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
水的电离平衡曲线如下图所示。下列说法正确的是 ( )
| A.图中对应点的温度关系为A>B |
| B.水的电离常数KW数值大小关系为B>D |
| C.温度不变,加入少量NaOH可使溶液从C点变到A点 |
| D.在B点对应温度下,将pH=2的H2SO4与pH=10的NaOH溶液等体积混合后,溶液显酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是( )
| A.水的离子积常数KW只与温度有关,但外加酸、碱、盐一定会影响水的电离程度 |
| B.Ksp不仅与难溶电解质的性质和温度有关,还与溶液中相关离子的浓度有关 |
| C.常温下,在0.10 mol·L-1的NH3·H2O溶液中加入少量NH4Cl晶体,能使溶液的pH减小,c(NH4+)/c(NH3·H2O)的值增大 |
| D.室温下,CH3COOH的KW=1.7×10-5,NH3·H2O的Kb=1.7×10-5,CH3COOH溶液中的c(H+)与NH3·H2O中的c(OH-)相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
一定温度下的难溶电解质AmBn在水溶液中达到沉淀溶解平衡时,其平衡常数Ksp=cm(An+)×cn(Bm-),称为难溶电解质的溶度积。已知下表数据:
| 物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| Ksp/25 ℃ | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
| 完全沉淀时的pH范围 | ≥9.6 | ≥6.4 | ≥3 |
 )∶[c(Cu2+)+c(Fe2+)+c(Fe3+)]>5∶4
)∶[c(Cu2+)+c(Fe2+)+c(Fe3+)]>5∶4查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com