
| A.除去液溴中少量的氯水,可向其中加少量KI |
| B.氯水和氯气均能使湿润的有色布条褪色,都是HClO作用的结果 |
| C.能与硝酸银反应生成白色沉淀的溶液中一定含有Cl— |
| D.某溶液能使淀粉碘化钾试纸变蓝,则溶液中一定含有Cl2 |
 浙江名校名师金卷系列答案
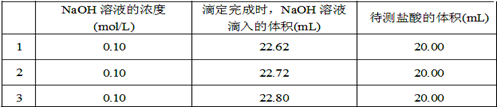
浙江名校名师金卷系列答案科目:高中化学 来源:不详 题型:实验题
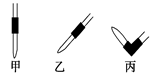
| A.滴定终点读数时俯视读数 | B.碱式滴定管尖嘴部分有气泡,滴定后消失 |
| C.锥形瓶水洗后未干燥 | D.称量NaOH固体中混有Na2CO3固体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
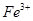 外还可能含有
外还可能含有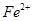 。若要确认其中的
。若要确认其中的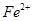 ,应选用 选填序号)。
,应选用 选填序号)。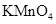 溶液
溶液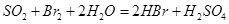 ,然后加入足量
,然后加入足量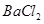 溶液,经适当操作后得干燥固体2.33g。由于此推知气体Y中
溶液,经适当操作后得干燥固体2.33g。由于此推知气体Y中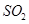 的体积分数为 。
的体积分数为 。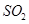 体积分数的结果,丙同学认为气体Y中还可能含量有
体积分数的结果,丙同学认为气体Y中还可能含量有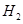 和Q气体。为此设计了下列探究实验状置(图中夹持仪器省略)。
和Q气体。为此设计了下列探究实验状置(图中夹持仪器省略)。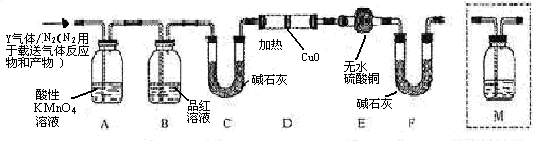
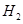 ,预计实验现象应是 。
,预计实验现象应是 。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.氯化钠溶液 | B.苯 | C.碳酸氢钠溶液 | D.四氯化碳 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.加入1 mLNaCl溶液,加热试管,将湿润的红色石蕊试纸靠近试管口 |
| B.加入1 mLNaCl溶液,加热试管,将湿润的蓝色石蕊试纸靠近试管口 |
| C.加入1 mLNaOH溶液,加热试管,将干燥的红色石蕊试纸靠近试管口 |
| D.加入1 mLNaOH溶液,加热试管,将湿润的红色石蕊试纸靠近试管口 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Cl2、SO2均能使品红溶液褪色,说明二者均有氧化性 |
| B.向溶液中滴加酸化的Ba(NO3)2溶液出现白色沉淀,说明该溶液中一定有SO42- |
| C.Fe与稀HNO3、稀H2SO4反应均有气泡产生,说明Fe与两种酸均发生置换反应 |
| D.分别充满HCl、NH3的烧瓶倒置于水中后液面均迅速上升,说明二者均易溶于水 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 O2(g) = H2O(g) △H=-241.8 kJ·mol-1
O2(g) = H2O(g) △H=-241.8 kJ·mol-1查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 产品标准 | GB5461 |
| 产品等级 | 一级 |
| 配料 | 食盐、碘酸钾、抗结剂 |
| 碘含量(以I计) | 20~50mg/kg |
| 分装日期 | |
| 分装企业 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com