
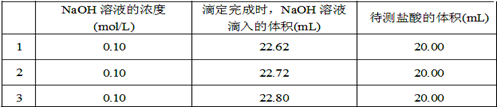
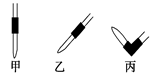
| A.滴定终点读数时俯视读数 | B.碱式滴定管尖嘴部分有气泡,滴定后消失 |
| C.锥形瓶水洗后未干燥 | D.称量NaOH固体中混有Na2CO3固体 |


科目:高中化学 来源:不详 题型:单选题
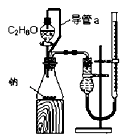 | 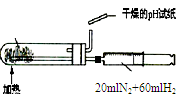 | 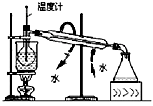 | 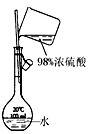 |
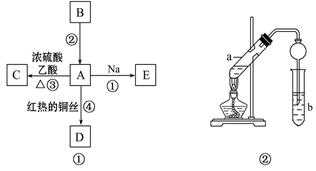
| A.测定乙醇分子结构 | B.合成氨并检验氨的生成并回收CCl4 | C.碘的CCl4溶液中分离I2 | D.配制稀硫酸溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用铁粉与稀硝酸反应,制取少量氢气,用排水法收集 |
| B.在蒸发皿中给十水碳酸钠加热脱水 |
| C.用酸式滴定管量取6.55mL的KMnO4溶液 |
| D.用分液漏斗分离溴乙烷与氢氧化钠溶液发生反应后的生成物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | 实验目的 | 实验方案 |
| A | 研究催化剂对过氧化氢分解速率的影响 | 分别向两支试管中加入等体积、等浓度的过氧化氢溶液,再在其中一只试管中加入少量MnO2 |
| B | 证明Mg(OH)2沉淀可以转化为Fe(OH)3沉淀 | 向2mol/LNaOH溶液中先加入3滴1mol/L MgCl2溶液,再加入3滴1mol/L FeCl3溶液 |
| C | 可以鉴别这两种溶液 | 将Na2CO3溶液与HCl溶液相互滴加 |
| D | 测定铝箔中氧化铝的含量 | 取a g铝箔与足量稀盐酸充分反应,将逸出的气体通过碱石灰后,测其体积为bL(标准状况下) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
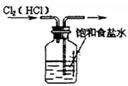 |  | 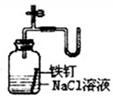 | 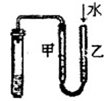 |
| ①除去Cl2中的HCl杂质 | ②用铜和稀硝酸制取少量NO | ③证明铁生锈时空气参与反应 | ④检验装置气密性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 浸出液
浸出液
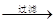 滤液
滤液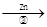
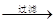 滤液
滤液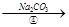
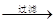 滤饼
滤饼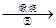 ZnO
ZnO查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 实验方案 | 实验现象 |
| ①用砂纸擦后的镁带与沸水反应,再向反应后溶液中滴加酚酞 | (A)浮于水面,熔成一个小球,在水面上无定向移动,随之消失,溶液变红色 |
| ②向新制的H2S饱和溶液中滴加新制的氯水 | (B)产生气体,可在空气中燃烧,溶液变成浅红色 |
| ③钠与滴有酚酞试液的冷水反应 | (C)反应不十分强烈,产生的气体可以在空气中燃烧 |
| ④镁带与2 mol·L-1的盐酸反应 | (D)剧烈反应,产生可燃性气体 |
| ⑤铝条与2 mol·L-1的盐酸反应 | (E)生成白色胶状沉淀,既而沉淀消失 |
| ⑥向AlCl3溶液滴加NaOH溶液至过量 | (F)生成淡黄色沉淀 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.除去液溴中少量的氯水,可向其中加少量KI |
| B.氯水和氯气均能使湿润的有色布条褪色,都是HClO作用的结果 |
| C.能与硝酸银反应生成白色沉淀的溶液中一定含有Cl— |
| D.某溶液能使淀粉碘化钾试纸变蓝,则溶液中一定含有Cl2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com