
 2Fe+Al2O3;放热;
2Fe+Al2O3;放热; Fe+Al2O3;
Fe+Al2O3;

 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氘原子中的质子和中子 |
| B.C2H4分子中的质子和电子 |
| C.Na2O2固体中的阴离子和阳离子 |
| D.常温下,pH=7的CH3COOH与CH3COONa混合溶液中的H+与OH- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
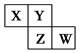
| A.元素W的最高价氧化物对应水化物的酸性最强 |
| B.单核阴离子半径的大小顺序为:r(W)>r(Y)>r(Z) |
| C.元素Y和元素Z的氢化物中均只存在极性共价键 |
| D.元素Y和元素Z的最高正化合价相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
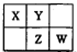
| A.元素X和元素W最高正价代数和一定为8 |
| B.若元素X的原子序数为a,则Z的原子序数一定为a+9 |
| C.常温下,若X的简单氢化物的水溶液能使红色石蕊试液变蓝,则元素Y的简单氢化物的沸点一定高于元素W的简单氢化物 |
| D.原子半径的大小顺序为:rW>rZ>rX>rY |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| X | Y |
| | Z |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.第一电离能:O>N>C |
| B.酸性强弱:HNO3>H2CO3>HClO |
| C.氢化物热稳定性:NH3>PH3>SiH4 |
| D.原子半径大小顺序:r (Mg)>r (Al)>r (N) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
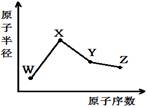
| A.化合物XZW既含离子键也含共价键 |
| B.对应气态氢化物的稳定性Y>Z |
| C.对应简单离子半径:X>W |
| D.Y的氧化物能与Z或X的最高价氧化物对应的水化物反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.TI元素是一种主族元素 |
| B.TI元素的相对原子质量是204 |
| C.铊元素的质量数是204.4 |
| D.TI原子最外层有3个能量相同的电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com