
【题目】一定条件下,可逆反应X(g)+3Y(g)2Z(g),若X,Y,Z起始浓度分别为c1、c2、c3(均不为0,单位mol/L),当达平衡时X,Y,Z的浓度分别为0.1mol/L,0.3mol/L,0.08mol/L,则下列判断不合理的是( )
A.c1:c2=1:3
B.平衡时,Y和Z的生成速率之比为3:2
C.X,Y的转化率不相等
D.c1的取值范围为0<c1<0.14mol/L
【答案】C
【解析】解:X(g) + 3Y(g) ![]() 2Z(g)
2Z(g)
起始: c1 c2 c3
平衡:0.1moL/L 0.3mol/L 0.08mol/L
A.由方程式可知,反应物的物质的量浓度的变化量与化学计量数成正比,则( c1﹣0.1moL/L):(c2﹣0.3mol/L)=1:3,则c1:c2=l:3,故A正确;
B.平衡时,Y和Z的生成速率之比为3:2,说明正逆反应速率相等,反应达到平衡状态,故B正确;
C.反应起始时c1:c2=l:3,由方程式可知,反应物的物质的量变化量与化学计量数呈正比,转化的物质的量也为1:3,则转化率应相等,故C错误;
D.如反应向正反应进行,则c1最小为0,如反应向逆反应方向进行,则c1最大为0.14,因反应为可逆反应,反应物不可能完全转化,则C1的取值范围为0<c1<0.14,故D正确.
故选C.
A.根据反应速率之比等于化学计量数之比判断;
B.反应达到平衡状态时,正逆反应速率相等;
C.根据起始量以及转化量判断转化率关系;
D.从可逆反应的特点的角度分析.


科目:高中化学 来源: 题型:
【题目】硫﹣氨热化学循环制氢示意图如下: 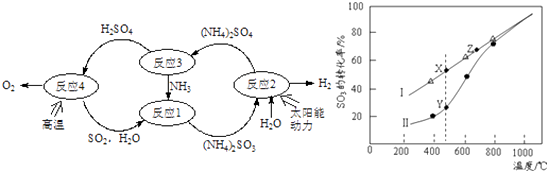
(1)反应1的离子方程式为 .
(2)反应2能量转化主要方式为 .
(3)反应3中控制反应条件很重要,不同条件下硫酸铵分解产物不同.若在400℃时分解,产物除水蒸气外还有A、B、C三种气体,A是空气中含量最多的单质,B能使湿润的红色石蕊试纸变蓝,C能使品红溶液褪色.则400℃时硫酸铵分解的化学方程式为 .
(4)反应4是由(a)、(b)两步反应组成:
H2SO4(l)=SO3(g)+H2O(g),△H=+177kJmol﹣1…(a)
2SO3(g)2SO2(g)+O2(g),△H=+196kJmol﹣1…(b)
①则H2SO4(l)分解为SO2(g)、O2(g)及H2O(g)的热化学方程式为: .
②在恒温密闭容器中,控制不同温度进行SO3分解实验.以SO3起始浓度均为cmolL﹣1 , 测定SO3的转化率,结果如图2,图中Ⅰ曲线为SO3的平衡转化率与温度的关系,Ⅱ曲线表示不同温度下反应经过相同反应时间且未达到化学平衡时SO3的转化率.
(i)图中点X与点Z的平衡常数K:
K(X)K(Z)(选填:>,<,=);
(ii)Y点对应温度下的反应速率:
v(正)v(逆)(选填:>,<,=);
(iii)随温度的升高,Ⅱ曲线逼近Ⅰ曲线的原因是: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】描述CH3﹣CH=CH﹣C≡C﹣CF3分子结构的下列叙述中,正确的是( )
A.6个碳原子有可能都在一条直线上
B.6个碳原子不可能都在一条直线上
C.6个碳原子有可能都在同一平面上
D.6个碳原子不可能都在同一平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有m g某气体,它的摩尔质量为M g·mol-1。若阿伏加德罗常数用NA表示,则:
(1)该气体的物质的量为________mol。
(2)该气体在标况下的密度为__________g/L。
(3)该气体在标准状况下的体积为____________L。
(4)该气体溶于0.1L水中(水的密度:1g·mL-1,且不考虑反应),其溶液中溶质的质量分数为_____。
(5)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为_____mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关系如图所示,由此确定,原溶液中含有的阳离子是( )

A. Mg2+、Al3+、Ba2+ B. H+、Mg2+、Al3+
C. H+、Cu2+、Al3+ D. 只有Mg2+、Al3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来,加“碘”食盐较多的使用了碘酸钾(KIO3),碘酸钾在工业上可用电解法制取.以石墨和不锈钢为电极,以KI溶液为电解液,在一定条件下电解,反应方程式为:KI+3H2O ![]() KIO3+3H2↑.下列有关说法正确的是( )
KIO3+3H2↑.下列有关说法正确的是( )
A.电解时,石墨作阴极,不锈钢作阳极
B.电解时,阳极反应是:I﹣﹣6e﹣+3H2O=IO3﹣+6H+
C.溶液调节至强酸性,对生产有利
D.电解前后溶液的pH几乎不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学反应 2AB+D 在四个不同条件下进行.B、D起始为0.反应物A的浓度(mol/L)随反应时间(min)变化情况如下表:
实验序号 | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
1 | 800℃ | 1.0 | 0.8 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
2 | 800℃ | C2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
3 | 800℃ | C3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
根据表中数据完成下列填空:
(1)在实验1,反应在10至20min内的平均速率为mol/(L.min)
(2)在实验2,A的初始浓度C2=mol/L,反应经20min就达到平衡,可推测实验2中还隐含的条件是 .
(3)设实验3的反应速率为υ3 , 实验1的反应速率为υ1 , 则υ3υ1(填“<“,“=“,“>“),且C31.0mol/L (填“<“,“>“或“=“).
(4)比较实验4和实验1,可推测该反应反应(填“吸热“或”放热“),理由是: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com