
【题目】(1)下列实验操作或叙述正确的是___________(填字母)。
A. 向饱和苯酚钠溶液中,不断通入足量二氧化碳气体,溶液最终呈浑浊
B. 用金属钠检验无水乙醇中含有的少量水
C.除去乙烷中少量的乙烯:与适量的氢气混合加热,把乙烯转化为乙烷
D.向苯酚浓溶液中滴入少量浓溴水可观察到白色的三溴苯酚沉淀
E.用氨水洗去试管内壁的银镜
F.证明氯乙烷分子中含有氯原子,可将氯乙烷溶于AgNO3的HNO3溶液中
G.乙醇与氢溴酸的反应中断裂了O-H 键
H. 甲醛与苯酚制取酚醛树脂的反应属于聚合反应
I.实验室制取乙烯气体时,将温度计的水银球放入液面下
(2)化合物A(C4H8Br2)可由下列反应制得,C4H10O![]() C4H8
C4H8![]() C4H8Br2,则A的结构式不可能的是(______)
C4H8Br2,则A的结构式不可能的是(______)
A.CH3CH2CHBrCH2Br B.CH3CH(CH2Br)2 C.CH3CHBrCHBrCH3 D.(CH3)2CBrCH2Br
【答案】AHI B
【解析】
(1)A、向饱和苯酚钠溶液中,不断通入足量二氧化碳气体,溶液最终呈浑浊,产生苯酚,故正确;
B、乙醇和水都可与钠反应,应用无水硫酸铜检验,故错误;
C、乙烯与氢气的加成反应应在催化剂条件下进行,在实验室难以完成,且易引入新杂质,应用溴水除杂,故错误;
D、向苯酚浓溶液中滴入少量浓溴水,会发生反应,产生白色的三溴苯酚沉淀,但是该沉淀会溶于苯酚中,故错误;
E、氨水和试管内壁的银不会发生反应,故错误;
F、氯乙烷溶于AgNO3的HNO3溶液中不会发生反应,故错误;
G、乙醇与氢溴酸的反应生成溴乙烷和水断裂了O-C键,故错误;
H、甲醛与苯酚制取酚醛树脂的反应属于聚合反应中的缩聚反应,故正确;
I、实验室制取乙烯气体时,加热混合液温度至170℃,将温度计的水银球放入液面下,故正确。
故答案选:AHI;
(2)由转化关系可以知道,C4H10O在浓硫酸、加热的条件下发生消去反应生成C4H8,C4H10O为醇,C4H8为烯烃,
A.若C4H8为CH3CH2CH=CH2,与溴发生加成反应生成CH3CH2CHBrCH2Br,所以A选项是正确的;
B.分子中2个溴原子不是分别连接在相邻的碳原子上,不可能是烯烃与溴的基础产物,故B错误;
C.若C4H8为CH3CH=CHCH3,与溴发生加成反应生成CH3CHBrCHBrCH3,所以C选项是正确的;
D. 若C4H8为(CH3)2C=CH2,与溴发生加成反应生成(CH3)2CBrCH2Br,所以D选项是正确的。
故答案选B。


 优学名师名题系列答案
优学名师名题系列答案科目:高中化学 来源: 题型:
【题目】25℃时,在含CH3COOH和CH3COO-的溶液中, CH3COOH、CH3COO-二者中各自所占的物质的量分数(a)随溶液pH变化的关系如图所示。

下列说法不正确的是
A. 在pH<4.76的溶液中,c(CH3COO-)<c(CH3COOH)
B. 在pH=7的溶液中,a(CH3COOH)=0,a(CH3COO-)=1.0
C. 在pH>4.76的溶液中,c(CH3COO-)与c(OH-)之和可大于c(H+)
D. 在pH=4.76的溶液中加盐酸,a(CH3COOH)与a(CH3COO-)之和保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组用如图所示装置进行实验,探究铁和浓硫酸反应的产物及性质。(夹持装置已略,气密性已检验)
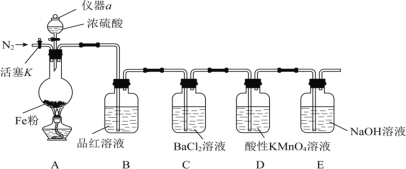
实验开始前,先打开活塞K通一段时间N2。关闭活塞K后,向A中滴加一定量的浓硫酸,加热观察到A中铁片上有气泡产生。
请回答下列问题:
(1)仪器a的名称是___。实验开始前,先通一段时间N2的目的是___。
(2)加热一段时间后发现B装置中溶液褪色,说明有__(填化学式)生成。再取出A中反应后的溶液少许,加入KSCN溶液未出现血红色,浓硫酸与铁反应的化学方程式是__。
(3)C装置中__(填“有”或“无”)沉淀生成。D装置中溶液紫色褪去,该反应的离子方程式为__。
(4)E装置的作用是__。(用离子方程式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A是合成二氢荆芥内酯的重要原料,其结构简式如下图,下列检验A中官能团的试剂和顺序正确的是( )
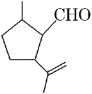
A. 先加酸性高锰酸钾溶液,后加银氨溶液,微热
B. 先加溴水,后加酸性高锰酸钾溶液
C. 先加银氨溶液,微热,再加入溴水
D. 先加入新制氢氧化铜,微热,酸化后再加溴水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,分别向NaX溶液和YCl溶液中加入盐酸和氢氧化钠溶液,混合溶液的PH与离子浓度变化关系如图所示,下列说法不正确的是( )
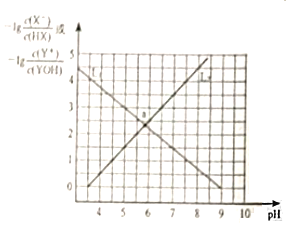
A.0.1mol/L的YX溶液中离子浓度关系为:c(Y+)>c(X-)>c(OH-)>c(H+)
B.L1表示-lg![]() 与pH的变化关系
与pH的变化关系
C.Kb(YOH)=10-10.5
D.a点时两溶液中水的电离程度不相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为:2FeSO4 + 6 Na2O2 = 2Na2FeO4 + 2Na2O + 2Na2SO4 + O2↑,该反应中还原剂是___________________(填化学式),被2 mol FeSO4还原的过氧化钠为_________mol
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。写出碱性条件下制高铁酸钾的离子反应方程式:__________________________
Ⅱ.已知:2Fe3++2I-=2Fe2++I2,2Fe2++Br2=2Fe3++2Br-。
(1)含有1 mol FeI2和2 mol FeBr2的溶液中通入2 mol Cl2,此时被氧化的离子是____________,被氧化的离子的物质的量分别是_____________________________________________
(2)若向含a mol FeI2和b mol FeBr2的溶液中通入c mol Cl2,当I-、Fe2+被氧化时,c为_____________(用含a、b的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】G(异戊酸薄荷醇酯)是一种治疗心脏病的药物。其合成路线如下:
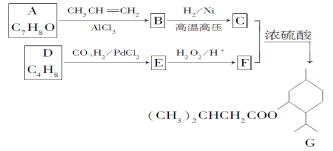
已知:①A能与氯化铁溶液发生显色反应;②RCH=CH2+CO+H2![]() RCH2CH2CHO;③
RCH2CH2CHO;③![]() ;
;
④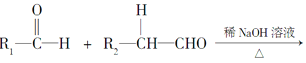
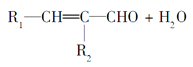 。
。
(1)A的名称为________。
(2)G中含氧官能团名称为________。
(3)D的分子中含有________种不同化学环境的氢原子。
(4)正戊醛可用作香料、橡胶促进剂等,写出以乙醇为原料制备CH3(CH2)3CHO的合成路线流程图(无机试剂任选)。合成路线流程图示例如下: H2C=CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH______________
CH3CH2OH______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中发生下列反应aA(g)![]() cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是( )
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是( )
A. 平衡向正反应方向移动B. a<c+d
C. D的体积分数变大D. A的转化率变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4mol甲烷与氯气发生取代反应,待反应完全后甲烷与氯气均无剩余,测知四种取代物物质的量相同,则消耗的氯气( )
A. 2molB. 10molC. 7.5molD. 16 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com