
| A、Al2O3做氧化剂 |
| B、N2是还原剂 |
| C、AlN既是氧化产物又是还原产物 |
| D、若有1mol CO生成,则反应中有2mol电子转移 |
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案科目:高中化学 来源: 题型:
| A、分别向Na2O2和Na2O与水反应后的溶液中立即滴入酚酞溶液,出现的现象不相同 |
| B、NaHCO3固体中含有的Na2CO3可用加热的方法除去 |
| C、Na2O2和Na2O均为白色固体,与CO2反应均放出O2 |
| D、Na2CO3和NaHCO3均能与盐酸和NaOH溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②④⑥ | B、②③⑥ |
| C、①②④ | D、②③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、强电解质溶液一定比弱电解质溶液的导电性强 |
| B、强电解质的水溶液中不存在分子 |
| C、SO2和乙醇均属共价化合物,在水中都不能电离,均属非电解质 |
| D、不同的弱电解质只要物质的量浓度相同,电离程度也相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Q1<Q2 |
| B、生成物总能量均高于反应物总能量 |
| C、生成1mol HCl气体时放出Q1热量 |
| D、1molHBr(g)具有的能量大于1molHBr(l)具有的能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
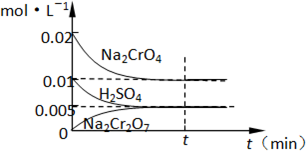 (1)工业酸性废水中含Cr2O72-离子会造成铬污染,排放前先将Cr2O72-还原成Cr3+,并转化成Cr(OH)3除去,工业上采用的方法是向废水中加入NaCl,以铁为电极进行电解,同时鼓入空气.结果溶液的PH值不断升高,溶液由酸性转变为碱性.Cr2O72-转化为毒性较低的Cr3+的离子方程式为:
(1)工业酸性废水中含Cr2O72-离子会造成铬污染,排放前先将Cr2O72-还原成Cr3+,并转化成Cr(OH)3除去,工业上采用的方法是向废水中加入NaCl,以铁为电极进行电解,同时鼓入空气.结果溶液的PH值不断升高,溶液由酸性转变为碱性.Cr2O72-转化为毒性较低的Cr3+的离子方程式为:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电子在核外运动时有确定的轨道和轨迹,电子云就是对其运动轨迹的准确描述 |
| B、原子核外电子在某一时刻的位置可以测定或计算出来 |
| C、人们常用小黑点的疏密程度来表示电子在原子核外出现的概率的大小 |
| D、电子云图中的小黑点表示电子的个数多少 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com