
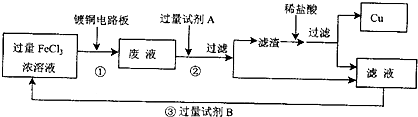
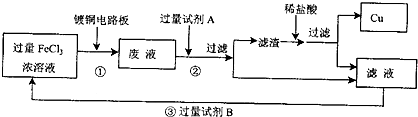
电子工业中常用FeCl3溶液腐蚀印刷电路板,欲从腐蚀后的废液中回收Cu及制取纯净的FeCl3溶液,需要下列试剂:①蒸馏水、②铁粉、③浓H2SO4、④浓盐酸、⑤烧碱、⑥浓氨水、⑦Cl2中的( )
A.①②④⑦ B.①③④⑥
C.②④⑥⑦ D.①④⑥⑦
A
用FeCl3溶液腐蚀印刷电路板发生的反应为:2Fe3++Cu=Cu2++2Fe2+,用蒸馏水稀释腐蚀后的废液;其中存在Fe2+和Cu2+,加入足量铁粉,Fe+Cu2+=Fe2++Cu,过滤后可得到Cu粉和Fe粉的混合物,此时再加入浓盐酸,将Fe粉溶解,过滤后即可回收Cu。在原滤液(主要是Fe2+)中通入足量Cl2则可得到FeCl3溶液,归纳所用试剂为:蒸馏水,铁粉,浓盐酸,氧气。
错因分析:错解B。①忽略加入水后2Fe3++Cu=Cu2++2Fe2+。②加入浓H2SO4后,会产生Fe2+被氧化成Fe3+,但却从外界引入了SO42-,且不易除去,所以氧化剂应选Cl2,而不是浓H2SO4。③最后加入NH3·H2O,会形成Fe(OH)3和Cu(OH)2沉淀,而达不到提纯FeCl3的目的。


 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②④⑦ | B、①③④⑥ | C、②④⑥⑦ | D、①④⑥⑦ |
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:013
A.①②④⑦ B.①③④⑥ C.②④⑥⑦ D.①④⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com