
【题目】下列指定反应的离子方程式正确的是( )
A.![]() 碱性溶液与
碱性溶液与![]() 反应:
反应:![]()
B.室温下用稀![]() 溶液吸收
溶液吸收![]()
C.用铝粉和![]() 溶液反应制取少量
溶液反应制取少量![]()
D.Na与![]() 水溶液反应:
水溶液反应:![]()
科目:高中化学 来源: 题型:
【题目】已知有下图所示物质相互转换关系

试回答:
(1)写出B的化学式__________,D的化学式__________;
(2)写出由E转变成F的化学方程式__________;
(3)向G溶液中加入A的离子方程式__________;
向G溶液中加入铜片的离子方程式__________;
(4)简述B溶液中阳离子的检验方法__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】B、E、H是生活中常见的有机物,H常用于食品包装,A的产量是石油化工发展水平的标志。根据如图转化关系回答问题:
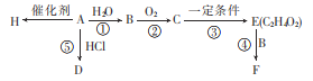
(1)写出A和F中官能团的名称:A___,F___。
(2)反应①、④的反应类型分别为___、___。
(3)写出D和E的结构简式:D___、E___。
(4)请写出下列反应的化学方程式:
I.写出反应②在催化剂存在的条件下并加热的化学方程式:___。
II.A→H的化学方程式:___。
(5)H是一种常见的高分子材料,由这种材料造成的环境问题是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向0.10mol·L-1的H2C2O4(二元弱酸)溶液中滴加NaOH溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示。下列说法不正确的是

A. 25℃时H2C2O4的一级电离常数为Ka1=104.3
B. pH=2.7的溶液中:c(H2C2O4)=c(C2O42-)
C. pH=7的溶液中:c(Na+)>2c(C2O42-)
D. 滴加NaOH溶液的过程中始终存在:c(OH-)+2c(C2O42-)+c(HC2O4-)=c(Na+)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A.将金属钠投入水中: Na+2H2O= Na+ +2OH-+H2↑
B.向AlCl3溶液中加入过量氨水: Al3+ +4NH3·H2O = AlO![]() +4NH
+4NH![]() +2H2O
+2H2O
C.向水中通入NO2: 2NO2+H2O= 2H++ NO![]() +NO
+NO
D.向Na2SiO3溶液中滴加稀盐酸: SiO![]() +2H+ = H2SiO3↓
+2H+ = H2SiO3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为相互串联的甲乙两个电解池,甲池若为用电解精炼铜的装置,请回答:
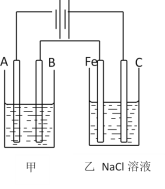
(1)A极材料和B极材料分别是 (_______)
a. 石墨、精铜 b. 石墨、粗铜
c.粗铜、精铜 d.精铜、粗铜
(2)若甲槽阴极增重12.8g,则乙槽阴极放出气体在标准状况下的体积为_________L。
(3)若乙槽剩余液体为400mL,则电解后得到碱液的物质的量浓度为__________ mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验现象与实验操作不相匹配的是( )
A.将镁条点燃后迅速伸入集满![]() 的集气瓶,集气瓶中产生浓烟并有黑色颗粒产生
的集气瓶,集气瓶中产生浓烟并有黑色颗粒产生
B.向盛有![]() 溶液的试管中加过量铁粉,充分振荡后加1滴
溶液的试管中加过量铁粉,充分振荡后加1滴![]() 溶液,黄色逐渐消失,再加
溶液,黄色逐渐消失,再加![]() 后溶液颜色不变
后溶液颜色不变
C.将![]() 溶液加入
溶液加入![]() 溶液中,有白色沉淀生成,
溶液中,有白色沉淀生成,![]() 结合
结合![]() 的能力强于
的能力强于![]()
D.制取较高浓度的次氯酸溶液,将![]() 通入碳酸钠溶液中
通入碳酸钠溶液中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】掌握仪器名称、组装及使用方法是中学化学实验的基础,如图为两套实验装置。
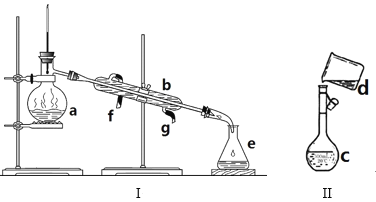
(1)写出下列仪器的名称:a、_____b、 _____
(2)若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器是____,将仪器补充完整后进行实验,温度计水银球的位置在____处。冷凝水由____(填f或g)口通入,___口流出。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可燃冰主要含有甲烷水合物(CH4·nH2O),还含少量CO2等物质。
(1)可燃冰中,CH4分子的空间构型为_______,CO2的电子式为________
(2)工业利用甲烷制氢气,化学方程式为CH4(g) + H2O(g)CO(g) + 3H2(g)
①下列措施能加快反应速率的是_______
a.降低温度 b.增加CH4浓度 c.使用催化剂
②若上述反应在恒容的密闭容器中进行,下列叙述中能说明该反应已达平衡状态的是______
a.c(H2) = 3c(H2O) b.混合气体的质量不再变化 c.单位时间内生成1 mol CO,同时消耗3 mol H2
(3)某种甲烷燃料电池工作原理如图所示:
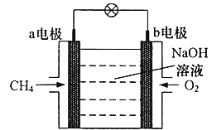
①电子移动方向为________,(填“a→b"或“b→a")
②b电极的电极反应式为____________。
(4)甲烷可催化还原NO,反应历程如图所示:

①该历程中,反应i为CH4+ 12Fe2O3=8Fe3O4+CO2+2H2O,
则反应ii的化学方程式为____________
②工业上催化还原2molNO,理论上需要______LCH4 (标准状况下)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com