
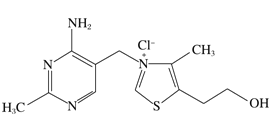
【题目】维生素B1可作为辅酶参与糖的代谢,并有保护神经系统的作用。该物质的结构式如图所示,以下关于维生素B1的说法正确的是
A. 只含σ键和π键
B. 既有共价键又有离子键
C. 该物质的熔点可能高于CsCl
D. 维生素B1晶体溶于水的过程中克服的微粒间作用力只有离子键
【答案】B
【解析】
依据图示结构,维生素B1中含有氯离子及另一种有机离子,存在离子键,B1是分子型物质,熔点不可能高于CsCl,同种元素原子之间形成非极性键,不同元素原子之间形成极性键,据此分析解答。
A.依据结构简式可知,维生素B1含有σ键和π键,离子键,故A错误;B.B1中含有氯离子及另一种有机离子,存在离子键,其它原子之间形成共价键,故B正确;C.B1结构中虽然有离子键,但分子堆积为晶体微粒之间靠的是分子间弱相互作用,而非正负离子吸引,因此属分子晶体,而氯化铯为离子晶体,所以沸点低于氯化铯,故C错误;D.维生素B1晶体溶于水的过程中克服的微粒间作用力:离子键、氢键、范德华力,故D错误;故答案为B。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】正丁醇CH3CH2CH2CH2OH和乙酸在浓硫酸作用下,通过酯化反应制得乙酸正丁酯,反应温度为115~125 ℃,反应装置如图,下列对该实验的描述错误的是( )
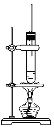
A. 不能用水浴加热
B. 长玻璃管起冷凝回流作用
C. 正丁醇和乙酸至少有一种能消耗完
D. 若加入过量乙酸可以提高醇的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A.密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA
B.1L0.1molL-1NaHCO3溶液中HCO3-和CO32-离子数之和为0.1NA
C.235g核素![]() U发生裂变反应:
U发生裂变反应:![]() U+
U+![]() n
n![]()
![]() Sr+
Sr+![]() Xe+10
Xe+10![]() n,净产生的中子(
n,净产生的中子(![]() n)数为10NA
n)数为10NA
D.标准状况下,11.2L甲烷和乙烯混合物中含氢原子数目为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气溶于水达到平衡后,若其他条件不变,只改变某一条件,下列叙述正确的是( )
A.加入少量水,水的电离平衡向电离方向移动
B.再通入少量氯气,Cl2+H2O![]() HCl+HCIO,平衡向正方向移动,c(Cl2)减少
HCl+HCIO,平衡向正方向移动,c(Cl2)减少
C.通入少量SO2,溶液漂白性增强
D.加入少量固体NaOH,一定有c(Na+)=c(Cl-)+c(ClO-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“题图”是部分元素的离子结构示意图和元素周期表的一部分。 请回答:
(1)图①、②中属于阴离子的是______(填序号),该元素的质子数为______;13号元素原子的最外层电子数为_________。
①![]() ②
②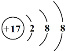
| ||||||
| ||||||
|
| |||||
(2)由表中原子序数为1、8、13的元素组成物质的化学式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜单质及其化合物在很多领域有重要用途,如金属铜用来制造电线电缆,五水合硫酸铜可用作杀菌剂等。
(1)基态Cu2+的核外电子排布式为____________。
(2)科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如下:
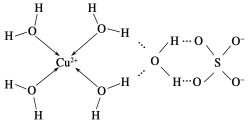
①胆矾的化学式用配合物的形式表示为____________。
②胆矾中SO42-的立体构型名称为________,H2O的VSEPR模型名称为____。
(3)向硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子。已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是______________________。
(4)Cu3N形成的晶体结构如下图所示,N3-的配位数是______。设晶胞边长为a cm,密度为b g/cm3,则阿伏加德罗常数可表示为______________(用含a、b的式子表示)。
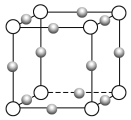
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某一恒温体积可变的密闭容器中发生反应:A(g)+B(g)![]() 2C(g) ΔH<0。t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程如下图所示。下列说法正确的是( )
2C(g) ΔH<0。t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程如下图所示。下列说法正确的是( )
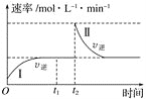
A.O~t2时,v正>v逆
B.Ⅰ、Ⅱ两过程达到平衡时,A的体积分数Ⅰ>Ⅱ
C.t2时刻改变的条件是向密闭容器中加C
D.Ⅰ、Ⅱ两过程达到平衡时,平衡常数Ⅰ<Ⅱ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】证明卤族元素的非金属性强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检查)。
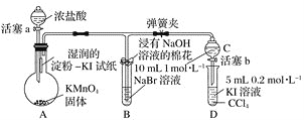
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a。
Ⅳ.……
(1)验证氯气的氧化性强于碘的实验现象是________________________________________。
(2)B中溶液发生反应的离子方程式是____________________________________________。
(3)为验证溴的氧化性强于碘,过程 Ⅳ 的操作和现象是____________________________。
(4)过程Ⅲ实验的目的是________________________________________________________。
(5)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下,原子半径逐渐________,得电子能力逐渐________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将少量稀盐酸滴加到盛有碳酸钙的U形管中,可观察到U形管中的脱脂棉剧烈燃烧。
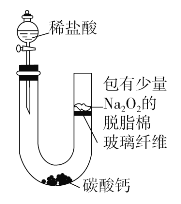
(1)稀盐酸与碳酸钙反应的离子方程式是__________________________
(2)从脱脂棉的燃烧可以推出Na2O2与CO2反应的结论是a.________________,b.________________。
(3)Na2O2与CO2反应的化学方程式是_________________________,还原剂是________,氧化剂是________。(填化学式)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com