
����Ŀ��������Ӧ��ͼ��ͼ�������һһ��Ӧ�����ж��������˵����ȷ����

A. �ܱ������з�Ӧ�ﵽƽ�⣬T0ʱ�ı������Ϊ�������
B. ��Ӧ�ﵽƽ��ʱ�����������ƽ��Ӱ���ϵ��ͼ��ʾ��������ӦΪ���ȷ�Ӧ����a��b
C. ���ʵİٷֺ������¶ȹ�ϵ��ͼ��ʾ����÷�Ӧ������ӦΪ���ȷ�Ӧ
D. ��Ӧ���ʺͷ�Ӧ�����仯��ϵ��ͼ��ʾ����÷�Ӧ������ӦΪ���ȷ�Ӧ����A��B��C�����壬��DΪ�����Һ��
���𰸡�D
��������A�������Ӧǰ������������䣬��ı�ѹǿƽ��Ҳ�Dz��ƶ��ģ�ѡ��A����ȷ��B��ͼ��B�������¶�G�ĺ����ǽ��͵ģ���������Ӧ�����ȷ�Ӧ��ѡ��B����ȷ��C������ͼ��C��֪��ƽ��ʱ������������¶ȣ�C�ĺ����ǽ��͵ģ���˵������Ӧ�Ƿ��ȷ�Ӧ��ѡ��C����ȷ��D�����£�����Ӧ���ʴ�����ӦΪ���ȷ�Ӧ����ѹ������Ӧ���ʴ���A��B��C�����塢DΪ�����Һ�����ƽ�������ƶ�����ͼ��һ�£�ѡ��D��ȷ����ѡD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ϊ2L�Ĺ̶�����������ͨ��3molX���壬��һ���¶��·������·�Ӧ:2X(g) ![]() Y(g)+3Z(g)��
Y(g)+3Z(g)��
(1)��5min��Ӧ�ﵽƽ�⣬�����ڵ�ѹǿΪ��ʼʱ��1.2������Y�ķ�Ӧ����Ϊ________mol/(L��min)��
(2)��������Ӧ�ڼס��ҡ��������ĸ�ͬ�����ܱ������н��У���ͬһ��ʱ���ڲ�������ڵķ�Ӧ���ʷֱ�Ϊ��:v(X)=3.5 mol/(L��min)����:v(Y)=2 mol/(L��min)����:v(Z)=4.5 mol/(L��min)������v(X)=3.5 mol/(L��s)��������������ͬ���¶Ȳ�ͬ�����¶��ɸߵ��͵�˳����(�����)______��
(3)��ﵽ(1)������ƽ����ϵ�г��뺤������ƽ��_______(��������������ҡ���������) �ƶ�����(1)������ƽ����ϵ�����߲���Y���壬��ƽ��_______(��������������ҡ���������) �ƶ���
(4)����ͬ��������ﵽ(1)������ƽ����ϵ���ٳ���0.5molX���壬��ƽ���X��ת������(1)������ƽ����X��ת������Ƚ�_________��
A.��ȷ�� B.ǰ�߶����ں��� C.ǰ��һ�����ں��� D.ǰ��һ��С�ں���
(5)�����¶Ⱥ�ѹǿ���䣬��ʼʱ����X��Y��Z���ʵ����ֱ�Ϊamol��bmol��cmol��aΪ����ֵ���ﵽƽ��ʱ����(1)��ƽ���Ч������b��c������Ĺ�ϵΪ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ҷ����������ᣬ������ˮ����ˮ��Һ������KMnO4��Һ��Ӧ�����ӷ���ʽΪ��2MnO4��+5H2C2O4+6H+=2Mn2++10CO2��+8H2O
Ϊ�˲ⶨ���ᾧ��H2C2O4��xH2O�е�xֵ��ijʵ��С�����ʵ�飬�������£�
�ٳ�ȡ1.260g���ᾧ�壬���100mL��Һ��
��ȡ25.00mL��H2C2O4��Һ������ƿ�ڣ��ټ�������ϡ���ᡣ
����Ũ��Ϊ0.1000mol/L��KMnO4����Һ���еζ������ζ��ﵽ�յ㡣
���ظ�ʵ�顣��¼�����������£�
ʵ����� | V(KMnO4��Һ) | |
�ζ�ǰ�̶�/mL | �ζ���̶�/mL | |
1 | 0.10 | 10.00 |
2 | 1.10 | 11.10 |
3 | 1.50 | 13.50 |
4 | 0.70 | 10.80 |
�ش��������⣺
��1���������Ҫʹ���ձ�����Ͳ������������ͷ�ιܣ���ȱ�ٵIJ�������Ϊ_______(������)������۵ζ������У�ʢװKMnO4��Һ������Ϊ__________________(������)��
��2����ʵ��ζ��ﵽ�յ�ı�־��__________________________;
��3���������ݣ�����H2C2O4��Һ�����ʵ���Ũ��Ϊ______mol/L��x=____________��
��4�����ζ��յ�ʱ���ӵζ��̶ܿȣ���xֵ��______������ƫ��������ƫС����������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ���У��ٹ��ˢ�����������һ�����ʵ���Ũ�ȵ���Һ�����õ��IJ���������
A.������B.������C.�Թ�D.��Һ©��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ӱ�컯ѧ��Ӧ���ʵ���������У��϶���ʹ��ѧ��Ӧ���ʼӿ�ķ�����(����)
�������¶ȡ���ʹ�ô�����������Ӧ��Ũ�ȡ��ܽ���״���巴Ӧ��ĥ�ɷ�ĩ��������ѹǿ
A. �٢ڢۢ� B. �٢ڢܢ� C. �٢ۢ� D. �٢ڢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����(VB2)-���������Ŀǰ����������ߵĵ��,���ʾ��ͼ����,�õ�ع���ʱ��ӦΪ:4VB2+11O2=4B2O3 +2V2O5������˵������ȷ����
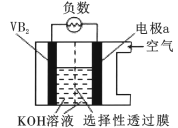
A. �缫a Ϊ�������
B. ͼ��ѡ������ĤΪ����������Ĥ
C. ��ع���������,�缫a��������pH��С
D. VB2�������ĵ缫��ӦΪ:2VB2 +22OH--22e- = V2O5+2B2O3 + 11H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E��Ϊ�л������A�ǻ�ѧʵ����������л����������ˮ����������ζ��B�IJ����ɺ���һ������ʯ�ͻ�����չ��ˮƽ���й����ʵ�ת����ϵ��ͼ����ʾ�� 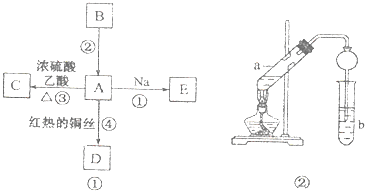
��1��A�й����ŵ�����Ϊ ��
��2��д�����з�Ӧ�Ļ�ѧ����ʽ��Ӧ������Ӧ����
��3��ʵ�������÷�Ӧ����ȡC��������ͼ��װ�ã� ��a�Թ��е���Ҫ��ѧ��Ӧ�ķ���ʽΪ�� ��
����ʵ�������θ���ܳ������������⣬��һ����Ҫ������ ��
���Թ�b�й۲쵽�������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1 mol A(g)��1 mol B(g)Ͷ��һ�ݻ��ɱ���ܱ�������,�������¿��淴Ӧ:A(g)+B(g)![]() xC(g),���ⶨC�ڷ�Ӧ������е����ʵ�������(C%)��ʱ��(t)����ͼ����ʾ��ϵ,�ɴ��ƶ�����˵������ȷ����
xC(g),���ⶨC�ڷ�Ӧ������е����ʵ�������(C%)��ʱ��(t)����ͼ����ʾ��ϵ,�ɴ��ƶ�����˵������ȷ����
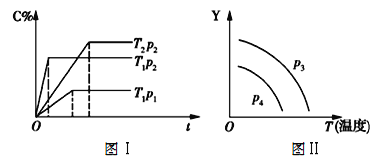
A. ���������淴Ӧ��x=3
B. ��ͼ����p3>p4,Y���ʾ��������ƽ��Ħ������
C. һ���¶���,��ﵽƽ�����������ټ���2 mol C,���´ﵽƽ��ʱ,C�����ʵ�����������
D. ��ͼ����p3<p4,Y���ʾA��ת����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ڵ�����Ϊ���ʣ�����ȥ���и�������������������Լ���д�ں����ϣ�
�����ױ����������Ҵ������ױ����壩 ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com