
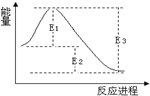
| A. | 该反应常温下一定可以自发进行 | |
| B. | 使用催化剂可以改变E1、E2、E3的大小,从而改变正逆反应速率 | |
| C. | E2为该反应的焓变,且该反应的△H<0 | |
| D. | 该反应反应物能量大于生成物能量,故可设计成原电池 |
分析 A.该反应为放热反应,△G=△H-T•△S<0反应自发进行;
B.使用催化剂可以改变反应的活化能,不能改变焓变;
C.E2为该反应的焓变,△H=E1-E3<0;
D.自发的氧化还原反应可以设计成原电池.
解答 解:A.该反应为放热反应,△H<0,只有满足常温下△G=△H-T•△S<0,反应才能自发进行,故A错误;B.使用催化剂可以改变E1、E3的大小,不能改变E2的大小,故B错误;
C.E2为该反应的焓变,△H=E1-E3<0,故C正确;
D.该反应不一定是自发的氧化还原反应,因此不一定可设计成原电池,故D错误;
故选C.
点评 本题涉及化学反应自发性、物质的能量和反应的吸放热之间的关系、催化剂的特点、原电池原理等知识,属于综合知识的考查,难度中等.


科目:高中化学 来源: 题型:解答题
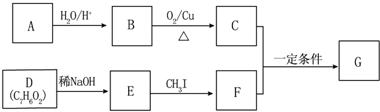
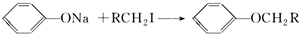
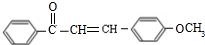 (不要求立体异构).
(不要求立体异构).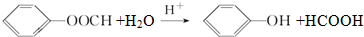 .
.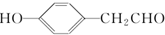 (写结构简式).
(写结构简式).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 在人类社会的发展进程中,金属起着重要的作用.
在人类社会的发展进程中,金属起着重要的作用.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 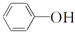 与 与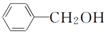 是同系物 是同系物 | |
| B. | 乙酸乙酯(CH3COOCH2CH3)的核磁共振氢谱出现三组峰,且峰面积之比为3:2:3 | |
| C. | 分子式为C4H10的有机物一氯代物共有8种 | |
| D. | 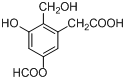 含氧官能团有4种 含氧官能团有4种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
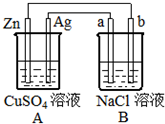 如图所示的装置中电极a、b均为碳棒,两烧杯中所盛溶液均为500mL 1.0mol/L.
如图所示的装置中电极a、b均为碳棒,两烧杯中所盛溶液均为500mL 1.0mol/L.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{a}{36V}$mol/L | B. | $\frac{a}{18V}$mol/L | C. | $\frac{a}{54V}$mol/L | D. | $\frac{a}{27V}$mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
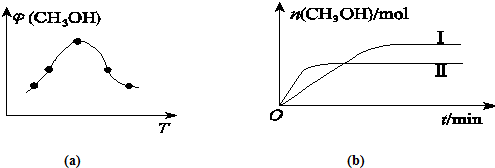
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
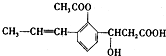 ,下列有关该有机化合物的说法不正确的是
,下列有关该有机化合物的说法不正确的是| A. | 含有四种官能团 | |
| B. | 能发生取代、加成、消去、氧化等反应• | |
| C. | 1mol该有机物最多可以与2molNaOH反应 | |
| D. | 该有机物属于芳香族化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com