
【题目】Fe2O3+2Al![]() Al2O3+2Fe所属基本反应类型是________。在该反应中________元素的化合价升高,该元素的原子________电子,被________;该反应中,________是氧化剂,________是氧化产物;氧化剂与还原剂的物质的量之比为___________;用双线桥标出该反应中电子转移的方向和数目_______________。
Al2O3+2Fe所属基本反应类型是________。在该反应中________元素的化合价升高,该元素的原子________电子,被________;该反应中,________是氧化剂,________是氧化产物;氧化剂与还原剂的物质的量之比为___________;用双线桥标出该反应中电子转移的方向和数目_______________。
 名师点拨卷系列答案
名师点拨卷系列答案科目:高中化学 来源: 题型:
【题目】已知反应:2SO2(g)+O2(g)2SO3(g)△H<0.某温度下,将2mol SO2和1mol O2置于10L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示.则下列说法正确的是( ) 
A.由图甲知,A点SO2的平衡浓度为0.4 mol/L
B.由图甲知,B点SO2、O2、SO3的平衡浓度之比为2:1:2
C.达平衡后,缩小容器容积,则反应速率变化图象可以用图乙表示
D.压强为0.50 MPa时不同温度下SO2转化率与温度关系如丙图,则T2>T1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 5 mol氢 B. 氢氧根离子的摩尔质量为17 g
C. 0.1 mol H 2 O分子约含6.02×10 22 个分子 D. 氩气的摩尔质量在数值上等于它的相对原子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中所涉及的A、B、C、D、E、F和G等都是中学化学教材中常见物质。其中B、E为金属单质,D为气体。反应①②是置换反应,反应①②③均在高温下进行。A为常温下最常见的液体,C有磁性,E、F既能溶于NaOH又能溶于HCl。
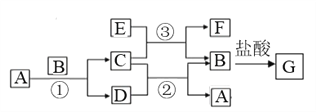
(1)C的俗名_____________,E与足量盐酸反应的离子方程式_________________;
(2)反应③化学方程式_______________________;E加入NaOH溶液中反应的离子反应方程式_______________________;
(3)检验G溶液中金属阳离子的方法________________________;
(4)F与氢氧化钠反应的化学方程式为_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应属于氧化还原反应的是
A. CaCO3+2HCl=CaCl2+CO2↑+ H2O
B. CaO+H2O=Ca(OH)2
C. 2H2O2![]() 2H2O+O2↑
2H2O+O2↑
D. CaCO3![]() CaO+CO2↑
CaO+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】鉴别甲烷、乙烯、乙炔三种气体可采用的方法是( )
A.通入溴水中,观察溴水是否褪色
B.通入酸性高锰酸钾溶液中,观察颜色变化
C.点燃,检验燃烧产物
D.点燃,观察火焰明亮程度及产生黑烟量的多少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以“物质的量”为中心的计算是化学计算的基础,下列与“物质的量”相关的计算正确的是
A.现有CO、CO2、O3三种气体,它们分别都含有1 mol O,则三种气体的物质的量之比为3∶2∶1
B.n g Cl2中有m个Cl原子,则阿伏加德罗常数NA的数值可表示为![]()
C.标准状况下,11.2 L X气体分子的质量为16 g,则X气体的摩尔质量是32
D.5.6 g CO和22.4 L CO2中含有的碳原子数一定相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是
A.乙烯可催熟水果
B.SO2、CO2和NO2都可形成酸雨
C.盐析可提纯蛋白质并保持其生理活性
D.通过石油的裂解可获得乙烯、丙烯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com