
【题目】中华人民共和国国家标准(CB2760﹣2011)规定葡萄酒中SO2最大使用量为0.25gL﹣1 . 某兴趣小组用图(a)装置(夹持装置略)收集某葡萄酒中的SO2 , 并对其含量进行测定. 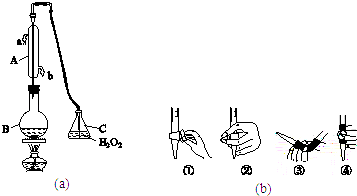
(1)仪器A的名称是 , 水通入A的进口为 .
(2)B中加入300.00mL葡萄酒和适量盐酸,加热使SO2全部逸出并与C中的H2O2完全反应,其化学方程式为 .
(3)除去C中过量的H2O2 , 然后用0.090 0molL﹣1NaOH标准溶液进行滴定,滴定前排气泡时,应选择图(b)中的;若滴定终点时溶液的pH=8.8,则选择的指示剂为;若用50mL滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积(填序号)(①=10mL,②=40mL,③<10mL,④>40mL).
(4)滴定至终点时,消耗NaOH溶液25.00mL,该葡萄酒中SO2含量为gL﹣1 .
(5)该测定结果比实际值偏高,分析原因并利用现有装置提出改进措施: .
【答案】
(1)冷凝管或冷凝器;b
(2)SO2+H2O2=H2SO4
(3)③;酚酞;④
(4)0.24
(5)原因:盐酸的挥发;改进措施:用不挥发的强酸如硫酸代替盐酸(或用蒸馏水代替葡萄酒进行对比实验,扣除盐酸挥发的影响)
【解析】解:(1)根据仪器A的构造可知,仪器A为冷凝管,冷凝管中通水方向采用逆向通水法,冷凝效果最佳,所以应该进水口为b,故答案为:冷凝管或冷凝器;b;(2)双氧水具有氧化性,能够将二氧化硫氧化成硫酸,反应的化学方程式为:SO2+H2O2=H2SO4 ,
故答案为:SO2+H2O2=H2SO4;(3)氢氧化钠溶液为碱性溶液,应该使用碱式滴定管,碱式滴定管中排气泡的方法:把滴定管的胶头部分稍微向上弯曲,再排气泡,所以排除碱式滴定管中的空气用③的方法;滴定终点时溶液的pH=8.8,应该选择酚酞做指示剂(酚酞的变色范围是8.2~10.0);若用50mL滴定管进行实验,当滴定管中的液面在刻度“10”处,滴定管的0刻度在上方,10mL刻度线下方还有40mL有刻度的溶液,另外滴定管50mL刻度线下有液体,因此管内的液体体积>(50.00mL﹣10.00mL)=40.00mL,所以④正确,
故答案为:③;酚酞;④;(4)根据2NaOH~H2SO4~SO2可知SO2的质量为: ![]() ×(0.0900mol/L×0.025L)×64g/mol=0.072g,该葡萄酒中的二氧化硫含量为:
×(0.0900mol/L×0.025L)×64g/mol=0.072g,该葡萄酒中的二氧化硫含量为: ![]() =0.24g/L,
=0.24g/L,
故答案为:0.24;(5)由于盐酸是挥发性酸,挥发的酸消耗氢氧化钠,使得消耗的氢氧化钠溶液体积增大,测定结果偏高;因此改进的措施为:用不挥发的强酸,如硫酸代替盐酸,或用蒸馏水代替葡萄酒进行对比实验,扣除盐酸挥发的影响,
故答案为:原因:盐酸的挥发;改进措施:用不挥发的强酸如硫酸代替盐酸(或用蒸馏水代替葡萄酒进行对比实验,扣除盐酸挥发的影响).
(1)根据仪器A特点书写其名称,为了充分冷却气体,应该下口进水;(2)二氧化硫具有还原性,能够与实验室反应生成硫酸,据此写出反应的化学方程式; (3)氢氧化钠应该盛放在碱式滴定管中,根据碱式滴定管的排气泡法进行判断;根据滴定终点时溶液的pH及常见指示剂的变色范围选用正确的指示剂;根据滴定管的构造判断滴定管中溶液的体积;(4)根据关系式2NaOH~H2SO4~SO2及氢氧化钠的物质的量计算出二氧化硫的质量,再计算出该葡萄酒中的二氧化硫含量;(5)根据盐酸是挥发性酸,挥发的酸消耗氢氧化钠判断对测定结果的影响;可以选用非挥发性的酸或用蒸馏水代替葡萄酒进行对比实验,减去盐酸挥发的影响.


科目:高中化学 来源: 题型:
【题目】3.52 克铜镁合金完全溶解于50mL、密度为1.400g/cm3、质量分数为63%的浓硝酸中,得到NO2气体3584mL(标准状况),向反应后的溶液中加入适量的1.0mo1/LNaOH溶液,恰使溶液中的金属离子全部沉淀。下列说法不正确的是
A. 合金中铜和镁的物质的量相等
B. 加入NaOH溶液的体积是100mL
C. 得到的金属氢氧化物的沉淀为6.24 克
D. 浓硝酸与合金反应中起氧化性的硝酸的物质的量为0.16 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚合物锂离子电池是以Li+嵌入化合物为正、负极的二次电池。如图为一种聚合物锂离子电池示意图,其工作原理为LiNiO2+6C![]() Li1-xNiO2+LixC6,下列说法错误的是
Li1-xNiO2+LixC6,下列说法错误的是

A. 该电池充电可能引起电池正极发生金属锂沉积
B. 充电时当外电路通过1mole-时理论上由2molLi0.9C6转化为Li0.4C6
C. 电池放电时电解质的微粒Li+由负极向正极移动
D. 电池放电时正极的电极反应式为Li1-xNiO2+xLi++xe-=LiNiO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将等体积,等物质的量浓度的NH4HCO3与NaCl溶液混合,析出部分NaHCO3晶体,过滤,所得滤液pH<7.下列关于滤液中的离子浓度关系不正确的是( )
A.![]() <1.0×10﹣7mol/L
<1.0×10﹣7mol/L
B.c(Na+)=c(HCO3﹣)+c(CO32﹣)+c(H2CO3)
C.c(H+)+c(NH4+)>c(OH﹣)+c(HCO3﹣)+2 c(CO32﹣)
D.c(Cl﹣)>c(HCO3﹣)>c(NH4+)>c(CO32﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将2.0molPCl3和2.0molCl2充入体积不变的1L密闭容器中,在一定条件下发生下述反应:PCl3(g)+Cl2(g)PCl5(g) 达到平衡时,PCl5为1.0mol;如果此时将PCl3和Cl2全部移走,在相同温度下再达平衡时PCl5的物质的量是( )
A.0.38mol
B.0.50mol
C.0.62mol
D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在KCl、FeCl3、Fe2(SO4)3三种盐配成的混合溶液中,若c(K+)为0.15 mol/L,c(Fe3+)为0.25 mol/L ,c(Cl-)为0.2 mol/L ,则c(SO42-)为
A. 0.1 mol/L B. 0.15 mol/L
C. 0.25 mol/L D. 0.35 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂废水中含游离态氮,通过下列实验测定其浓度
①取水样10.0mL于锥形瓶,加入10.0mLKI溶液(足量),滴入指示剂2﹣3滴.
②取一滴定管依次用自来水,蒸馏水洗净,然后注入0.01molL﹣1的Na2S2O3溶液,调整液面,记下读数.
③将锥形瓶置于滴定管下进行滴定,发生的反应为:I2+2Na2S2O3=2NaI+Na2S4O6 .
试回答下列问题:
(1)步骤①加入的指示剂是 .
(2)步骤②应使用式滴定管.
(3)试描述滴定终点的现象: .
(4)若耗去Na2S2O3溶液20.00mL,则废水中C12的物质的量浓度为 .
(5)请指出实验中的一处明显错误: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,PbO2与Cr3+反应,产物是Cr2O72-和PbSO4,则参加反应的PbO2与Cr3+的物质的量之比为( )
A.3∶2B.3∶1C.1∶1D.3∶4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com