
| A. | Q1<Q2 | |
| B. | 正交硫不如单斜硫稳定 | |
| C. | 正交硫具有的能量比单斜硫低 | |
| D. | 等质量的单斜硫和正交硫完全燃烧生成的二氧化硫一样多 |
分析 正交硫在一定条件下可以转化为单斜硫需要吸收能量,说明单斜硫具有的能量大于正交硫,物质具有能量越高,其稳定性越弱;物质能量越高,等量燃烧时放热热量越多,据此进行解答.
解答 解:正交硫在一定条件下可以转化为单斜硫需要吸收能量,说明单斜硫具有的能量大于正交硫,
A.由于单斜硫具有的能量大于正交硫,则等质量的二者燃烧时单斜硫放出热量较大,即Q1<Q2,故A正确;
B.单斜硫具有的能量较高,其稳定性较弱,则正交硫比单斜硫稳定,故B错误;
C.根据分析可知,正交硫具有的能量比单斜硫低,故C正确;
D.单斜硫和正交硫都是硫的单质,根据质量守恒定律可知,等质量的单斜硫和正交硫完全燃烧生成的二氧化硫一样多,故D正确;
故选B.
点评 本题考查了反应热与焓变的综合应用,题目难度不大,涉及物质稳定性与具有能量的关系、反应热大小比较等知识,明确化学反应与能量变化的关系为解答关键,注意物质具有能量与稳定性的关系.


科目:高中化学 来源: 题型:解答题
| 温度/℃ | 1000 | 1150 | 1300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤的气化和液化是物理变化 | |
| B. | 煤的干馏是化学变化 | |
| C. | 石油裂解的目的是为了提高轻质油的产量和质量 | |
| D. | 石油的分馏是物理变化,得到的各个馏分都是纯净物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 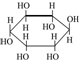 与丙三醇互为同系物 与丙三醇互为同系物 | |
| B. | 高聚物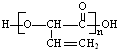 与 与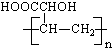 的单体相同 的单体相同 | |
| C. | 按系统命名法,化合物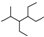 的名称为2-甲基-3,4-乙基己烷 的名称为2-甲基-3,4-乙基己烷 | |
| D. | 等物质的量的甲烷和乙酸完全燃烧时,耗氧量相等,生成的CO2的量也相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④⑤ | B. | ②③⑤⑧ | C. | ②③④⑦ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | NaCl (NaCl ) | B. | MgSO4(MgO) | C. | CuSO4(CuO) | D. | CuCl2(CuCl2) |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
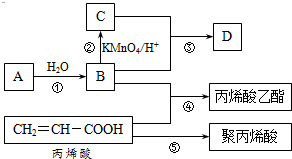 A、B、C、D是四种常见的有机物,其中A是一种气态烃,在标准状况下的密度为1.25g/L;B与C在浓硫酸和加热条件下发生反应,生成的有机物有特殊香味;A、B、C、D在一定条件下的转化关系如图所示v(反应条件已省略):
A、B、C、D是四种常见的有机物,其中A是一种气态烃,在标准状况下的密度为1.25g/L;B与C在浓硫酸和加热条件下发生反应,生成的有机物有特殊香味;A、B、C、D在一定条件下的转化关系如图所示v(反应条件已省略): ,C中官能团的名称为羧基.
,C中官能团的名称为羧基. ,加聚反应.
,加聚反应.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com