
���� ��1������Һ��c��H+��=10-11mol/L��c��OH-��=0.01mol/L��Kw=c��H+����c��OH-���������Һ�����ԣ�˵������n��H+�����ڼ���n��OH-����
��2����25��ʱ��0.1mol/L��HaA��Һ��$\frac{c��{H}^{+}��}{c��O{H}^{-}��}$=1010������Һ��c��H+����c��OH-��=1��10-14�������Һ��c��H+��=0.01mol/L��0.1mol/L��˵�����Ჿ�ֵ��룻
�ڸ��������ᣬ��ˮϡ�ʹٽ����룬�����������̶�С����Һ�������̶ȣ�������Һ��c��H+����С���¶Ȳ��䣬ˮ�����ӻ��������䣻
��NaaA��ǿ�������Σ����������ˮ�����Һ�ʼ��ԣ�
��� �⣺��1������Һ��c��H+��=10-11mol/L��c��OH-��=0.01mol/L��Kw=c��H+����c��OH-��=10-11��0.01=1��10-13��
���¶��£�pH=a��NaOH��Һ��c��OH-��=10a-13��pH=b��H2SO4��Һc��H+��=10-bmol/L��
����Һ�����ԣ�˵������n��H+�����ڼ���n��OH-������a+b=12����c��OH-��=10a-13��Va=10-b��Vb L��Va��Vb=10��1���ʴ�Ϊ��1��10-13��10��1��
��2����25��ʱ��0.1mol/L��HaA��Һ��$\frac{c��{H}^{+}��}{c��O{H}^{-}��}$=1010������Һ��c��H+����c��OH-��=1��10-14�������Һ��c��H+��=0.01mol/L��0.1mol/L��˵�����Ჿ�ֵ��룬�������������ʣ��ʴ�Ϊ��������ʣ�
��a�����������ᣬ��ˮϡ�ʹٽ����룬����Һ��c��HaA����С���ʴ���
b����ˮϡ�ʹٽ�������룬��Һ�����������ʵ�������������ʵ�����С����$\frac{c��{H}^{+}��}{c��HaA��}$ ������ȷ��
c���¶Ȳ��䣬ˮ�����ӻ��������䣬��c��H+����c��OH-���ij˻����䣬�ʴ���
d���¶Ȳ��䣬ˮ�����ӻ��������䣬��Ϊ��ˮϡ����Ȼ�ٽ�����룬�����������̶�С����Һ�������̶ȣ�������Һ��������Ũ�ȼ�С����c��OH-��������ȷ��
��ѡbd��
��NaaA��ǿ�������Σ����������ˮ�����Һ�ʼ��ԣ�ˮ�����ӷ���ʽΪAn++H2O?HA��n-1��++OH-��
�ʴ�Ϊ�����ԣ�An++H2O?HA��n-1��++OH-��
���� ���⿼���������Һ�����жϼ�������ʵĵ��롢����ˮ���֪ʶ�㣬Ϊ��Ƶ���㣬���ؿ���ѧ�������жϼ�����������ע�⣺��ˮϡ����Ȼ�ٽ�������룬������Һ��c��H+������������Ǽ�С��Ϊ�״��㣮


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
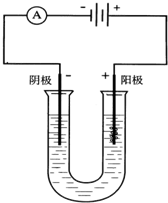 ��ͼ��ʯī���缫�����������Һ��д���缫��Ӧ������ܷ�Ӧʽ��
��ͼ��ʯī���缫�����������Һ��д���缫��Ӧ������ܷ�Ӧʽ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
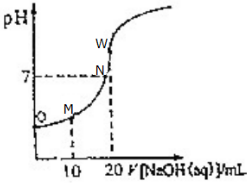
| A�� | N�������NaOHǡ���к� | |
| B�� | O����Һ��pH��1 | |
| C�� | M����ڣ�2c��Na+���Tc��CH3COO-��+c��CH3COOH�� | |
| D�� | W����Һ��ˮ�ĵ���̶���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ�Ӱ뾶Y��Z�����Ӱ뾶Z-��M2+ | |
| B�� | MX2��ˮ������Ӧʱ��MX2ֻ�������� | |
| C�� | X��Y�γɵĻ����������ǿ�ᷴӦ������ǿ�Ӧ | |
| D�� | MX2��MZ2���ֻ������У��������������Ӹ����Ⱦ�Ϊ1��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Q1��Q2 | |
| B�� | �������絥б���ȶ� | |
| C�� | ��������е������ȵ�б��� | |
| D�� | �������ĵ�б�����������ȫȼ�����ɵĶ�������һ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
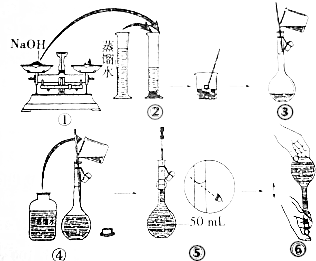
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com