
| 选项 | Na2B2O7 | CaF2 | H3BO3 | NH3 |
| A | 原子晶体 | 金属晶体 | 原子晶体 | 分子晶体 |
| B | 离子晶体 | 分子晶体 | 离子晶体 | 分子晶体 |
| C | 离子晶体 | 离子晶体 | 分子晶体 | 分子晶体 |
| D | 分子晶体 | 离子晶体 | 分子晶体 | 离子晶体 |
| A. | A | B. | B | C. | C | D. | D |
分析 离子晶体是阴、阳离子通过离子键形成的晶体,常见离子晶体有:常见的有强碱、活泼金属氧化物、大多数盐类等;
原子晶体是原子之间通过共价键形成的晶体,常见的原子晶体有:一些非金属单质,若金刚石、硼、硅、锗等;一些非金属化合物,如二氧化硅、碳化硅、氮化硼等;
分子晶体是分子间通过分子间作用力(包括范德华力和氢键)构成的晶体,常见的分子晶体有:所有非金属氢化物、部分非金属单质(金刚石、晶体硅等除外)、部分非金属氧化物(二氧化硅等除外)、几乎所有的酸、绝大多数的有机物晶体、所有常温下呈气态的物质、常温下呈液态的物质(除汞外)、易挥发的固态物质等.
解答 解:Na2B2O7是由Na+、B2O72-通过离子键形成的晶体,属于离子晶体;
CaF2SO2是由Ca2+、F-通过离子键形成的晶体,属于离子晶体;
H3BO3是由H3BO3通过分子间作用力构成的晶体,属于分子晶体;
NH3是由NH3通过分子间作用力构成的晶体,属于分子晶体;
故选:C.
点评 本题考查晶体类型判断,难度不大,掌握常见物质所属晶体类型是解题的关键.


科目:高中化学 来源: 题型:选择题
| A. | $\frac{2a-4b}{V}$ | B. | $\frac{2(a-b)}{V}$ | C. | $\frac{a-2b}{V}$ | D. | $\frac{2a-b}{V}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
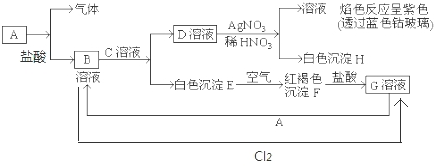
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
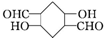 )
)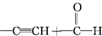 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$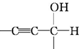
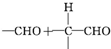 $\stackrel{稀NaOH}{→}$
$\stackrel{稀NaOH}{→}$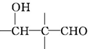
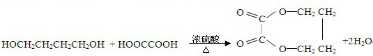 (注明条件).
(注明条件).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢化物的沸点Y>R>X | B. | 含氧酸酸性R>X | ||
| C. | X、Y不可能共存于离子化合物中 | D. | 原子半径Z>R>X>Y |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
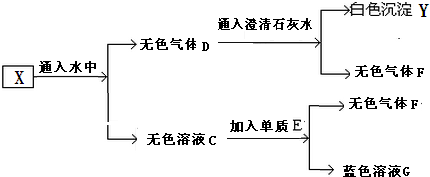
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只含有1个双键的直链有机物 | B. | 含2个双键的直链有机物 | ||
| C. | 含1个双键的环状有机物 | D. | 含一个叁键的直链有机物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com