
【题目】(12分) 为测定NaOH、Na2C03混合物中Na2C03的质量分数,甲同学拟采用图(1)
所示装置来测定。乙同学拟采用图(2)所示装置来测定。
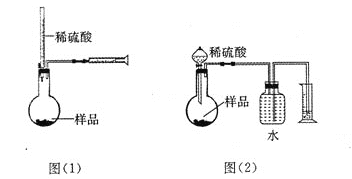
请回答下列问题:
(1)甲同学用图(1)装置来测定,在没有放样品前,检查该装置气密性的方法之一是从酸式滴定管向烧瓶中加入一定量的水,观察到 现象,证明此装量不漏气。实验时称得样品的质量为mg,酸式滴定管的起始读数为amL,终了读数为bmL,注射器测定排出的气体为c mL(已折算成标准状况),该样品中Na2C03的质量分数为(用含a、b、c、m的代数式表示)____ 。
(2)本实验选用稀H2S04而未选用稀盐酸的原因是 。
(3)乙同学观察了甲同学的实验后很受启发,并发现自己的图(2)原实验设计方案会造成误差.其原因之一可能是C02在水中溶解度较大,引起测量气体体积减小。
丙同学经思考后。建议乙同学将图(2)中某部分稍作改进,就可避免此种误差,写出你的改进方案 。
(4)丁同学提出将图(2)装置中量气装置去掉,只用反应装置和天平也能较准确地测出样品中Na2C03的质量分数,请你分析丁同学方案中,除了测定样品的质量,还需测定的另两个数据是 、 。
(5)还可以用其他实验方法测定试样中纯碱的质量分数,请简述一种与上述各方法不同的实验方法 。
【答案】(1)注射器增大的体积与加入水的体积相等。
Na2CO3的质量分数为:m(Na2CO3) /m(样品)=53(c—b+a)/11200m。
(2)稀硫酸不易挥发,稀盐酸易挥发出氯化氢气体,产生误差。
(3)将水换成饱和NaHCO3溶液,或在贮水瓶中的水面上加一层植物油都可防止CO2溶于水。
(4)所需数据:反应前装有药品的整个装置的质量,反应后整个装置的质量。
(5)称量一定质量的样品配成溶液,加入足量的BaCl2溶液后得到沉淀,将沉淀进行过滤、洗涤、干燥、冷却、称量。由沉淀(BaCO3)质量计算出Na2CO3的质量,最后计算出Na2CO3的质量分数。
【解析】试题分析:(1)检查该装置气密性从酸式滴定管向烧瓶中加入一定量的水,密闭性良好时容器内压强增大,注射器活塞会被向外推,直到压强再次与外界大气压平衡,注射器增大的体积与加入水的体积相等;据已知条件得V(CO2)=(c—b+a)mL,n(CO2)= (c—b+a)×10—3L/22.4L/mol=(c—b+a)/22400mol,据C守恒,n(Na2CO3)= n(CO2)= (c—b+a)/22400mol,m(Na2CO3)=n(Na2CO3)×106g/mol=53(c—b+a)/11200g,所以样品中Na2C03的质量分数=m(Na2CO3)/m=53(c—b+a)/11200m。
(2)本实验选用稀H2S04而未选用稀盐酸是因为稀硫酸不易挥发,稀盐酸易挥发出氯化氢气体,产生误差。
(3)可以利用CO2在饱和NaHCO3溶液溶解度非常小将水换成饱和NaHCO3溶液,或在贮水瓶中的水面上加一层植物油都可防止CO2溶于水
(4)根据整个反应过程中,质量减轻是因为生成了CO2气体,所以称量出反应前后装置的质量差值即为CO2的质量,再根据C原子守恒可以求出Na2CO3的物质的量从而求出质量及质量分数,所以还需测定的另两个数据是:反应前装有药品的整个装置的质量,反应后整个装置的质量。
(5)实验关键是计算出Na2CO3的质量,可以把它转变成气体,也可以转变成沉淀,通过称量
沉淀的量计算Na2CO3的质量,具体步骤是:称量一定质量的样品配成溶液,加入足量的BaCl2
溶液后得到沉淀,将沉淀进行过滤、洗涤、干燥、冷却、称量。由沉淀(BaCO3)质量计算出Na2CO3
的质量,最后计算出Na2CO3的质量分数。


 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案科目:高中化学 来源: 题型:
【题目】两种有机物A和B可以互溶,有关性质如下:
相对密度(20℃) | 熔点 | 沸点 | 溶解性 | |
A | 0.7893 | -117.3℃ | 78.5℃ | 与水以任意比混溶 |
B | 0.7137 | -116.6℃ | 34.5℃ | 不溶于水 |
(1)若要除去A和B的混合物中少量的B,可采用_______(填代号)方法即可得到A。
a.重结晶 b.蒸馏 c.萃取 d.加水充分振荡,分液
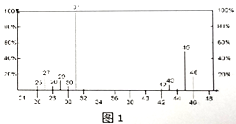
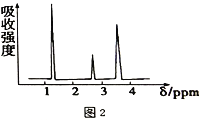
(2)将有机物A置于氧气流中充分燃烧,实验测得:生成5.4gH2O和8.8gCO2,消耗氧气6.72L(标准状况下),则该物质的最简式为_________,若要确定其分子式,是否必需有其它条件_______(填“是”或“否“),已知有机物A的质谱、核磁共振氢谱如图1所示,则A的结构简式为________。
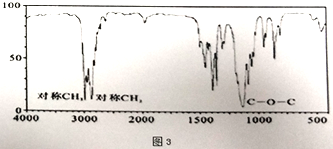
(3)若质谱图2显示B的相对分子质量为74,红外光谱如图3所示,则B的结构简式为_________,其官能团的名称为_________。
(4)准确称取一定质量的A和B的混合物,在足量氧气中充分燃烧,将产物依次通过足量的无水氯化钙和碱石灰,发现质量分别增重19.8g和35.2g.计算混合物中A和B的物质的量之比_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了充分利用铜资源,某工厂利用废旧黄铜灰(含有Cu、Zn、CuO、ZnO及少量的FeO、Fe2O3、SiO2等)制取金属铜并得副产物锌盐,其生产流程如下:
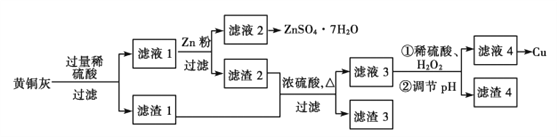
(1)滤渣1的主要成分为__________。稀硫酸溶解黄铜灰过程中,Cu是否参与了反应,如果参与请写出该反应的离子反应方程式,如果没反应请写出理由:_____________________。
(2)滤渣1及滤渣2与浓硫酸反应的步骤中存在缺陷,可将实验改进为先让滤渣与_______反应,产物再溶于稀硫酸,这样改进的优点是_____________________________________。
(3)写出滤液3与H2O2反应的离子反应方程式____________________________________,滤液3反应中需要调节PH的目的是______________________________________________。
(4)25 ℃时,沉淀Cu2+、Zn2+两种金属离子(M2+),所需S2-最低浓度的对数值lg c(S2-)与lg c(M2+)关系如下图所示。
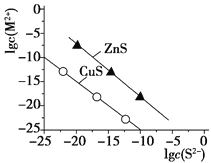
则Ksp(CuS)=_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环境监测测定水中溶解氧的方法是:
①量取a mL水样,迅速加入固定剂MnSO4溶液和碱性KI溶液(含KOH),立即塞好瓶塞,反复振荡,使之充分反应,其反应式为:2Mn2++O2+4OH-===2MnO(OH)2(该反应极快)。
②测定:开塞后迅速加入1~2 mL浓硫酸(酸化,提供H+),使之生成I2,再用b mol/L的Na2S2O3溶液滴定(以淀粉为指示剂),消耗V mL。有关反应式为:MnO(OH)2+2I-+4H+===Mn2++I2+3H2O、I2+2S2O![]() ===2I-+S4O
===2I-+S4O![]() 。
。
试回答:
(1)滴定过程中用到的玻璃仪器除了酸式滴定管、碱式滴定管外还缺少_____________。
(2)滴定操作时,左手控制滴定管,右手________,眼睛要注视________。
(3)水中溶解氧的计算式是______(以g/L为单位)。
(4)滴定(I2和S2O![]() 反应)以淀粉为指示剂,终点时溶液由________色变为________色,且半分钟内不褪色。
反应)以淀粉为指示剂,终点时溶液由________色变为________色,且半分钟内不褪色。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮氧化物是造成雾霾天气的主要原因之一,消除氮氧化物有多种方法。
(1)目前,应用最广泛的烟气氮氧化物脱除技术是NH3催化还原法,化学反应可表示为:
2NH3(g)+NO(g)+NO2(g)== 2N2(g)+3H2O(g) △H<0
①该反应中,反应物总能量_____(填“>”、“<”或“=”)生成物总能量。
②当该反应有2mol N2(g)生成时,转移电子的物质的量为__mol。
③该反应中,还原剂为______(填化学式),氧化产物与还原产物的质量比为______________。
(2)也可以利用甲烷催化还原氮氧化物.已知:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574kJ/mol
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867kJ/mol
则CH4(g)将NO(g)还原为N2(g)的热化学方程式是_________________。
(3)还可利用ClO2消除氮氧化物的污染,反应过程如下(部分反应物或生成物略去):![]()
反应I的产物中还有两种强酸生成,且其中一种强酸为硝酸,且硝酸与NO3物质的量相等,则化学反应方程式为______,反应中若生成22.4L N2(标准状况),则消耗ClO2______g。
(4)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。

①氢氧燃料电池的能量转化主要形式是________,工作时电流方向为________(用a、b和箭头表示)。
②负极的电极反应式为__________________。
③电极表面镀铂粉的原因为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O]又称摩尔盐。某兴趣小组制备硫酸亚铁铵的实验方案示意图如下:
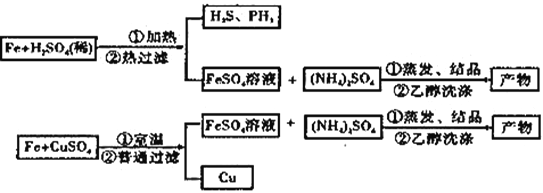
方案A(上图)方案B(下图)
已知:H2S、PH3为有毒气体,都能被CuSO4溶液吸收除去。
请回答下列问题:
(1)实验前都需进行将废铁屑放入碳酸钠溶液中煮沸,倾倒出液体,用水洗净铁屑的操作步骤。从以下仪器中选择组装,完成该操作必需的仪器有_________(填编号)。
①铁架台②玻璃棒③广口瓶④石棉网⑤烧杯⑥漏斗⑦酒精灯
(2)方案A中FeSO4溶液的制备:将处理好的铁屑放入锥形瓶,加入过量的3 mol·L-1H2SO4溶液,加热至充分反应为止。趁热过滤,收集滤液和洗涤液。下右图装置中方框内选择更适合用于实验方案A的装置是________(填“甲”或“乙”)。
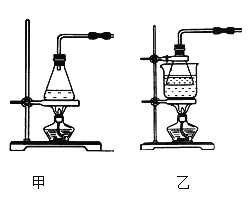
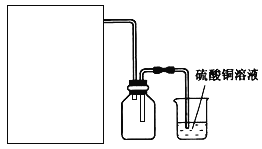
(3)方案A中废铁屑中含氧化铁,无需在制备前除去,理由是(用离子方程式回答)___________,用无水乙醇洗涤晶体的原因是___________________。
(4)实验方案B中FeSO4溶液的制备:用“五水硫酸铜结晶水的测定”实验中的废弃物——无水硫酸铜粉末代替稀硫酸与铁屑反应制备硫酸亚铁。当用无水硫酸铜配制的溶液由蓝色完全变为浅绿色时停止反应,过滤,收集滤液即得硫酸亚铁溶液。此方案的优点有_______________(填编号)。
a.充分利用了实验室废弃物——硫酸铜粉末,避免了药品浪费,又回收了金属铜,实现了变废为宝。
b.避免了有毒气体的排放对环境造成的污染。
c.原子利用率达到100%。
d.避免了在加热中Fe2+被氧化成Fe3+, 有利于产品质量等级的提高,并节约了能源。
(5)产品中Fe3+杂质的定量分析
①配制Fe3+浓度为1.0mg/mL的标准溶液100mL。称取_______mg高纯度的硫酸铁铵[(NH4)Fe(SO4)2·12H2O],加2.00 mL经处理的去离子水,振荡溶解后,加入2mol·L-1HBr溶液l m L和l mol·L-1KSCN溶液0.5 mL,加水制成100 mL溶液。配制过程中必须用到的定量仪器为____________(选填编号)。
a.精确度为0.001g的电子天平b.精确度为0.1mg的电子天平
c.100 mL容量瓶d.酸式滴定管e.10mL量筒
②将上述溶液稀释为浓度分别为0.2、1.0、3.0、5.0、7.0、10.0(单位:mg/L)的溶液。分别测定不同浓度溶液对光的吸收程度,并将测定结果绘制成曲线如下。
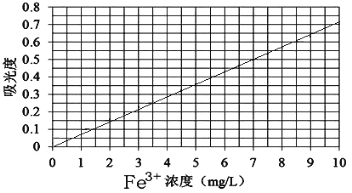
③取该兴趣小组所得的硫酸亚铁铵产品,按步骤①配得产品溶液10mL,稀释至100 mL,然后按步骤②的方法进行测定,两次测定所得的吸光度分别为0.490、0.510,则该兴趣小组所配产品硫酸亚铁铵溶液中所含Fe3+浓度为_________mg/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中,所选装置或实验设计合理的是
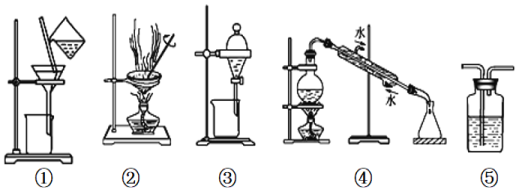
A. 用图①和②所示装置可以除去Na2CO3中的CaCO3杂质,并获得Na2CO3固体
B. 用乙醇提取溴水中的溴选择图③所示装置
C. 用图④所示装置可以分离乙醇水溶液
D. 图⑤所示装置中盛有饱和Na2CO3溶液除去CO2中含有的少量HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图1是铜锌原电池示意图。图2中,x轴表示实验时流入正极的电子的物质的量,y轴表示( )

A. 铜棒的质量 B. c(Zn2+) C. c(H+) D. c(SO42-) -
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盐酸普鲁卡因[H2N![]() COOCH2CH2N+H(C2H5)2·Cl-]是一种麻醉药,可由乙烯和苯合成。流程如下:
COOCH2CH2N+H(C2H5)2·Cl-]是一种麻醉药,可由乙烯和苯合成。流程如下:
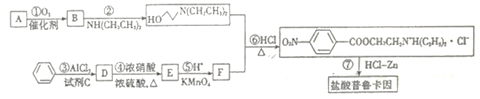
已知: I.B核磁共振氢谱只有1组峰; D的相对分子质量为92。
II.试剂C 是一氯代烃,与苯的反应为: ![]()
回答下列问题:
(1)F的结构简式为______________,它含有的官能团名称是_____________________。
(2)反应④的反应类型为______反应,其化学方程式:___________________________。
(3)反应③的化学方程式为______________________________________。
(4)E的既能发生银镜反应,又能遇FeCl3溶液显色且不含酰胺键的芳香族同分异构体有____种,任写其一种结构简式:________________________________。
(5)参照上述合成路线,设计由甲苯合成对氨基苯甲酸(H2N![]() COOH)的合成路线(其他无机试剂任选)_____________。
COOH)的合成路线(其他无机试剂任选)_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com