
【题目】为了充分利用铜资源,某工厂利用废旧黄铜灰(含有Cu、Zn、CuO、ZnO及少量的FeO、Fe2O3、SiO2等)制取金属铜并得副产物锌盐,其生产流程如下:
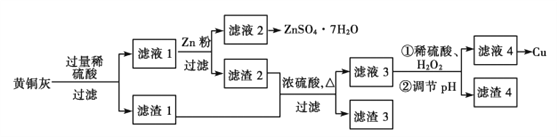
(1)滤渣1的主要成分为__________。稀硫酸溶解黄铜灰过程中,Cu是否参与了反应,如果参与请写出该反应的离子反应方程式,如果没反应请写出理由:_____________________。
(2)滤渣1及滤渣2与浓硫酸反应的步骤中存在缺陷,可将实验改进为先让滤渣与_______反应,产物再溶于稀硫酸,这样改进的优点是_____________________________________。
(3)写出滤液3与H2O2反应的离子反应方程式____________________________________,滤液3反应中需要调节PH的目的是______________________________________________。
(4)25 ℃时,沉淀Cu2+、Zn2+两种金属离子(M2+),所需S2-最低浓度的对数值lg c(S2-)与lg c(M2+)关系如下图所示。
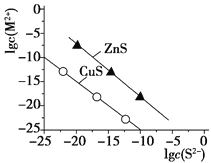
则Ksp(CuS)=_____________________。
【答案】 Cu和SiO2 Cu+2Fe3+=2Fe2++Cu2+ O2 滤渣1及滤渣2用浓硫酸浸取可能产生的有毒气体是SO2污染环境,同时减少了硫酸的用量(其它合理答案均可得分) 2Fe2++H2O2+2H+=2Fe3++2H2O 调节pH,使Fe3+转化为氢氧化铁沉淀除去 1×10-35
【解析】(1)黄铜灰中不与稀硫酸反应的物质是Cu和二氧化硅,所以加入稀硫酸过滤后的滤渣1的主要成分是单质铜和二氧化硅。黄铜灰中有氧化铁,与稀硫酸反应得到Fe3+,单质铜可以与其反应,方程式为:Cu+2Fe3+=2Fe2++Cu2+。注意:因为氧化铁为少量,所以最后一定剩余单质铜,滤渣1中应该有单质铜。
(2)滤渣2主要含单质铜和铁,滤渣1主要含单质铜和二氧化硅,加入浓硫酸反应,将单质铁和铜转化为盐溶液,滤渣3为二氧化硅。此步反应中的最大问题是,生成二氧化硫这样的污染性气体,所以应该先加入氧气氧化,将金属单质氧化为金属氧化物,再与稀硫酸反应。同时这样的操作可以减少硫酸的用量(因为用浓硫酸时,一部分硫酸转化为二氧化硫,而使用稀硫酸时,所有的硫酸都转化为硫酸盐)。
(3)在滤液3中加入硫酸和过氧化氢的目的是为了将Fe2+氧化为Fe3+,所以方程式为:2Fe2++H2O2+2H+=2Fe3++2H2O。滤液3氧化以后,溶液中主要是Cu2+和Fe3+,调节pH的目的是将Fe3+转化为氢氧化铁沉淀,以将两种金属阳离子分离。
(4)从图中得到:横坐标为-10的时候纵坐标的数值为-25,即c(S2-)=1×10-10mol/L的时候,c(Cu2+)=1×10-25mol/L,所以CuS的Ksp=1×10-35。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】图是一种分子式为C4H8O2的有机物的红外光谱图,则该有机物可能为( )
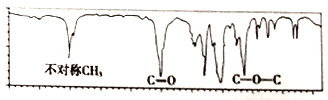
A. HCOOCH2CH2CH3 B. CH3CH2COOH
C. CH3COOCH2CH3 D. (CH3)2CHCH2COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项中的物质,能满足如图中阴影部分关系的
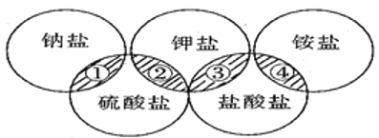
选项 | ① | ② | ③ | ④ |
A | NaCl | K2SO4 | KCl | (NH4)2SO4 |
B | NaCl | K2SO4 | KCl | NH4Cl |
C | Na2SO4 | K2SO4 | KCl | NH4Cl |
D | Na2SO4 | K2SO4 | KCl | (NH4)2SO4 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离方程式书写正确的是
A. NaHCO3![]() Na+ + HCO3-
Na+ + HCO3-
B. CaCO3 = Ca2+ + CO32-
C. Cu(NO3)2 = Cu2+ + (NO3-)2
D. HClO = H+ + ClO-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下,在溶液中可发生以下两个反应:①Cl2 + 2Br- = Br2 + 2Cl-;②Br2 + 2Fe2+ = 2Fe3+ + 2Br-。现将标准状况下 1.12L 的氯气通入 1L 0.05mol/L 的 FeBr2溶液中,由此判断下列说法正确的是
A. 氧化性强弱:Cl2 > Fe3+ > Br2 B. 还原性强弱:Br- >Fe2+ >Cl-
C. 反应后溶液中 c(Fe3+):c(Br- ) =1:1 D. 反应后溶液中 c(Fe2+):c(Cl-) =1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质属于常见氧化剂的一组是( )
A.Cl2、O2、FeCl3、KMnO4
B.O2、KMnO4、C,H2
C.Na、K、FeCl2、H2、CO
D.CuO、CO、Fe2O3、H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(12分) 为测定NaOH、Na2C03混合物中Na2C03的质量分数,甲同学拟采用图(1)
所示装置来测定。乙同学拟采用图(2)所示装置来测定。
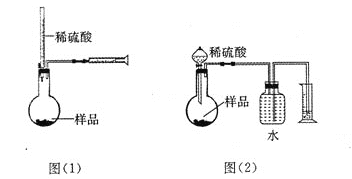
请回答下列问题:
(1)甲同学用图(1)装置来测定,在没有放样品前,检查该装置气密性的方法之一是从酸式滴定管向烧瓶中加入一定量的水,观察到 现象,证明此装量不漏气。实验时称得样品的质量为mg,酸式滴定管的起始读数为amL,终了读数为bmL,注射器测定排出的气体为c mL(已折算成标准状况),该样品中Na2C03的质量分数为(用含a、b、c、m的代数式表示)____ 。
(2)本实验选用稀H2S04而未选用稀盐酸的原因是 。
(3)乙同学观察了甲同学的实验后很受启发,并发现自己的图(2)原实验设计方案会造成误差.其原因之一可能是C02在水中溶解度较大,引起测量气体体积减小。
丙同学经思考后。建议乙同学将图(2)中某部分稍作改进,就可避免此种误差,写出你的改进方案 。
(4)丁同学提出将图(2)装置中量气装置去掉,只用反应装置和天平也能较准确地测出样品中Na2C03的质量分数,请你分析丁同学方案中,除了测定样品的质量,还需测定的另两个数据是 、 。
(5)还可以用其他实验方法测定试样中纯碱的质量分数,请简述一种与上述各方法不同的实验方法 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.淀粉和纤维素水解最终产物都是葡萄糖B.油脂水解可得到氨基酸和甘油
C.蛋白质水解的最终产物是多肽D.蔗糖在人体内水解产物只有葡萄糖
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com