
����Ŀ����ͼ��A����ȡ�屽��ʵ��װ�ã�B��C�ǸĽ����װ�ã�����ϸ�������Ա�����װ�ã��ش��������⣺
A.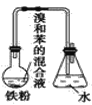 B.
B. 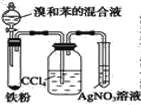 C.
C. 
(1)д������װ��������ͬ��������Ҫ��Ӧ�Ļ�ѧ����ʽ��__________________��������ķ�Ӧ�ķ�Ӧ����Ϊ________________
(2)װ�� A �� C �������˳��������ܣ���������______________��
(3)�ڰ�װ�� B װ��������ҩƷ��Ҫʹ��Ӧ��ʼ��Ӧ��װ�� B ���еIJ�����_____________������ʽΪ C8H10�����ڱ���ͬϵ��Ľṹ��_______________�֡�
(4)װ�� B��C �Ϻõؽ���� A �м�װҩƷ��ʹװ�ü�ʱ�ܷ��ì�ܣ������˲�����A װ������һ������ʵ������ɵĺ����______________��
(5)B �в�����ϴ��ƿ����װ�ã���������_______________����Ӧ��ϴ��ƿ�п��ܳ��ֵ�������_________________��
(6)B װ��Ҳ�����������Ե�ȱ�㣬ʹʵ���Ч�����û����������С�������ȱ����_________��
���𰸡�2Fe + 3Br2 = 2FcBr3��![]() ȡ����Ӧ ����HBr���������������� B��������Һ©���Ļ�����ʹ��ͱ��Ļ��Һ���������� 4 ��ͱ������ݳ�����Ⱦ���� ���շ�Ӧ����HBr�ݳ����������ͱ����� CCl4����ɫ��Ϊ��ɫ ����HBr�ݳ����������ͱ��������ܻ�������Ӧ���У�ԭ�������ʵͣ������ڵ��ܲ���AgNO3��Һ�ж��ײ�������
ȡ����Ӧ ����HBr���������������� B��������Һ©���Ļ�����ʹ��ͱ��Ļ��Һ���������� 4 ��ͱ������ݳ�����Ⱦ���� ���շ�Ӧ����HBr�ݳ����������ͱ����� CCl4����ɫ��Ϊ��ɫ ����HBr�ݳ����������ͱ��������ܻ�������Ӧ���У�ԭ�������ʵͣ������ڵ��ܲ���AgNO3��Һ�ж��ײ�������
��������
(1)A��B��C����װ�ö�����ȡ�屽,���ᷢ��������ķ�Ӧ���������ȡ����Ӧ��
(2)�������ӷ����������ܵ����������������ã�
(3)������ͱ��Ļ��Һ�����ۻ�ϲ��ܷ�����Ӧ������ʽΪ C8H10�����ڱ���ͬϵ��Ϊ�뱽���2��-CH2���ҽṹ���ƣ��ݴ��жϸ�����
(4) ����Br2�ͱ������ӷ�������Aװ�ò��ܼ�ʱ���ܷ⣬���Ի���ɱ����������ݳ�����Ⱦ�������ݴ˻ش�
(5) B��ϴ��ƿ��װ��CCl4�л��ܼ������������ձ���������������������CCl4���ʳ�ɫ������CCl4��Һ������ɫ��Ϊ��ɫ��
(6)��ԭ�������ʺ�ʵ�鰲ȫ�Ƕ�˼�������⡣
(1)����װ�þ����屽���Ʊ�װ�ã����Ʊ�ԭ��Ϊ��������Ӧ���廯��������Һ�����廯���Ĵ��������屽���廯�⣬��Ӧ�Ļ�ѧ����ʽΪ2Fe + 3Br2 = 2FcBr3��![]() �����б�������ķ�ӦΪȡ����Ӧ���ʴ�Ϊ��2Fe + 3Br2 = 2FcBr3��
�����б�������ķ�ӦΪȡ����Ӧ���ʴ�Ϊ��2Fe + 3Br2 = 2FcBr3��![]() ��ȡ����Ӧ��
��ȡ����Ӧ��
(2) A��C�г����ܵ������ǽ���Ӧ���ɵ�HBr���嵼��ˮ�У����ڸ÷�Ӧ���ȣ����Գ�����Ҳ�������������ã��ʴ�Ϊ������HBr���������������ã�
(3)װ��B���Կ��Ʒ�Ӧ�ķ�����ֹͣ��Bװ��ͨ����Һ©�����ƣ�������Һ©��������ʱ����Ӧ��ʼ������ʽΪ C8H10�����ڱ���ͬϵ��Ľṹ�У��Զ��ױ����ڶ��ױ�������ױ���������4�֣��ʴ�Ϊ��B��������Һ©���Ļ�����ʹ��ͱ��Ļ��Һ���������ϣ�4��
(4)����Br2�ͱ������ӷ�������Aװ�ò��ܼ�ʱ���ܷ⣬���Ի���ɱ����������ݳ�����Ⱦ�������ʴ�Ϊ����ͱ������ݳ�����Ⱦ������
(5)B��ϴ��ƿ��װ��CCl4�л��ܼ������������ձ���������������������CCl4���ʳ�ɫ������CCl4��Һ������ɫ��Ϊ��ɫ���ʴ�Ϊ�����շ�Ӧ����HBr�ݳ����������ͱ�������CCl4����ɫ��Ϊ��ɫ��
(6)Bװ���д��ڵ���Ҫ����������ڱ��������������Ļӷ��Ҳ��ܻ������Ӷ�����ԭ���ϵ��˷ѣ������ʽ��ͣ������ֱ�Ӳ���AgNO3��Һ�У�����ӦͻȻֹͣ��������ѹǿͻȻ���ͣ����������������ʴ�Ϊ������HBr�ݳ����������ͱ��������ܻ�������Ӧ���У�ԭ�������ʵͣ������ڵ��ܲ���AgNO3��Һ�ж��ײ���������


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ��ɹ����Ƴ�һ��ȫ�µ���-ʯī˫���ӵ��(AGDIB)����������AGDIB��ز����������õ�ʯī��������Ϊ�缫���ϣ��Գ�����κ�̼�����ܼ�Ϊ���Һ���õ�ع���ԭ���ǣ��������У�ʯī���������Ӳ�㷴Ӧ�������缫������-﮺Ͻ�Ӧ���ŵ�������෴����ط�ӦʽΪCxPF6+ LiyAl![]() Cx+LiPF6+ Liy-1Al������˵������ȷ����
Cx+LiPF6+ Liy-1Al������˵������ȷ����
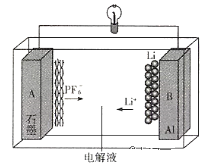
A.�����ǵ�ظ���
B.���ʱ�����缫��������﮺Ͻ�Ӧ�ǻ�ԭ��Ӧ
C.���ʱA���������ŵ�ʱA�缫�ĵ缫��ӦʽΪCxPF6+e-=Cx+![]()
D.�Ͼ�AGDIB��ؽ������ŵ紦��������Li+����ʯī�ж������ڻ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NOx Ϊ��Ҫ�ɷֵ��������ۺ������ǵ�ǰ��Ҫ���о����⡣
I.����β���е� NO(g)�� CO(g)��һ�������¿ɷ�����Ӧ��������N2 �� CO2��
��1����֪:��N2(g)+O2(g)![]() 2NO(g) ��H1= +180.5 kJ��mol-1 ��CO ��ȼ���ȡ�H2 = - 283.0 kJ��mol-l����Ӧ�� 2NO(g)+2CO(g)
2NO(g) ��H1= +180.5 kJ��mol-1 ��CO ��ȼ���ȡ�H2 = - 283.0 kJ��mol-l����Ӧ�� 2NO(g)+2CO(g)![]() N2(g)+2CO2(g) ��H3 =_______��
N2(g)+2CO2(g) ��H3 =_______��
��2��ij�о�С���������ݻ�Ϊ 5 L �ĺ����ܱ������У��ֱ���� 0.4mol NO �� 0.4 mol CO��������Ӧ�� �������ֲ�ͬʵ�������½���������Ӧ����ϵ���Ա����¶Ȳ��䣩����Ӧ��ϵ��ѹǿ��ʱ��ı仯��ͼ��ʾ��
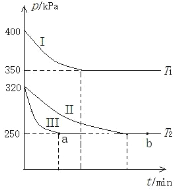
���¶ȣ�T1_____T2���������=����������
��CO ��ƽ��ת���ʣ���_____��_____���������=����������
�۷�Ӧ���ʣ�a ��� v��_____b ��� v�� ���������=����������
��T2 ʱ��ƽ�ⳣ�� Kc=_____��
��3���� NO�� CO��һ��������ͨ�����ֲ�ͬ�Ĵ�����cat1��cat2�����з�Ӧ����ͬʱ���ڲ������ѵ��ʣ��ѵ��ʼ� NO��ת���ʣ���ͼ��ʾ��M ��_____����ǡ����ǡ�����Ӧ�¶��µ�ƽ���ѵ��ʣ� ˵������_________��
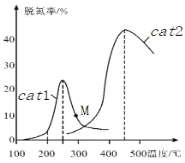
��N2O��һ��ǿ�������壬�����γɿ�������Ⱦ��о�N2O�ķֽⷴӦ 2N2O=2N2+O2�Ի�����������Ҫ���塣
��4�������������ܴ������� N2O �ķֽ����ʣ���Ӧ����Ϊ��
��һ�� I2(g)![]() 2I(g)����ƽ�⣬ƽ�ⳣ��ΪK
2I(g)����ƽ�⣬ƽ�ⳣ��ΪK
�ڶ��� I(g)+N2O(g)��N2(g)+IO(g) v = k1��c(N2O)��c(I) ����Ӧ
������ IO(g)+N2O(g)��N2(g)+O2(g)+1/2I2(g) �췴Ӧ
���пɽ�����Ϊ�ڶ�����Ӧ��Ӱ���һ����ƽ�⡣ʵ�����������ʱN2O�ֽ����ʷ���v=k��c(N2O)��[c(I2)]0.5��kΪ���ʳ�������
�� k =_____���ú� K �� k1 �Ĵ���ʽ��ʾ����
�����б�����ȷ����_____��
a��IO Ϊ��Ӧ���м����
b����������Ũ�ȴ�С����Ӱ�� N2O�ķֽ�����
c���ڶ������ܷ�Ӧ�������������
d�������ή�ͷ�Ӧ�Ļ�ܣ��Ӷ�Ӱ���H
��5��ͨ�� N2O �������ɼ����� N2O �ĺ������乤��ԭ����ͼ��ʾ
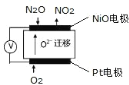
��NiO�缫�ϵĵ缫��ӦʽΪ_____��
��N2OŨ��Խ�ߣ����ѹ������Խ_____������ߡ��͡���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��As2O3(��˪)������������(���ӽṹ��ͼ��ʾ)�������������� AsCl3��AsCl3�� LiAlH4��ԭ���� AlH3������˵����ȷ����( )
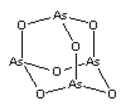
A.As2O3 ������ As ԭ�ӵ��ӻ���ʽΪ sp
B.LiAlH4Ϊ���ۻ�����
C.AsCl3�ռ乹��Ϊƽ����������
D.AlH3���Ӽ��Ǵ��� 109.5��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ȳ��һ����Ҫ���л�����ԭ�ϣ�����ȲΪԭ���ڲ�ͬ�ķ�Ӧ�����¿���ת�������»����
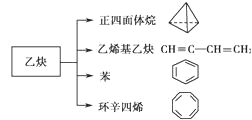
����˵����ȷ����( )
A.1mol��ϩ����Ȳ���� 3mol Br2�����ӳɷ�Ӧ
B.�������������ȡ������ֻ��1��
C.������ϩ�˴Ź���������2���
D.������ϩ�뱽��Ϊͬϵ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ���о��л���A�������ṹ��ijͬѧ��������ʵ�顣
i.��9.0gA �����������г��ȼ�գ���ʹ��������λ���ͨ��������Ũ����ͼ�ʯ��,�������߷ֱ�����5.4g��13.2g��
ii.ͨ�������������Է�������Ϊ90��
ili.ͨ������������A�к��С�OH�͡�COOH��
��ش��������⡣
��1��9.0gA��ȫȼ������ˮ�����ʵ�����____________mol��
��2��A��ʵ��ʽ��____________��
��3��A�ķ���ʽ��____________��
��4����һ�������£�������A���ӿ��Է�Ӧ�õ�һ����Ԫ���ķ��ӣ���A�Ľṹ��ʽ��____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ƿdz���Ҫ�Ĺ�ҵԭ�ϣ����ȴ����������������ڴ������������Ʊ���ʵ����ģ�ҵ����ʳƷ�㾫������(![]() ) �ļ����������¡�
) �ļ����������¡�
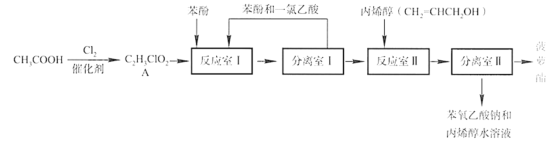
��1���������ĺ˴Ź�����������__________�����շ塣
��2��A�й����ŵ�������__________��
��3����������д�����з�Ӧ�Ļ�ѧ����ʽ:
i.�Ʊ�A: __________���÷�Ӧ����__________��Ӧ��
ii.��Ӧ��I�еķ�Ӧ: __________��
��4��������II�IJ������ñ���Na2CO3��Һϴ�ӣ�������NaOHϴ�ӵ�ԭ����__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����( )
A.NH3 �Ǽ��Է��ӣ������� N ԭ�Ӵ��� 3 �� H ԭ������ɵ������ε�����
B.����������ˮ��ԭ��֮һ�ǰ���������ˮ����֮�����γ����
C.�Ҵ�������ˮ����֮��ֻ���ڷ��»���
D.�ȵĸ��ֺ������������ǿ����������˳��ΪHClO>HClO2>HClO3>HClO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���û�ѧ����������������ȷ���ǣ� ��
A.��KI-������Һ�еμ�ϡ���ᣬ��Һ����ɫ��4I����O2��2H2O=2I2��4OH��
B.�����£�0.1 mol/L��HF ��Һ��pH>1��HF��H2O![]() H3O+��F��
H3O+��F��
C.KHSO4������״̬�¿ɵ��磺KHSO4 = K+��H+��SO42��
D.BaSO4��ˮ��Һ�����Լ�����BaSO4![]() Ba2+��SO42��
Ba2+��SO42��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com