
【题目】Na、Al、Fe都是重要的金属元素。下列说法正确的是
A.氧化物都是碱性氧化物
B.氢氧化物都是白色固体
C.单质都可以与水反应
D.单质在空气中都形成致密氧化膜
【答案】C
【解析】
A.Na、Al、Fe的氧化物中,过氧化钠能跟酸起反应,除生成盐和水外,还生成氧气,不是碱性氧化物,氧化铝不但可以和碱反应还可以和酸反应均生成盐和水,为两性氧化物,故A错误;
B.氢氧化钠、氢氧化铝为白色固体,而氢氧化铁为红褐色固体,故B错误;
C.钠与水反应2Na+2H2O=2NaOH+H2↑,生成氢氧化钠和氢气,铁与水蒸汽反应生成氢气与四氧化三铁,3Fe+4H2O(g)![]() Fe3O4+4H2,在金属活动性顺序表中,铝介于二者之间,铝和水2Al+6H2O
Fe3O4+4H2,在金属活动性顺序表中,铝介于二者之间,铝和水2Al+6H2O![]() 2Al(OH)3+3H2↑,反应生成氢氧化铝和氢气,高温下氢氧化铝分解阻碍反应进一步进行,但铝能与水反应,故C正确;
2Al(OH)3+3H2↑,反应生成氢氧化铝和氢气,高温下氢氧化铝分解阻碍反应进一步进行,但铝能与水反应,故C正确;
D.Na在空气中最终生成碳酸钠,不是形成致密氧化膜,Al在空气中与氧气在铝的表面生成一层致密的氧化物保护膜,阻止Al与氧气的进一步反应,铁在空气中生成三氧化二铁,不是形成致密氧化膜,故D错误;
故答案为C。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】苯甲酸乙酯可由苯甲酸与乙醇在浓硫酸共热下反应制得,反应装置如图(部分装置省略),反应原理如下:
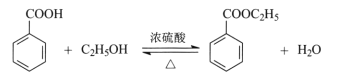
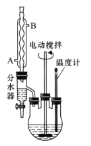
实验操作步骤:
①向三颈烧瓶内加入12.2g苯甲酸、25mL乙醇、20mL苯及4mL浓硫酸,摇匀,加入沸石。
②装上分水器、电动搅拌器和温度计,加热至分水器下层液体接近支管时将下层液体放入量筒中。继续蒸馏,蒸出过量的乙醇,至瓶内有白烟(约3h),停止加热。
③将反应液倒入盛有80mL冷水的烧杯中,在搅拌下分批加入碳酸钠粉末至溶液无二氧化碳逸出,用pH试纸检验至呈中性。
④用分液漏斗分出有机层,水层用25mL乙醚萃取,然后合并至有机层。用无水CaC12干燥,粗产物进行蒸馏,低温蒸出乙醚。当温度超过140℃时,直接接收210-213℃的馏分,最终通过蒸馏得到纯净苯甲酸乙酯12.8mL。
可能用到的有关数据如下:
相对分子质量 | 密度(g/cm3) | 沸点/℃ | 溶解性 | |
苯甲酸 | 122 | 1.27 | 249 | 微溶于水,易溶于乙醇、乙醚 |
苯甲酸乙酯 | 150 | 1.05 | 211-213 | 微溶于热水,溶于乙醇、乙醚 |
乙醇 | 46 | 0.79 | 78.5 | 易溶于水 |
乙醚 | 74 | 0.73 | 34.5 | 微溶于水 |
回答以下问题:
(1)反应装置中分水器上方的仪器名称是______,其作用是____
(2)步骤①中加浓硫酸的作用是_________,加沸石的目的是______。
(3)步骤②中使用分水器除水的目的是_________。
(4)步骤③中加入碳酸钠的目的是________ 。
(5)步骤④中有机层从分液漏斗的____(选填“上口倒出”或“下口放出”)。
(6)本实验所得到的苯甲酸乙酯产率是________%。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若某氖原子质量是a g,12C的原子质量是b g,NA是阿伏加德罗常数的值,下列说法正确的是
A.氖元素的相对原子质量一定是![]()
B.该氖原子的摩尔质量是aNAg
C.Wg该氖原子的物质的量一定是![]() mol
mol
D.Wg该氖原子所含质子数是![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验:
①向Fe2(SO4)3和CuSO4的混合液中加入过量铁粉,充分反应,有红色固体析出,过滤。
②取①中滤液,向其中滴加KSCN溶液,观察现象。
判断下列说法正确的是
A. 氧化性Cu2+>Fe3+
B. ①中所得固体只含铜
C. ①中滤液含有Cu2+和Fe2+
D. ②中不会观察到溶液变红
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组以Mg(NO3)2为研究对象,拟通过实验初步探究硝酸盐热分解的规律。
(提出猜想)小组提出如下4种猜想:
甲:Mg(NO2)2、NO2、O2 乙:MgO、NO2、O2
丙:Mg3N2、O2 丁:MgO、NO2、N2
(1)查阅资料得知,NO2可被NaOH溶液吸收,反应的化学方程式为:_________。
(2)实验前,小组成员经讨论认定猜想丁不成立,理由是________。
(实验操作)
(3)设计如图装置,用氮气排尽装置中空气,其目的是_______;加热Mg(NO3)2固体,AB装置实验现象是:________,说明有Mg(NO3)2固体分解了,有NO2生成。

(4)有同学提出可用亚硫酸钠溶液检验是否有氧气产生,但通入之前,还需在BD装置间增加滴有酚酞的氢氧化钠溶液,其作用是:_______。
(5)小组讨论后认为即便通过C后有氧气,仅仅用亚硫酸钠溶液仍然难以检验,因为:______,改进的措施是可在亚硫酸钠溶液中加入_______。
(6)上述系列改进后,如果分解产物中有O2存在,排除装置与操作的原因,未检测到的原因是______。(用化学方程式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2(g)+2ICl(g)![]() I2(g)+2HCl(g),该反应分①、②两步进行,其能量曲线如图所示,
I2(g)+2HCl(g),该反应分①、②两步进行,其能量曲线如图所示,
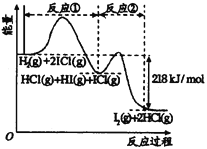
下列有关说法正确的是
A. 反应①为吸热反应
B. 反应①和②均是同种元素间发生的氧化还原反应
C. 反应①比反应②的速率慢,与相应正反应的活化能有关
D. HI(g)+ICl(g) ![]() I2(g)+HCl(g) △H=-218 kJ/mol
I2(g)+HCl(g) △H=-218 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以乙烯与甲苯为主要原料,按下列路线合成一种香料W:

(1)实验室制备乙烯的反应试剂与具体反应条件为____。
(2)上述①~④反应中,属于取代反应的是___。
(3)检验反应③是否发生的方法是____。
(4)写出两种满足下列条件的![]() 同分异构体的结构简式。____、____。
同分异构体的结构简式。____、____。
a.能发生银镜反应 b.苯环上的一溴代物有两种
(5)设计一条由乙烯制备A的合成路线。(无机试剂可以任选)____。
(合成路线常用的表示方式为: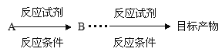 )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次氯酸溶液是常用的消毒剂、漂白剂。某学习小组根据需要欲制备浓度不小于0.8mol/L的次氯酸溶液。
(查阅资料)
资料1:常温常压下,Cl2O为棕黄色气体,沸点为 3.8 ℃,42 ℃以上会分解生成 Cl2和O2, Cl2O易溶于水并与水立即反应生成 HClO。
资料2:将氯气和空气(不参与反应)按体积比 1∶3 混合通入潮湿的碳酸钠中发生反应2Cl2+2Na2CO3+H2O![]() Cl2O+2NaCl+2NaHCO3,用水吸收 Cl2O(不含Cl2)制得次氯酸溶液。
Cl2O+2NaCl+2NaHCO3,用水吸收 Cl2O(不含Cl2)制得次氯酸溶液。
(装置及实验)用以下装置制备次氯酸溶液

回答下列问题:
(1)各装置的连接顺序为_____→_____→_____→____→E。
(2)装置 A 中反应的离子方程式是______。
(3)装置 E中反应的化学方程式是_____。
(4)装置 B 中多孔球泡和搅拌棒的作用是_______;反应过程中,装置B需放在冷水中,其目的是_____。
(5)装置 C 的主要作用是_____。
(6)此方法相对于用氯气直接溶于水制备次氯酸溶液的优点是(答出一条即可)_____。
(7)若装置B中生成的Cl2O气体有20%滞留在E前各装置中,其余均溶于装置E的水中,装置E所得500mL次氯酸溶液浓度为0.8mol/L,则至少需要含水8%的碳酸钠的质量为___g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙炔在不同条件下可以转化成许多化合物,如图,下列叙述错误的是( )
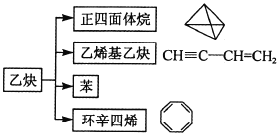
A. 正四面体烷的一氯代物及二氯代物均只有1种
B. 乙炔生成乙烯基乙炔是加成反应
C. ![]() 与环辛四烯(C8H8)互为同分异构体
与环辛四烯(C8H8)互为同分异构体
D. 等质量的苯与乙烯基乙炔完全燃烧时的耗氧量不同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com