
设NA表示阿伏加德罗常数的值,下列说法正确的是
A.1mol OH含有的电子数目为9NA
B.1mol Cl2和氢氧化钠完全反应,转移的电子数目为NA
C.室温下,1L pH=1的H2SO4溶液中,由水电离出的H+数目为0.1NA
D.1mol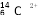 所含中子数目为6NA
所含中子数目为6NA
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源:2014-2015学年湖南省怀化市高三第一次模拟考试理综化学试卷(解析版) 题型:填空题
【化学——选修3:物质结构与性质】(15分)
目前半导体生产展开了一场“铜芯片”革命——在硅芯片上用铜代替铝布线,古老的金属铜在现代科技应用上取得了突破,用黄铜矿(主要成分为CuFeS2)生产粗铜,其反应原理如下:

(1)基态铜原子的外围电子层排布为__________________,硫、氧元素相比,第一电离能较大的元素是________(填元素符号)。
(2)反应①、②中均生成有相同的气体分子,该分子的中心原子杂化类型是________,其立体结构是______________。
(3)某学生用硫酸铜溶液与氨水做了一组实验:CuSO4溶液 蓝色沉淀
蓝色沉淀 沉淀溶解,得到深蓝色透明溶液。写出蓝色沉淀溶于氨水的离子方程式_______________________;深蓝色透明溶液中的阳离子内存在的化学键类型有 。
沉淀溶解,得到深蓝色透明溶液。写出蓝色沉淀溶于氨水的离子方程式_______________________;深蓝色透明溶液中的阳离子内存在的化学键类型有 。
(4)铜是第四周期最重要的过渡元素之一,其单质及化合物具有广泛用途,铜晶体中铜原子堆积模型为_____________;铜的某种氧化物晶胞结构如图所示,若该晶体的密度为d g/cm3,阿伏加德罗常数的值为NA,则该晶胞中铜原子与氧原子之间的距离为________cm。((用含d和NA的式子表示)。

查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省泉州市高三3月月考理综化学试卷(解析版) 题型:选择题
某研究小组测定不同温度下、不同初始浓度的某溶液中R的水解速率,c(R)随时间的变化曲线如图。下列说法不正确的是

A.在0-6min之间,25℃时R的水解速率为0.05 mol·L—1·min—1
B.在0-24min之间,曲线3对应水解速率最小
C.由曲线1可以得出结论:其它条件不变,水解速率随浓度增大而增大
D.由曲线2、3可以得出结论:其它条件不变,水解速率随温度升高而增大
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省福州市高三3月月考理综化学试卷(解析版) 题型:选择题
下列关于乙酸说法错误的是
A.乙酸与甲酸甲酯(HCOOCH3)互为同分异构体
B.乙酸与乙醇都能与Na反应,生产H2
C.加入生石灰再蒸馏可以除去冰醋酸中少量的水
D.饱和Na2CO3溶液可除去乙酸乙酯中少量的乙酸
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市石景山区高三上学期期末考试化学试卷(解析版) 题型:选择题
利用下图装置进行实验(必要时可加热),不能得出相应结论的是
溶液① | 固体② | 溶液③ | 实验结论 |
| |
A | 稀硫酸 | Na2CO3 | Na2SiO3 | 非金属性:C>Si | |
B | 浓盐酸 | MnO2 | Na2S | 氧化性:Cl2>S | |
C | 盐酸 | CaCO3 | C6H5ONa | 酸性:碳酸>苯酚 | |
D | 稀硫酸 | Na2CO3 | CaCl2 | CO2不与氯化钙反应 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市石景山区高三上学期期末考试化学试卷(解析版) 题型:选择题
下列比较中,正确的是
A.原子半径:Na>Mg B.碱性:NaOH>KOH
C.结合H+的能力:CO32<Cl D.还原性:I<Br
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省商丘市高三第一次模拟考试化学试卷(解析版) 题型:实验题
(8分)三草酸合铁酸钾晶体易溶于水,难溶于乙醇,可用作某些化学反应的催化剂,化学式为K3[Fe(C2O4)3]·3H2O。实验室以铁屑为原料制备三草酸合铁酸钾晶体相关反应过程如图所示:

请回答下列问题:
(1)制备过程中加入H2O2目的是______________,得到K3[Fe(C2O4)3]溶液后,需要加入乙醇,其目的是_________________。
(2)晶体中所含的结晶水可通过重量分析法测定,主要步骤有:①称量,②置于烘箱中脱结晶水,③冷却,④称量,⑤重复脱水、冷却、称量至恒重,⑥计算。步骤⑤的目的是___________________。
(3) 可被高锰酸钾溶液氧化放出CO2,测定产物中K3[Fe(C2O4)3]·3H2O含量时,可用酸性高锰酸钾标准溶液进行滴定。
可被高锰酸钾溶液氧化放出CO2,测定产物中K3[Fe(C2O4)3]·3H2O含量时,可用酸性高锰酸钾标准溶液进行滴定。
①写出滴定过程中发生反应的离子方程式_____________;
②取10.0g产物配成100mL溶液,从中取出20mL于锥形瓶中,用0.1mol·L-1的酸性高锰酸钾溶液进行滴定,达到滴定终点时消耗酸性高锰酸钾溶液24mL。则产物中K3[Fe(C2O4)3]·3H2O的质量分数为_________。(K3[Fe(C2O4)3]·3H2O相对分子质量为491)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省商丘市高三第一次模拟考试化学试卷(解析版) 题型:选择题
下列离子方程式正确的是
A.0.01mol NH4Al(SO4)2溶液与0.01mol·L-1Ba(OH)2溶液等体积混合 +Al3++2
+Al3++2 +2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3·H2O
+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3·H2O
B.Na2S2O3溶液中加入稀硫酸: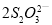 +4H+=
+4H+= +3S↓+2H2O
+3S↓+2H2O
C.将标准状况下的11.2L氯气通入200mL2mol·L-1的FeBr2溶液中,离子反应方程式为:4Fe2++6Br-+5Cl2=4Fe3++3Br2+10Cl-
D.铁粉中滴加少量浓硝酸:Fe+3 +6H+=Fe3++3NO2↑+3H2O
+6H+=Fe3++3NO2↑+3H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省菏泽市高三第一次模拟考试理科综合化学试卷(解析版) 题型:选择题
原子结构决定元素的性质,下列说法中,正确的是
A.Na、Al、Cl的原子半径依次减小,Na+、Al3+、Cl-的离子半径也依次减小
B.在第VIA族元素的氢化物(H2R)中,热稳定性最强的其沸点也最高
C.第2周期元素的最高正化合价都等于其原子的最外层电子数
D.非金属元素的非金属性越强,其氧化物对应水化物的酸性也一定越强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com