
| A. | 石炭酸与NaOH溶液混合:H++OH-→H2O | |
| B. | 稀HNO3洗涤试管中的银镜:Ag+NO3-+2H+═Ag++NO↑+H2O | |
| C. | 乙烯使酸性KMnO4褪色:5C2H4+12MnO4-+36H+→12Mn2++10CO2↑+28H2O | |
| D. | 向CH2BrCOOH中加入足量的氢氧化钠溶液并加热: |
分析 A.石炭酸为苯酚,属于弱酸,在离子反应中保留化学式;
B.电子不守恒;
C.遵循电子、电荷及原子守恒;
D.加入足量的氢氧化钠,-Br、-COOH均与NaOH反应.
解答 解:A.石炭酸与NaOH溶液混合的离子反应为C6H5OH+OH-→C6H5O-+H2O,故A错误;
B.稀HNO3洗涤试管中的银镜的离子反应为3Ag+NO3-+4H+═3Ag++NO↑+2H2O,故B错误;
C.乙烯使酸性KMnO4褪色的离子反应为5C2H4+12MnO4-+36H+→12Mn2++10CO2↑+28H2O,故C正确;
D.向CH2BrCOOH中加足量的氢氧化钠溶液并加热的离子反应为CH2BrCOOH+2OH-$→_{△}^{H_{2}O}$CH2OHCOO-+Br-+H2O,故D错误;
故选C.
点评 本题考查离子反应方程式的书写,为高考常见题型,综合性较强,涉及有机物的结构与性质、氧化还原反应等,注重基础知识的考查,选项A为解答的易错点,题目难度不大.


科目:高中化学 来源: 题型:解答题
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度(mol/L) | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
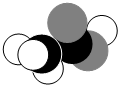
| A. | C2H5OH | B. | CH3COOH | C. | CH3CHO | D. | HCOOCH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
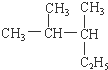 2,3-二甲基戊烷
2,3-二甲基戊烷
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
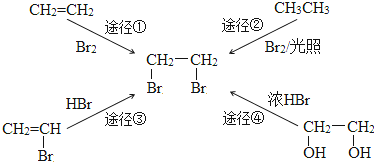
| A. | 途径① | B. | 途径② | C. | 途径③ | D. | 途径④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 若a为浓硫酸,b为Na2SO3固体,c中盛紫色石蕊溶液,则c中溶液变红 | |
| B. | 若a为醋酸溶液,b为贝壳,c中盛过量澄清石灰水,则c中溶液变浑浊 | |
| C. | 若a为浓盐酸,b为MnO2,c中盛品红溶液,则c中溶液褪色 | |
| D. | 若a为浓氨水,b为生石灰,c中盛AlCl3溶液,则c中产生白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗NaOH溶 液的体积(mL) | 20.05 | 20.00 | 18.50 | 19.95 |
| 醋酸浓度 (mol/L) | 0.0010 | 0.0100 | 0.0200 | 0.1000 | 0.2000 |
| pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 熔点:金刚石>食盐>干冰 | B. | 热稳定性:HCl>H2S>PH3 | ||
| C. | 沸点:HF>HBr>HCl | D. | 离子半径:Na+<Mg2+<Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{1}^{2}$H原子的中子数和质子数 | |
| B. | ${\;}_{18}^{36}$Ar原子中的质量数和中子数 | |
| C. | ${\;}_{4}^{8}$Be2+离子中的电子数和质子数 | |
| D. | ${\;}_{12}^{26}$Mg2+离子中的中子数和电子数 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com